Clear Sky Science · ru
Молекулярные механизмы комплексов флотиллинов в организации мембранных микродоменов
Скрытые комнаты на поверхности клетки
Каждая клетка в вашем организме окружена тонкой мембраной, которая на первый взгляд кажется простой, но на деле разделена на бесчисленные крошечные «районы». Эти районы помогают контролировать приём сигналов, поступление питательных веществ и вывод отходов. В этом исследовании показано, как пара долго остававшихся загадкой белков — флотиллины — образует миниатюрные защищённые «комнаты» на внутренней стороне мембраны — структуры, которые могут влиять на такие разнообразные процессы, как клеточная сигнализация, транспорт грузов и даже распространение рака. 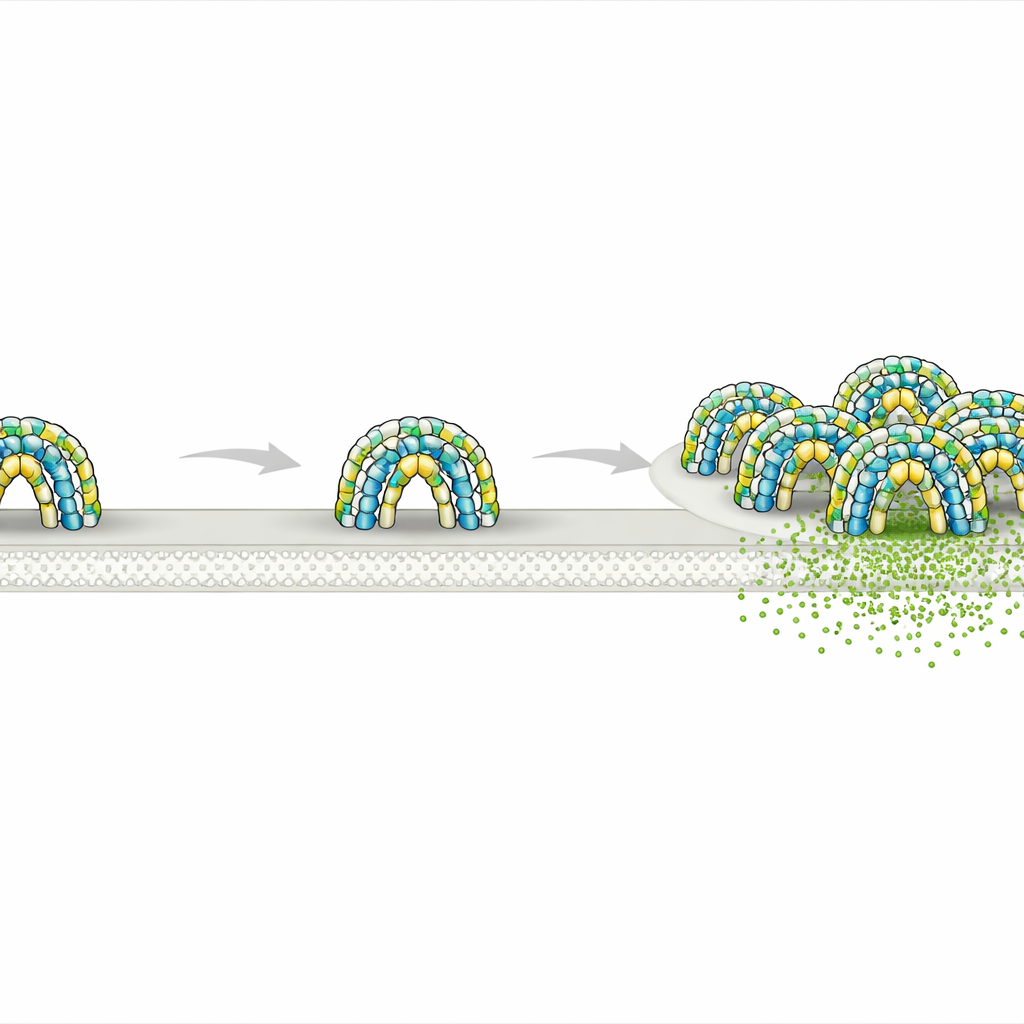
Вглядываясь в крошечные мембранные кварталы
Биологи давно знают, что мембраны клеток не однородны. Липиды и белки группируются в маленькие участки, действующие как временные рабочие площадки для конкретных задач, таких как передача сигналов или сортировка грузов. Флотиллин‑1 и флотиллин‑2 — два белка, которые постоянно маркируют такие участки, образуя яркие точечные структуры на поверхности клетки и участвуя в эноцитозе — процессе поглощения веществ клеткой — а также в сигнальных и трафиковых путях белков. Однако оставалось неизвестным, какую именно форму принимают структуры флотиллина и как они отвоёвывают себе место на мембране.
Купола, ограждающие круги мембраны
Используя высокоразрешающую крио‑электронную микроскопию очищенных человеческих белков, исследователи обнаружили, что флотиллин‑1 и флотиллин‑2 собираются в удивительно крупный комплекс из 44 копий белков, чередующихся между двумя типами. Вместе они формируют жёсткий купол, расположенный на внутренней стороне мембраны. Основание этого купола построено из сегментов, якорящихся в мембране, богатых гидрофобными аминокислотами и липидными присоединениями, которые частично втыкаются в мембрану. Выше расположены длинные спиральные «стебли», образующие плотно упакованную стенку в виде барабана, а крышу составляет череда сцепленных между собой белковых сегментов. Кольцо флотиллина у основания определяет круглый участок мембраны диаметром примерно 30 нанометров — фактически ограждая крошечный диск мембраны и пространство непосредственно над ним.
Гибкие купола в живых клетках
Чтобы проверить, существуют ли такие купола в реальных клетках, команда модифицировала человеческие Т‑клетки так, чтобы те продуцировали флотиллин‑1 и флотиллин‑2 с флуоресцентными метками, а затем визуализировала их сочетанием световой микроскопии и крио‑электронной томографии. Они наблюдали полые куполообразные структуры, прикреплённые к внутренней поверхности плазматической мембраны, очень похожие по форме на те, что были определены в очищенных образцах. Многие купола выглядели немного деформированными или частично раскрытыми; в некоторых внутри обнаруживались дополнительные плотности, вероятно представляющие другие белки, временно захваченные под «крышей». В отдельных участках несколько куполов собирались в сгустки на плоских или изогнутых мембранах, в том числе на эндосомах и небольших внеклеточных везикулах, что указывает на возможность слияния одиночных куполов в более крупные мембранные платформы. 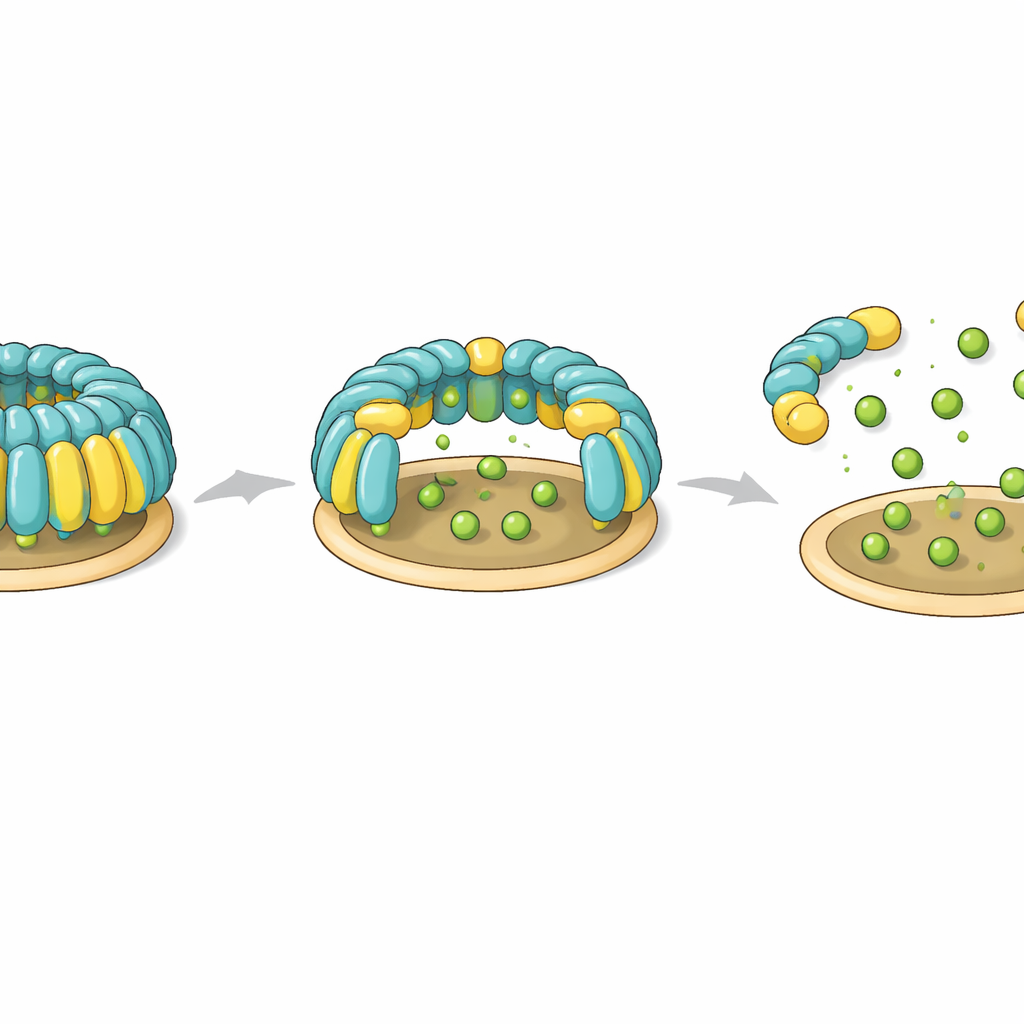
Молекулярный переключатель для сборки и разборки куполов
Исследование также выделяет потенциальный регулятор, который клетки могут использовать для сборки или разрушения флотиллиновых куполов. Две специфические тирозиновые остатки — по одному в каждом флотилллине — расположены в местах, напоминающих петли, которые соединяют основание‑якорь с спиральной стенкой. В составе целого комплекса эти остатки помогают формировать плотное гидрофобное ядро, фиксирующее ориентацию доменов. Когда исследователи вводили мутации, имитирующие добавление отрицательного заряда, как это происходит при фосфорилировании тирозинов ферментами, купол целиком не формировался. Мутации без заряда не нарушали сборку. Эти наблюдения указывают на то, что фосфорилирование в этих «петлевых» точках может выступать обратимым переключателем, дестабилизирующим купол и приводящим к его раскрытию или распаду в процессе, например, флотиллин‑зависимого эноцитоза.
Переосмысление роли этих доменов в формировании мембраны
Ранее флотиллиновые участки чаще рассматривали как «липидные рифы», богатые холестерином и родственными жирами. Удивительно, но при изучении гигантских мембранных пузырей, снятых с клеток, флотиллины предпочитали более жидкие, не‑рифовые области, а не жёсткие, насыщенные холестерином участки. Липидный анализ показал лишь умеренное обогащение одного конкретного молекулы — сфингозина — в комплексах флотиллина, тогда как другие липиды, ассоциируемые с рифами, не концентрировались. Это указывает на иной принцип организации: вместо того чтобы быть пассажирами заранее существующих липидных рифов, флотиллиновые купола сами выступают в роли структурных контейнеров, которые латерально сегрегируют фрагменты мембраны, улавливая определённые белки и липиды в своём ограждённом пространстве.
Почему эта крошечная архитектура важна
Проще говоря, комплексы флотиллина ведут себя как модульные навесы, которые клетки могут разворачивать на своей внутренней поверхности, чтобы отгородить небольшие круглые участки мембраны. Каждый купол может содержать свой уникальный набор партнёрских белков и липидов и, объединяясь с другими, строить более крупные функциональные зоны для сигнализации, сортировки грузов или формирования везикул. Поскольку купола гибки и могут открываться/закрываться, а их сборка чувствительна к фосфорилированию, клетки способны динамически перестраивать эти структуры в ответ на внешние сигналы. Эта работа поэтому переквалифицирует флотиллины из расплывчатых «маркёров рифов» в конкретные архитектурные элементы, помогающие формировать мембрану в специализированные микро‑рабочие пространства.
Цитирование: Lu, MA., Qian, Y., Ma, L. et al. Molecular mechanisms of flotillin complexes in organizing membrane microdomains. Nat Commun 17, 2541 (2026). https://doi.org/10.1038/s41467-026-69197-3
Ключевые слова: флотиллин, мембранные микродомены, крио‑электронная микроскопия, эндоцитоз, липидные рифы