Clear Sky Science · ru
Выживание тканевых макрофагов зависит от митохондриальной функции, регулируемой SerpinB2 при хроническом воспалении
Почему имеют значение иммунные клетки жира
Большинство людей воспринимают жировую ткань как пассивное хранилище, но на самом деле это оживлённая ткань, наполненная иммунными клетками, которые контролируют воспаление и уровень сахара в крови. В этом исследовании показано, как специфическая группа долгоживущих иммунных клеток в глубоком брюшном жире действует как защитник от сахарного диабета 2‑го типа — и как хроническое воспаление при ожирении постепенно уничтожает их, повреждая их «энергетические станции», митохондрии.
Два типа «стражей» жира
Висцеральная жировая ткань — жир вокруг внутренних органов — содержит два основных типа иммунных клеток, называемых макрофагами. Один тип короткоживущий и постоянно обновляется из крови; эти «воспалительные» макрофаги склонны усиливать воспаление и инсулинорезистентность. Другой тип — долгоживущие тканевые макрофаги, которые зарождаются рано в жизни и обычно помогают поддерживать спокойную среду в ткани, способствуют здоровому накоплению жира и повышают общую чувствительность к инсулину. Отслеживая эти клетки у мышей и сравнивая активность генов, исследователи показали, что резидентные макрофаги обогащены генами, снижающими воспаление и повышающими чувствительность к инсулину, тогда как поступающие моноцит‑производные макрофаги экспрессируют гены, ухудшающие контроль сахара в крови.
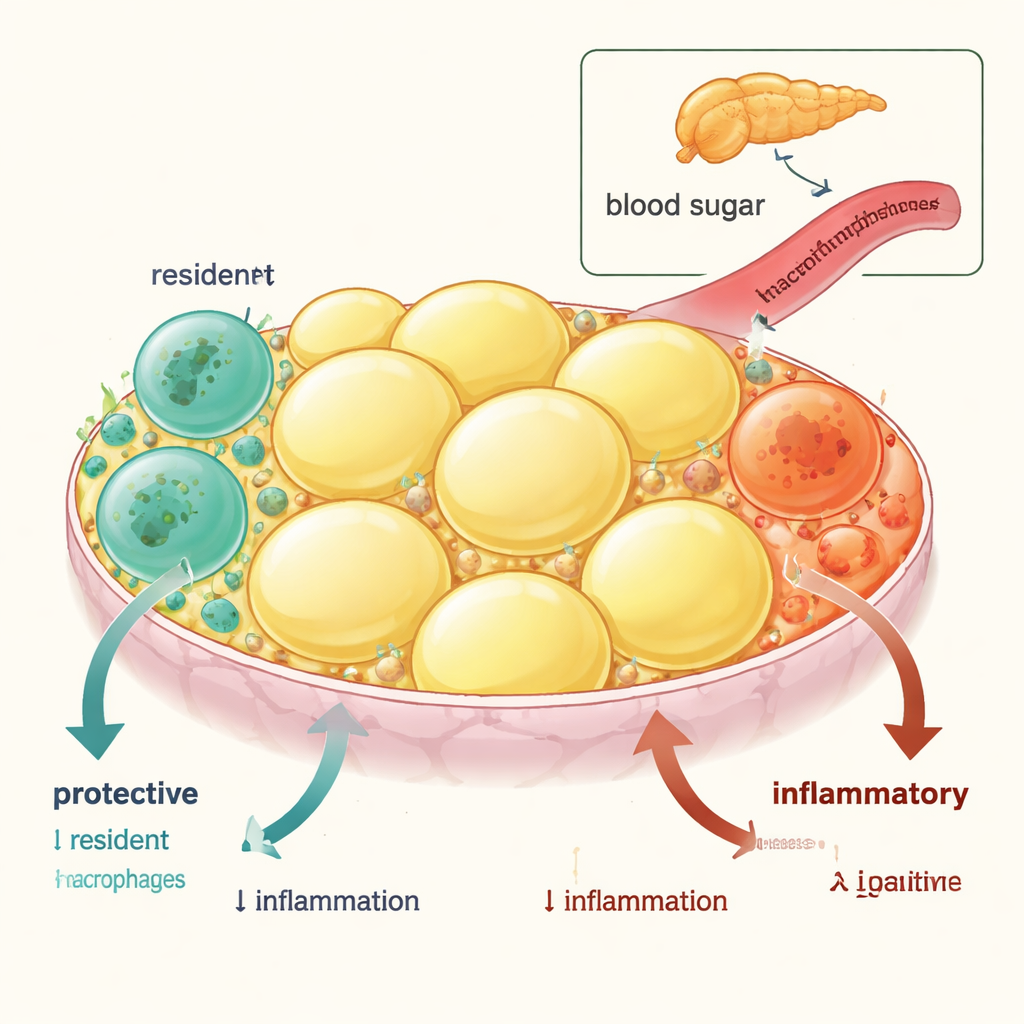
Когда воспаление убивает «хороших»
При ожирении этот защитный баланс меняется. Команда обнаружила, что как у ожиревших мышей, так и у людей с ожирением или диабетом количество резидентных макрофагов в висцеральном жире снижается, в то время как воспалительных макрофагов становится больше. Тщательное визуализирование и маркеры гибели клеток объяснили причину: резидентные макрофаги чаще подвергаются запрограммированной гибели (апоптозу), тогда как воспалительные клетки — нет. Удивительно, что когда ожиревших мышей перевели с высокожировой диеты на обычную, популяция резидентных макрофагов постепенно восстановилась за счёт местного размножения, а метаболическое здоровье улучшилось — что показывает: потеря этих клеток вызвана воспалительным состоянием и обратима.
Одна белковая молекула связывает митохондрии и выживание
Ключевой подсказкой стал белок SerpinB2, прежде всего известный по ролям в свертывании крови. Исследователи обнаружили, что SerpinB2 активно синтезируется в резидентных макрофагах, но гораздо меньше — в воспалительных. При ожирении у людей и мышей резидентные макрофаги резко снижали экспрессию SerpinB2, а более высокий индекс массы тела коррелировал с меньшим числом клеток, положительных по SerpinB2. Эксперименты на клетках с дефицитом SerpinB2 показали повышенную утечку цитохрома c — ключевого белка — из митохондрий в цитоплазму, что является классическим триггером апоптоза. Эти макрофаги с недостатком SerpinB2 имели ослабленные антиоксидантные защиты, больше митохондриальных реактивных форм кислорода (ROS) и повышенное потребление кислорода — все признаки перегруженных, стрессированных митохондрий, которые толкают клетки к воспалительному поведению и гибели.
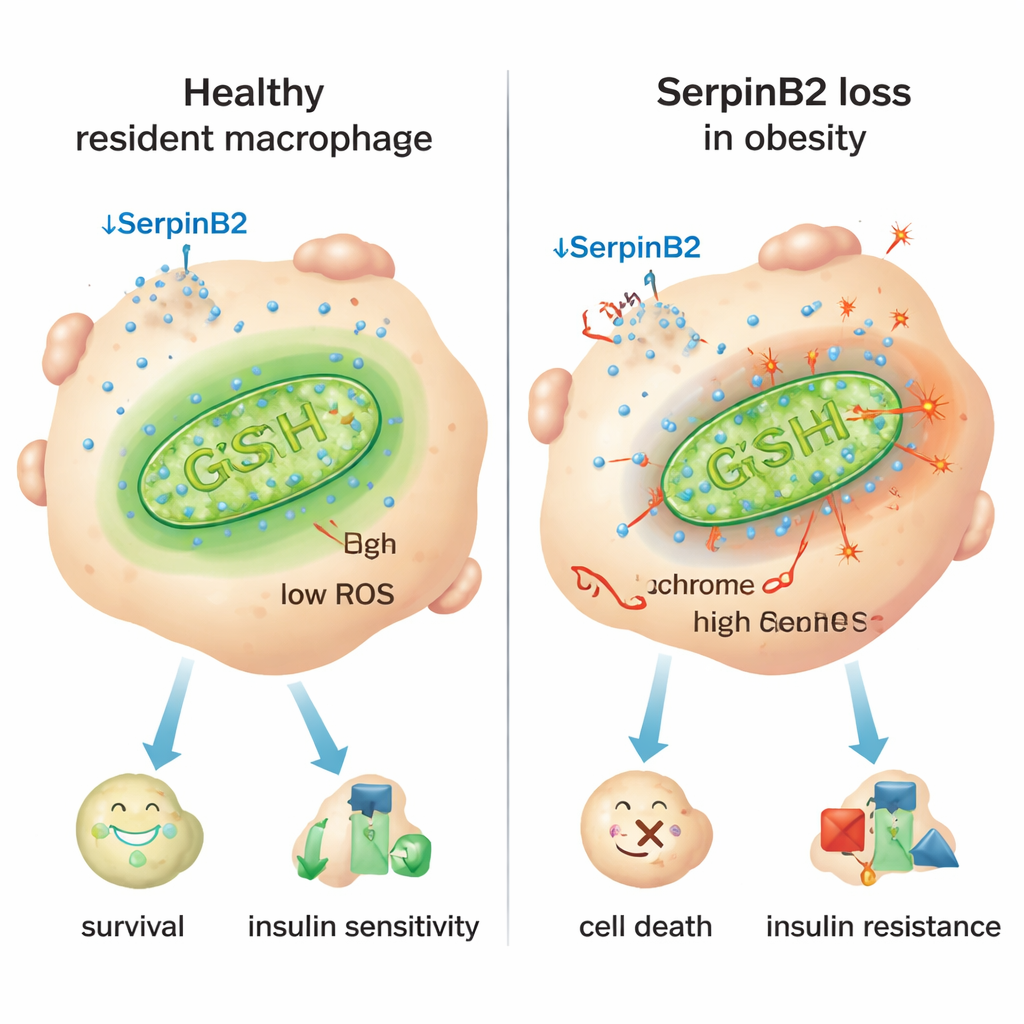
Воспалительный переключатель и возможное решение
Исследование проследило этот митохондриальный стресс до хронических воспалительных сигналов при ожирении, особенно до иммунного медиатора интерферона‑γ (IFN‑γ), который в избытке продуцируется в жировой ткани. IFN‑γ активирует транскрипционный репрессор Икарус (Ikaros), который связывается с контрольной областью гена SerpinB2 и подавляет его. У мышей, у которых миелоидные клетки не могли реагировать на IFN‑γ, резидентные макрофаги сохраняли SerpinB2, лучше выживали, а животные демонстрировали более низкий уровень сахара в крови, улучшенную чувствительность к инсулину и меньшие адипоциты. Напротив, удаление SerpinB2 специально в макрофагах усугубляло нарушение толерантности к глюкозе и инсулинорезистентность, отчасти потому, что жировая ткань становилась более воспалённой и разрасталась. Повышение уровня антиоксиданта глутатиона с помощью добавки N‑ацетилцистеина (NAC) восстановило митохондриальную защиту, спасло выживание резидентных макрофагов, уменьшило адипоциты и улучшило метаболические показатели даже при отсутствии SerpinB2.
Что это значит для метаболического здоровья
Для широкого читателя ключевая мысль такова: не весь жир и не все иммунные клетки в нём вредны. Специализированная группа долгоживущих макрофагов в висцеральном жире защищает нас от неконтролируемого воспаления и высокого уровня сахара в крови, поддерживая здоровье митохондрий посредством антиоксидантных механизмов, зависящих от SerpinB2. При ожирении хронические воспалительные сигналы выключают SerpinB2, митохондрии подвергаются стрессу, эти защитные клетки гибнут, и вместо них приходят более вредные макрофаги, что способствует инсулинорезистентности. Работа указывает, что терапии, направленные на сохранение резидентных макрофагов — блокируя тормоз IFN‑γ/Ikaros на SerpinB2 или поддерживая антиоксидантные защиты на основе глутатиона — могли бы помочь предотвратить или лечить метаболические заболевания, связанные с ожирением.
Цитирование: Vasamsetti, S.B., Sadaf, S., Uddin, M.A. et al. Tissue-resident macrophage survival depends on mitochondrial function regulated by SerpinB2 in chronic inflammation. Nat Commun 17, 1493 (2026). https://doi.org/10.1038/s41467-026-69196-4
Ключевые слова: висцеральный жир, макрофаги, митохондрии, инсулинорезистентность, SerpinB2