Clear Sky Science · ru
Метаболическая инженерия биосинтеза доксорубицина через оптимизацию P450‑редокс‑партнёров и структурный анализ DoxA
Почему происхождение противоракового препарата важно
Доксорубицин — один из ключевых препаратов современной химиотерапии, применяемый при раке крови, опухолях молочной железы и других новообразованиях. И тем не менее, несмотря на десятилетия использования, способ его получения удивительно косвенный: промышленность обычно получает препарат из родственного соединения, вместо того чтобы позволить природному микробу завершить синтез. В этом исследовании объясняют, почему продуцирующая бактерия испытывает трудности на заключительных химических стадиях, и показывают, как перенастройка её внутренней «аппаратуры» резко повышает выход полностью сформированного доксорубицина, открывая путь к более надёжным и потенциально дешевым поставкам.
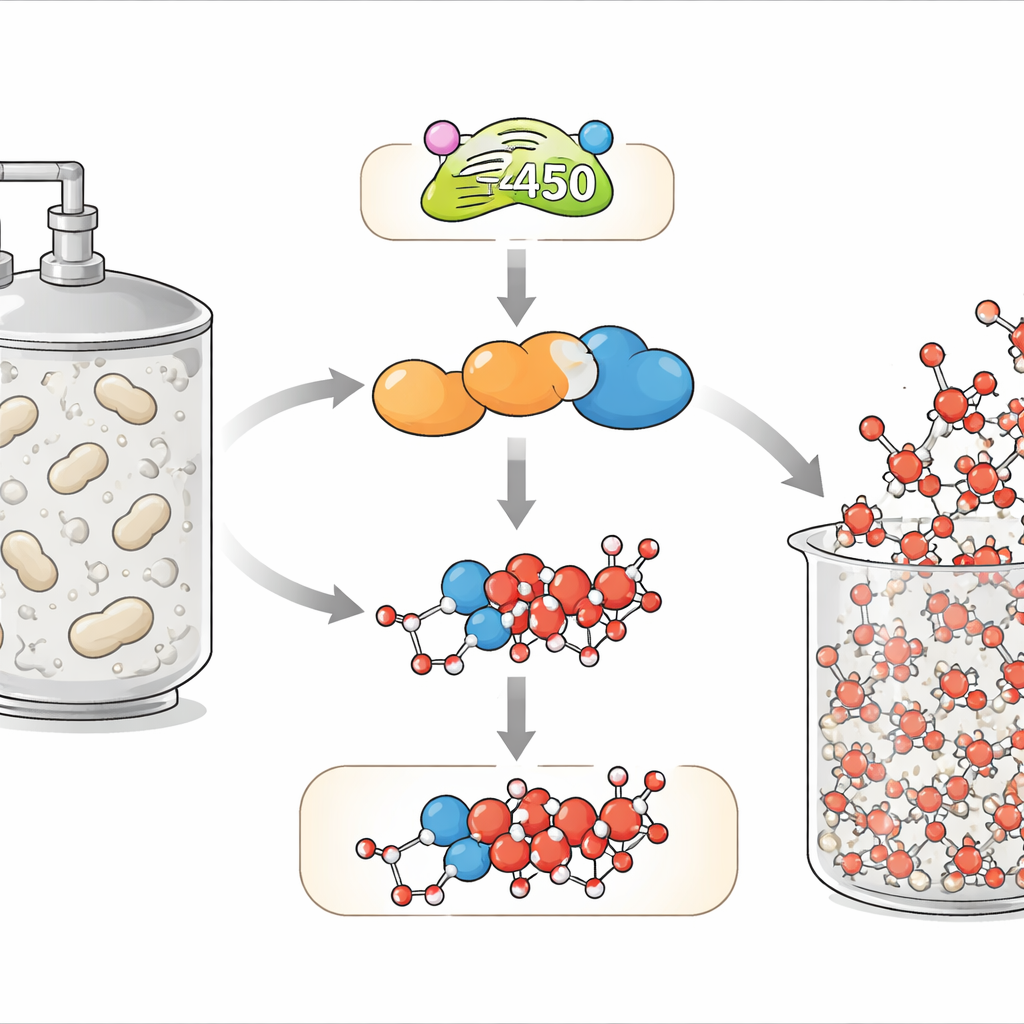
От почвенных бактерий до спасительного лекарства
Доксорубицин относится к антрациклинам — семейству природных молекул, которые синтезируют почвенные бактерии рода Streptomyces. Эти соединения имеют жёсткий плоский углеродный каркас, который вклинивается между основаниями ДНК, и присоединённый сахарный фрагмент, располагающийся в бороздке двойной спирали. Вместе эти элементы блокируют механизмы работы с ДНК в клетке и в конечном счёте приводят к её гибели — свойство, полезное против быстро делящихся раковых клеток. Классический продуцент, Streptomyces peucetius, преимущественно синтезирует предшественник — даунорубицин, и лишь небольшое количество более эффективного доксорубицина, который отличается всего лишь одним дополнительным кислородсодержащим фрагментом. Это крошечное структурное изменение резко повышает активность, но оказывается для микроба неожиданно трудновыполнимым.
Поиск правильной «электропроводки» внутри клетки
Ключевой фермент, выполняющий последние три окислительных шага на каркасе препарата, называется DoxA и принадлежит к семейству цитохромов P450. Как миниатюрная химическая фабрика, DoxA нуждается в стабильном потоке электронов для активации кислорода и внедрения новых кислородных групп в молекулу лекарства. Внутри бактерии эти электроны передаются по цепочке вспомогательных белков, известных как редокс‑партнёры. Геном S. peucetius содержит несколько кандидатур, поэтому изначально было неясно, какие именно работают с DoxA. Сравнивая активность генов и метаболизм в нормальном штамме, мутанте с избытком даунорубицина и мутанте с избытком доксорубицина, исследователи выделили один ферредоксин (Fdx4) и одну ферредоксин‑редуктазу (FdR3) как естественных партнёров. Восстановление этой троицы в пробирочных реакциях подтвердило, что DoxA работает лучше всего, когда подключён к этой конкретной цепочке передачи электронов — подобно тому, как устройство работает правильно только с подходящим адаптером питания.
Освобождение фермента от его собственного замедления
Даже при корректной «электропроводке» DoxA часто задерживается на последнем шаге превращения даунорубицина в доксорубицин. Ранее возникало предположение, что сам продукт может «заклинивать» фермент. Команда обратилась к соседнему гену dnrV, функция которого оставалась неясной. Биохимические тесты показали, что белок DnrV прочно связывает ряд антрациклинов, включая доксорубицин, не подвергая их химическим изменениям. Добавление DnrV в реакции с DoxA значительно улучшало течение реакций, обеспечивая полное превращение предшественников в конечный препарат и предотвращая разрушительные побочные реакции. Практически DnrV действует как внутренняя губка, поглощающая только что образовавшийся доксорубицин и не дающая ему заблокировать фермент или нанести вред ДНК в продуцирующей клетке.
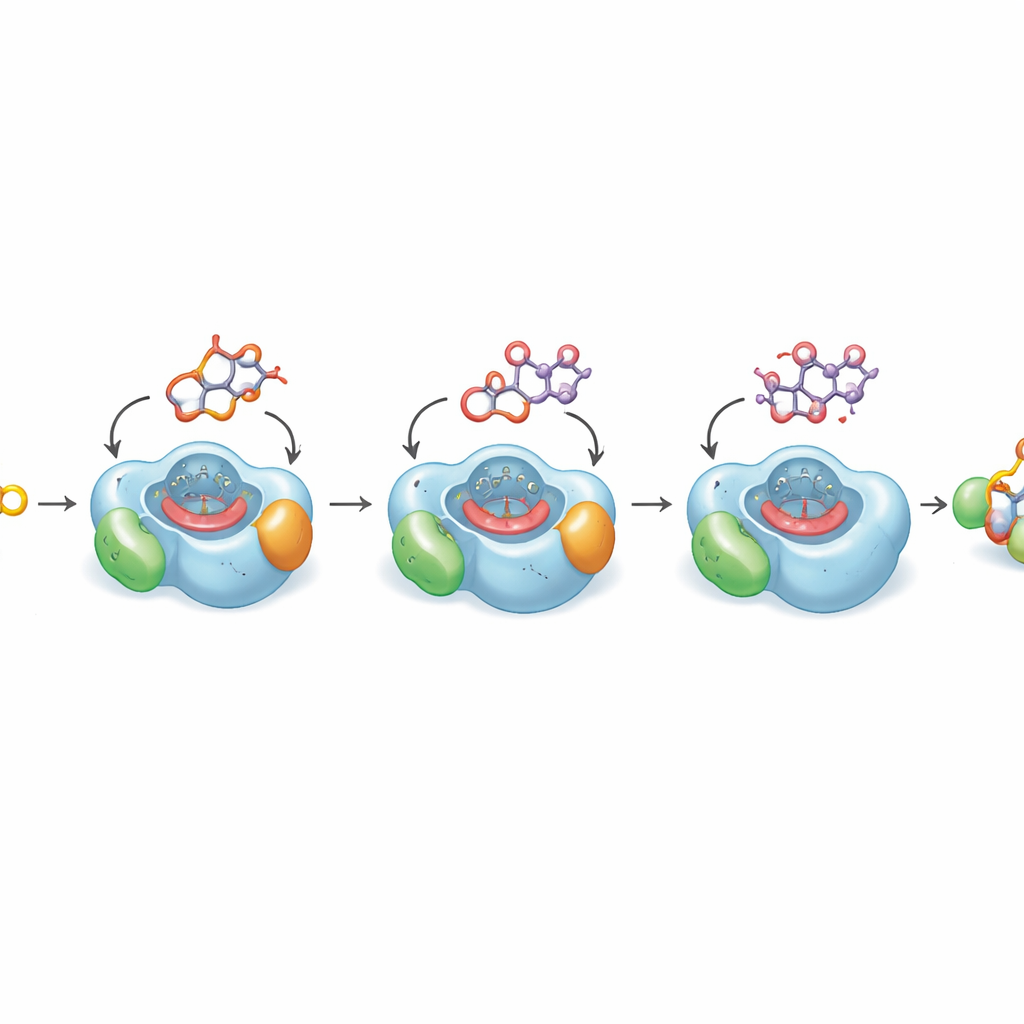
Понимание, почему последний шаг настолько медленный
Чтобы выяснить, почему ключевое заключительное окисление по сути медленное, авторы определили высокоразрешающие кристаллические структуры DoxA в комплексе с тремя последовательными интермедиатами. Эти структуры показывают, как плоское ядро препарата и присоединённый сахар укладываются в плотную полость над гемовой группой фермента — реактивным металлическим центром, который выполняет окисление. Для ранних шагов атом углерода, подлежащий модификации, располагается близко к гему в благоприятной позиции для реакции. Но в финальном субстрате, даунорубицине, фрагмент молекулы, требующий гидроксилирования, сгибается от гема в небольшую маслянистую выемку — конфигурацию, которую квантовые расчёты показывают как энергетически предпочтительную. Компьютерные моделирования на микросекундных временных масштабах подтверждают, что молекула лишь изредка принимает продуктивную позу для последующего введения кислорода. Эта структурная предрасположенность объясняет естественную неэффективность превращения в доксорубицин.
Создание лучшего штамма для производства доксорубицина
Опиравшись на эти данные, исследователи рационально переработали бактерию вместо того, чтобы полагаться на случайную мутagenез. Они ввели ген репарации ДНК для стабилизации производства, затем установили дополнительные копии doxA, оптимальных редокс‑партнёров fdx4 и fdr3, а также полезного связывающего белка dnrV под тщательно подобранными промоторами для балансировки их уровня. Также они оптимизировали условия культивирования и использовали специальные смолы для поглощения токсичных и липких промежуточных продуктов. В лабораторных колбах и в 20‑литровом биореакторе лучший конструированный штамм дал 336 миллиграммов доксорубицина на литр культуры при соотношении доксорубицин:даунорубицин 81:19 — примерно на 180% больше по сравнению со стартовым штаммом и с гораздо более чистой продуктовой смесью.
Что это значит для будущих поставок противоракового препарата
Разобрав как электрическую систему поддержки, так и трёхмерную структуру ключевого фермента, эта работа объясняет, почему медицински важный микроорганизм плохо справлялся с синтезом нашего ценного антрациклина. Сопоставление DoxA с его естественными редокс‑партнёрами, добавление связывающего белка и уравновешивание экспрессии генов превратили вялого продуцента в надёжного производителя. Хотя дальнейшая настройка фермента может ещё более ускорить заключительный химический шаг, исследование уже приблизило полностью биологическое производство доксорубицина к промышленной реальности. Для пациентов и систем здравоохранения такие достижения могут означать более надёжный, масштабируемый и экономически эффективный доступ к одному из основных препаратов химиотерапии.
Цитирование: Koroleva, A., Artukka, E., Yamada, K. et al. Metabolic engineering of doxorubicin biosynthesis through P450-redox partner optimization and structural analysis of DoxA. Nat Commun 17, 2358 (2026). https://doi.org/10.1038/s41467-026-69194-6
Ключевые слова: производство доксорубицина, биосинтез антрациклинов, инженерия ферментов, микробное производство лекарств, цитохром P450