Clear Sky Science · ru
Атипичная протеинкиназа С запускает выведение глюкозы через кишечник при сахарном диабете
Превращение кишечника в «клапан» для сахара
У людей с диабетом в крови циркулирует избыточное количество сахара. Бариатрические операции, такие как желудочное шунтирование, способны удивительно быстро нормализовать уровень глюкозы в крови — ещё до заметной потери веса — но механизмы этого остаются не до конца ясны. В этом исследовании обнаружен кишечный «сахарный клапан» — механизм, при котором кишечник откачивает глюкозу из крови и частично возвращает её в просвет кишки — что указывает на новую мишень для лекарств, способных воспроизвести преимущества операции без хирургического вмешательства.
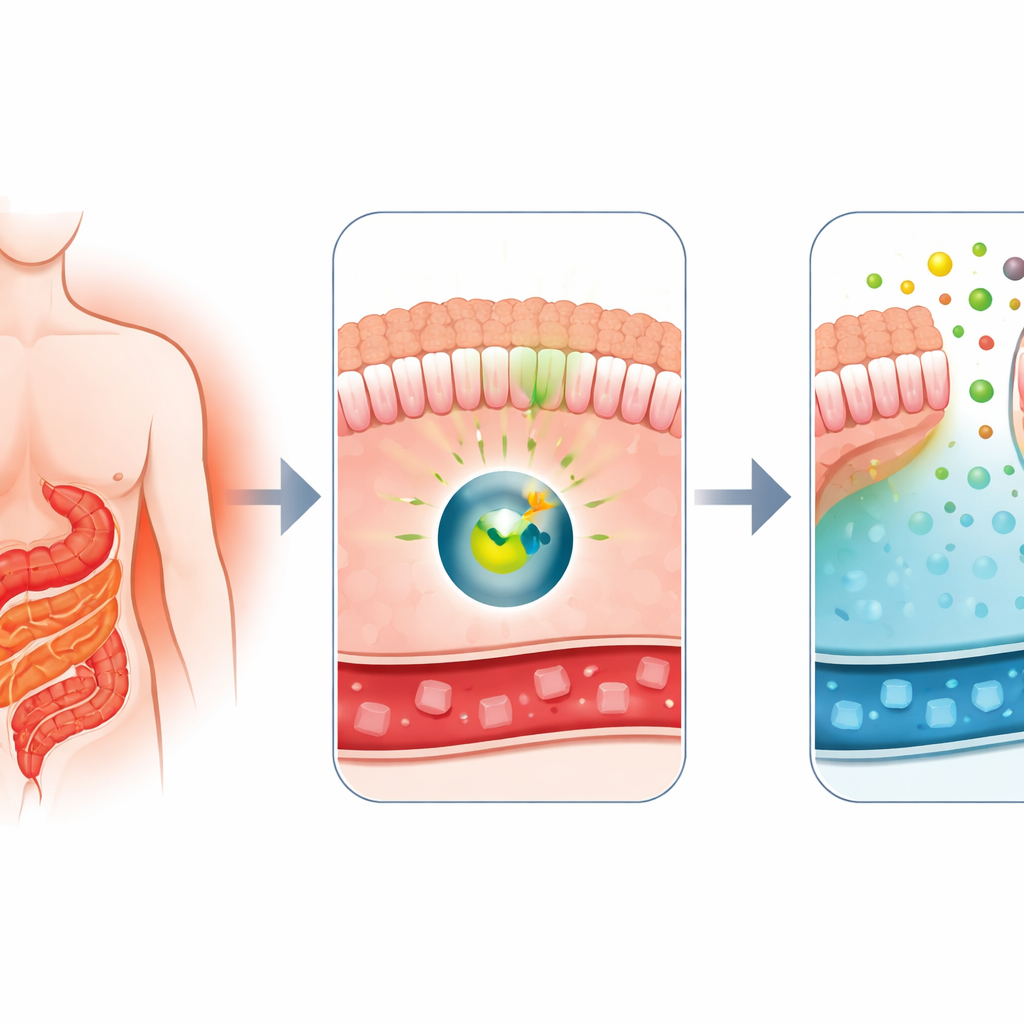
Почему операция быстро меняет уровень сахара в крови
Врачи давно заметили, что рукс-энт-уай (Roux-en-Y) — распространённая операция по снижению веса — также является одним из самых эффективных методов лечения сахарного диабета 2 типа. Вскоре после вмешательства у пациентов часто наблюдается значительное улучшение гликемии, даже до существенной потери массы тела. Ранее эта группа показала, что после шунтирования участки тонкой кишки начинают вести себя как губка: всасывать глюкозу из кровотока и выделять часть её в просвет кишки. Это необычное поведение, называемое выведением кишечной глюкозы, по-видимому, опирается на транспортёр GLUT1. Главный вопрос заключался в том, какой молекулярный переключатель заставляет кишечник перейти в этот режим очистки сахара?
Поиск молекулярного переключателя с помощью больших данных
Чтобы найти этот переключатель, исследователи использовали крупномасштабную вычислительную систему поиска лекарств, основанную на Connectivity Map — базе данных о том, как тысячи веществ изменяют активность генов в клетках. Они сравнивали профили экспрессии генов в пяти ситуациях, при которых выведение кишечной глюкозы было повышено (включая ткани от шунтированных крыс и клетки, обработанные сигналом роста кишечника), с профилями, создаваемыми известными препаратами. Одна группа соединений последовательно выделялась: активаторы протеинкиназы С (PKC), семейства ферментов, передающих сигналы внутри клетки. При дальнейшем изучении команда сосредоточилась на «атипичном» подклассе PKC, особенно на ферменте PKCζ, чья активность в кишечных клетках наиболее полно соответствовала состоянию, напоминающему шунтирование и сопровождающемуся выведением глюкозы.
Как работает «сахарный насос» кишечных клеток
При детальном анализе отдельных кишечных клеток с помощью секвенирования РНК одиночных клеток авторы обнаружили, что шунтирование повышает уровень и PKCζ, и GLUT1 в определённых клетках всасывающего эпителия дистальной части тонкой кишки. В культуре клеток и в человеческих кишечных органоидах искусственное повышение PKCζ или обработка простратином — растительным соединением, безопасно активирующим эти атипичные PKC — стимулировали перемещение GLUT1 на поверхность клетки. На мембране GLUT1 вел себя как двунаправленный насос: он оттягивал больше глюкозы с кровяной стороны клетки и позволял излишкам выходить в просвет кишки. Важно, что такое перенаправление сахара не приводило к значительному увеличению собственных процессов расщепления глюкозы клетками (гликолиза), что указывает на то, что основной эффект — утилизация и удаление глюкозы, а не дополнительное производство энергии.
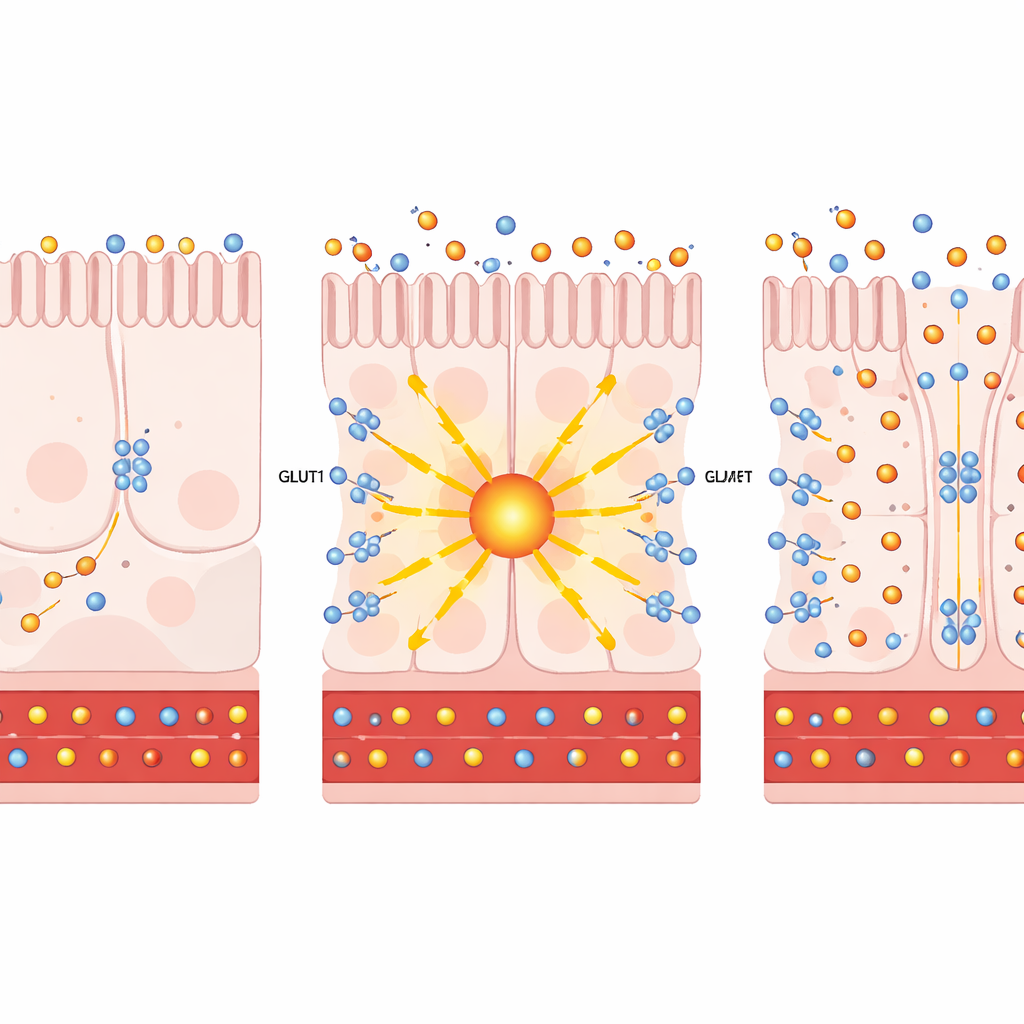
От клеток к мышам: имитация операции без скальпеля
Далее команда проверила, может ли активация этого пути в живых животных улучшать течение диабета. У тучных мышей с инсулинорезистентностью доставка дополнительного PKCζ специально в кишечник приводила к замедленному набору веса, снижению натощаковой гликемии и улучшению толерантности к глюкозе. Радиоактивные маркеры показали усиленное поглощение сахара дистальным отделом кишечника и вымывание его в просвет кишки. Сходные результаты получили и в диабетических моделях мышей при лечении простратином: мыши прибавляли меньше веса, лучше справлялись с нагрузкой глюкозой и перенаправляли больше глюкозы в кишечник, причём без изменений уровня инсулина, потребления пищи или целостности барьера кишечника. На срезах ткани GLUT1 локализовался как на стороне, обращённой к крови, так и на стороне, обращённой в просвет, что делало его идеально расположенным для выкачивания глюкозы из циркуляции и сброса её в кишечник.
Что это может означать для будущего лечения диабета
Для неспециалиста главный вывод таков: кишечник можно превратить в контролируемый путь эвакуации избыточного сахара из крови. Активация определённого фермента внутри кишечных клеток — атипичной PKC — позволяла заставить клетки переместить больше транспортёров GLUT1 на поверхность и функционировать как обратимый сток, оттягивая глюкозу из крови и сбрасывая её часть в просвет кишки. У мышей такое кишечное выведение глюкозы улучшало гликемию и ограничивало набор веса без чрезмерной стимуляции секреции инсулина, изменений аппетита или повреждения кишечника. Хотя простратин и родственные соединения ещё не утверждены как лекарства от диабета, эта работа выделяет путь aPKC–GLUT1 как перспективную мишень для будущих препаратов, которые могли бы частично воспроизвести метаболические преимущества желудочного шунтирования без операции.
Цитирование: Kang, C.W., Hong, ZY., Oh, J.H. et al. Atypical protein kinase C activation drives intestinal glucose excretion in diabetes mellitus. Nat Commun 17, 2417 (2026). https://doi.org/10.1038/s41467-026-69193-7
Ключевые слова: выведение глюкозы через кишечник, сахарный диабет 2 типа, транспортёр GLUT1, атипичная протеинкиназа С, простратин