Clear Sky Science · ru
Могут ли возбужденные феры-оксильные состояния объяснить удлинённые железо‑кислородные связи в каталитических интермедиатах гемовых пероксидаз?
Почему связи между железом и кислородом важны в ферментах
Внутри наших клеток специальные белки — ферменты — используют кислород для безопасного осуществления мощных химических реакций. Среди них гемовые пероксидазы опираются на пару железо–кислород в своём центре, чтобы разлагать перекись водорода, реакционноспособную и потенциально повреждающую молекулу. Десятилетиями учёные спорили о точной природе этой железо‑кислородной связи: ближе ли она по характеру к плотной двойной связи или к более рыхлой одинарной — и что это значит для работы ферментов? В этом исследовании эту загадку решают с помощью ультрабыстрого рентгена и продвинутых расчётов, показывая, что ответ кроется в мимолётных возбужденных состояниях самого железо‑кислородного узла.
Наблюдая фермент в реальном времени
Исследователи сосредоточились на бактериальной пероксидазе, обесцвечивающей красители, — гемовом ферменте, который обычно проходит через два ключевых высокоэнергетических состояния, известных как Соединение I и Соединение II. Оба состояния включают атом железа, связанный с кислородом, и являются центральными для того, как фермент разлагает перекись водорода и окисляет другие молекулы. Предыдущие эксперименты на сходных ферментах дали загадочно большие длины железо‑кислородных связей, что некоторые интерпретировали как следствие изменения активного центра из‑за рентгена или присоединения дополнительного протона. Чтобы избежать таких артефактов, команда использовала временноразрешающую серийную фемтосекундную рентгеновскую кристаллографию на свободно‑электронном рентгеновском лазере, регистрируя дифракцию и рентгено‑эмиссионные сигналы от тысяч маленьких кристаллов белка при комнатной температуре в пределах десятков фемтосекунд — быстрее, чем успевает возникнуть повреждение.
Наблюдение химии внутри кристаллов
В их установке микрокристаллы слегка модифицированной версии фермента смешивали с перекисью водорода непосредственно на движущейся ленте и затем пробовали с задержками от получаса секунды до десятков минут. Ранние временные точки благоприятствуют образованию Соединения I, тогда как поздние — доминированию Соединения II. Структурные данные показали, что в обоих интермедиатах атом железа находится рядом с одним атомом кислорода в кармане гема, а защитные петли белка смещаются, чтобы экранировать этот сильно окислительный центр. Важно, что точные измерения выявили постоянную длину железо‑кислородной связи около 1,83 ангстрема во всех временных точках — длиннее, чем ожидается для классического феррила (Fe(IV)=O) с двойной связью, и ближе к одинарной связи, однако спектральные сигнатуры рентгено‑эмиссии и оптического поглощения ясно указывали на высокие степени окисления, согласующиеся с Соединениями I и II.
Отсечение простых объяснений
Поскольку эксперименты проводили ультракороткими импульсами при комнатной температуре, обычные виновники искажённых длин связей — рентген‑индуцированное восстановление и криогенные артефакты — могли быть в значительной мере исключены. Команда также проверила, не протонировался ли кислород, связанный с железом, превращая двойную связь в гидроксидоподобную одинарную. Однако известные кислотно‑основные свойства сходных гемовых центров вместе с предыдущими химическими исследованиями сильно противоречат такой протонизации в этом типе ферментов. Спектроскопические данные дополнительно показали, что железо остаётся в высокой степени окисления и в низкоспиновом состоянии после реакции с перекисью водорода, как и ожидалось для подлинных ферриловых интермедиатов, подкрепляя идею о том, что неожиданно длинная связь должна возникать вследствие более тонких электронных эффектов, а не простой смены химической формы.
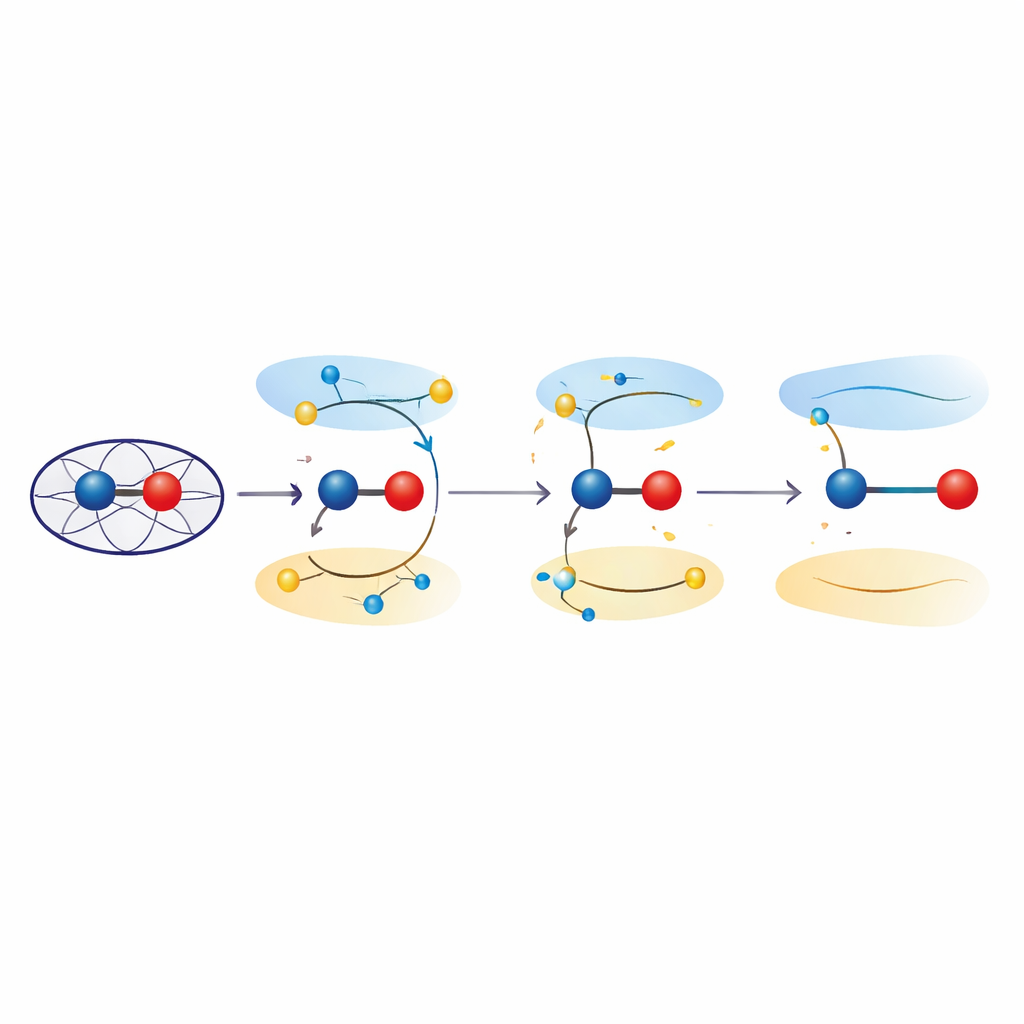
Возбужденные состояния, растягивающие связи
Чтобы исследовать эти эффекты, авторы обратились к квантово‑механическим расчётам как упрощённых моделей, так и полной белковой среды. С помощью временно‑зависимой теории функционала плотности и комбинированных подходов квантовой механики/молекулярной механики они исследовали, как продвижение электронов из связывающих в антисвязывающие орбитали в железо‑кислородном узле изменяет предпочтительную длину связи. Эти возбужденные состояния, энергетически близкие к основному ферриловому состоянию, последовательно давали расстояния железо‑кислород в диапазоне 1,8–1,9 ангстрема — что совпадает с кристаллографическими наблюдениями. Анализ распределения электронов показал, что в этих состояниях пара железо‑кислород перестаёт вести себя как чистая двойная связь Fe(IV)=O и приобретает «ферриц‑оксильный» характер, по сути представляя собой Fe(III), связанное с радикалом, локализованным на кислороде. Квантовая доработка экспериментальных структур подтвердила, что такие описания в терминах возбужденных состояний по меньшей мере так же хорошо согласуются с данными, как и обычные модели основного состояния.
Что это означает для понимания силы ферментов
Проще говоря, работа предлагает, что длинные железо‑кислородные связи, наблюдаемые в этих гемовых пероксидазах, не требуют привлечения повреждения, восстановления или скрытых протонов. Вместо этого они могут возникать естественно, когда ферриловый узел кратко обращается к низкорасположенным возбужденным состояниям, которые ослабляют связь и придают ей ферриц‑оксильный характер. Для неспециалистов это означает, что «рабочая сторона» многих активирующих кислород ферментов может быть более динамичной и электронно гибкой, чем считалось ранее: тонкие сдвиги в распределении электронов изменяют прочность связи и реакционную способность, не меняя общей химии. Признание этих возбужденных состояний может изменить трактовку структурных данных о мощных биологических окислителях и помочь в разработке искусственных катализаторов, которые имитируют или специально настраивают этот деликатный электронный баланс.
Цитирование: Williams, L.J., Kamps, J.J., Brânzanic, A.M.V. et al. Can ferric-oxyl excited states explain elongated iron-oxygen bonds in heme peroxidase catalytic intermediates?. Nat Commun 17, 2324 (2026). https://doi.org/10.1038/s41467-026-69192-8
Ключевые слова: гемовая пероксидаза, ферриловый интермедиат, железо‑кислородная связь, возбужденные электронные состояния, свободно‑электронный рентгеновский лазер