Clear Sky Science · ru
Аутокринный сигнал TGFβ1, запускаемый MerTK, регулирует реакцию микроглии на нейродегенерацию
Как уборочная бригада мозга формирует течение болезни
Когда нервные клетки в мозге и зрительном нерве отмирают, они оставляют после себя завалы обломков. Специализированные клетки иммунной системы — микроглия — выступают в роли уборочной бригады мозга, поглощая эти остатки. Но микроглия делает не только уборку: её реакция может либо защищать нервные цепи, либо усугублять такие заболевания, как болезнь Альцгеймера. В этом исследовании выявлена скрытая петля самосвязи внутри микроглии, которую запускают обломки от погибающих нервных волокон и которая помогает определять, насколько сильно эти клетки откликаются на повреждение.
Триггер, скрытый в умирающих нервных волокнах
Чтобы изучить этот процесс, исследователи использовали модель на мышах, в которой зрительный нерв пережимают, что вызывает дегенерацию длинных отростков зрительных нейронов, не убивая сами тела клеток. Это чисто изолирует последствия распада аксонов. На поверхности этих дегенерирующих волокон жирная молекула выворачивается наружу и действует как сигнал «съешь меня» для близлежащей микроглии. Эти сигналы распознаются рецептором на микроглии под названием MerTK, одним из небольшого семейства белков, которые узнают обломки. Селективно удалив MerTK в микроглии, команда показала, что без этого рецептора микроглия не могла развернуть обычную реакцию на повреждение: она меньше делилась, меньше мигрировала и включала меньше генов, связанных с контролем повреждений и воспалением.
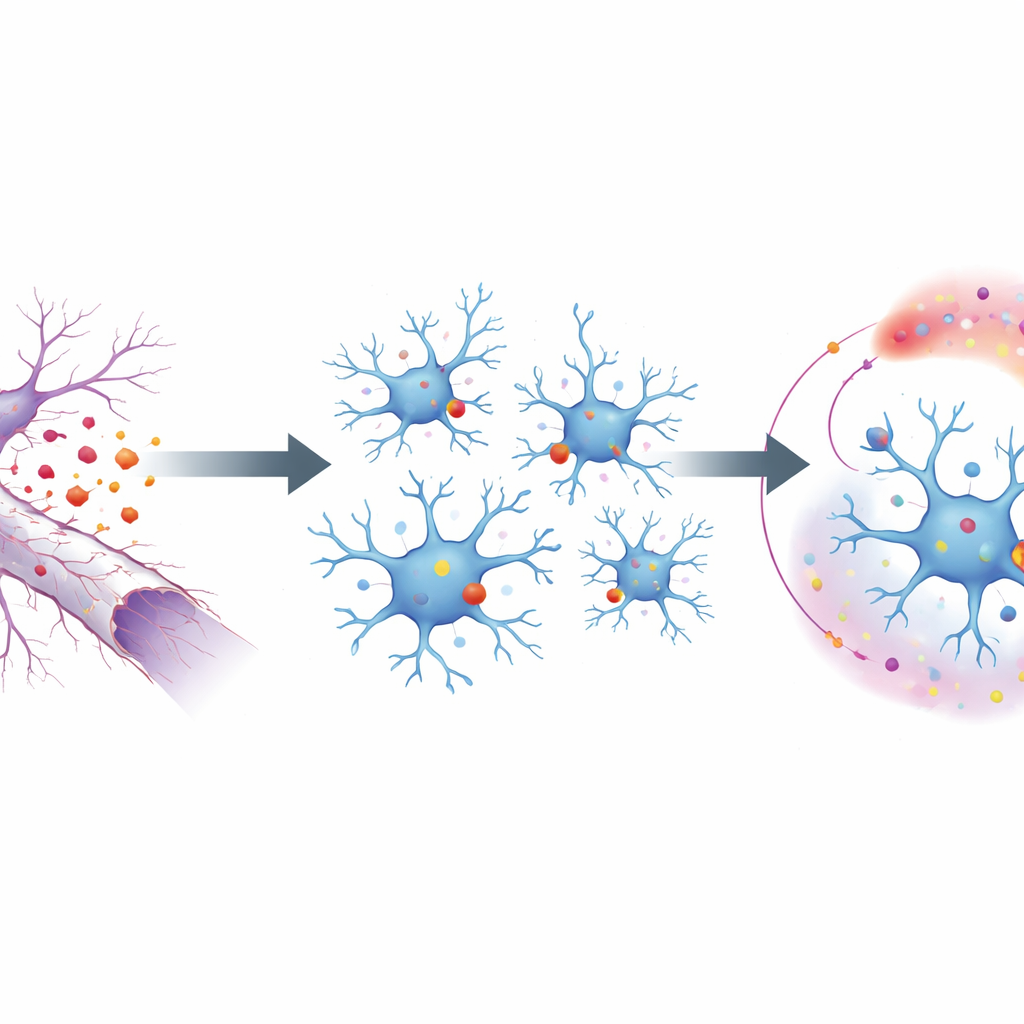
От поверхностного сигнала к генетической перепрограмме
Заглянув внутрь микроглии, учёные проследили, как поверхностный сигнал MerTK преобразуется в изменения активности генов. Они обнаружили, что MerTK активирует молекулярную цепочку, включающую фосфолипазу C, которая, в свою очередь, усиливает работу двух ключевых контрольных белков в ядре — PU.1 и IRF8. Эти факторы действуют как начальники на сборочной линии микроглии, включая множество генов, необходимых для активированного состояния. С помощью карт связывания ДНК команда обнаружила, что PU.1 и IRF8 напрямую связываются со специфическим участком в гене, кодирующем TGFβ1, мощный сигнальный белок. Когда этот участок связывания был мутирован так, что «начальники» больше не могли к нему прикрепляться, микроглия в повреждённых нервах уже не могла увеличить производство TGFβ1, хотя другие базовые функции оставались невредимыми.
Петля самосигнализации в микроглии
Следующий вопрос — что собственно делает TGFβ1 в этом контексте. Исследование показывает, что микроглия синтезирует TGFβ1 и затем сама на него откликается, формируя аутокринную, или самоподдерживающуюся, петлю. Когда TGFβ1 или его рецепторы были генетически удалены только в микроглии, повреждение всё ещё приводило к дегенерации аксонов, но микроглия больше не демонстрировала полный набор программ активации. Она размножалась меньше и выражала меньше генов, отвечающих на повреждение и воспаление, хотя многие маркёры гомеостатической идентичности по-прежнему подавлялись другими сигналами. Ключевой каскадный компонент сигнального пути TGFβ — фосфорилированный SMAD2 — появлялся специфически в микроглиальных ядрах после повреждения и в значительной степени исчезал, когда TGFβ1 или его рецепторы были выведены из строя, что подтверждает разрыв автосигнальной петли.
От зрительного нерва мыши до мозга при болезни Альцгеймера
Чтобы проверить, важен ли этот путь за пределами искусственной модели повреждения, авторы изучили широко используемую модель болезни Альцгеймера на мышах. В этих животных микроглия, скапливавшаяся вокруг амилоидных бляшек, демонстрировала высокий уровень PU.1, IRF8, TGFβ1 и активированного TGFβ-сигналинга, что перекликалось с наблюдениями в зрительном нерве. Затем команда обратилась к человеческим данным одноядрового РНК-секвенирования мозговой ткани пациентов с болезнью Альцгеймера. Там микроглия выделялась как основной тип клеток, экспрессирующий человеческие аналоги MerTK, PU.1, IRF8 и TGFB1. В посмертных срезах мозга пациентов микроглия также проявляла яркие признаки активного TGFβ-сигналинга, в отличие от ткани контрольных доноров. В совокупности эти наблюдения свидетельствуют, что та же самая петля самосвязи действует и при человеческом заболевании.
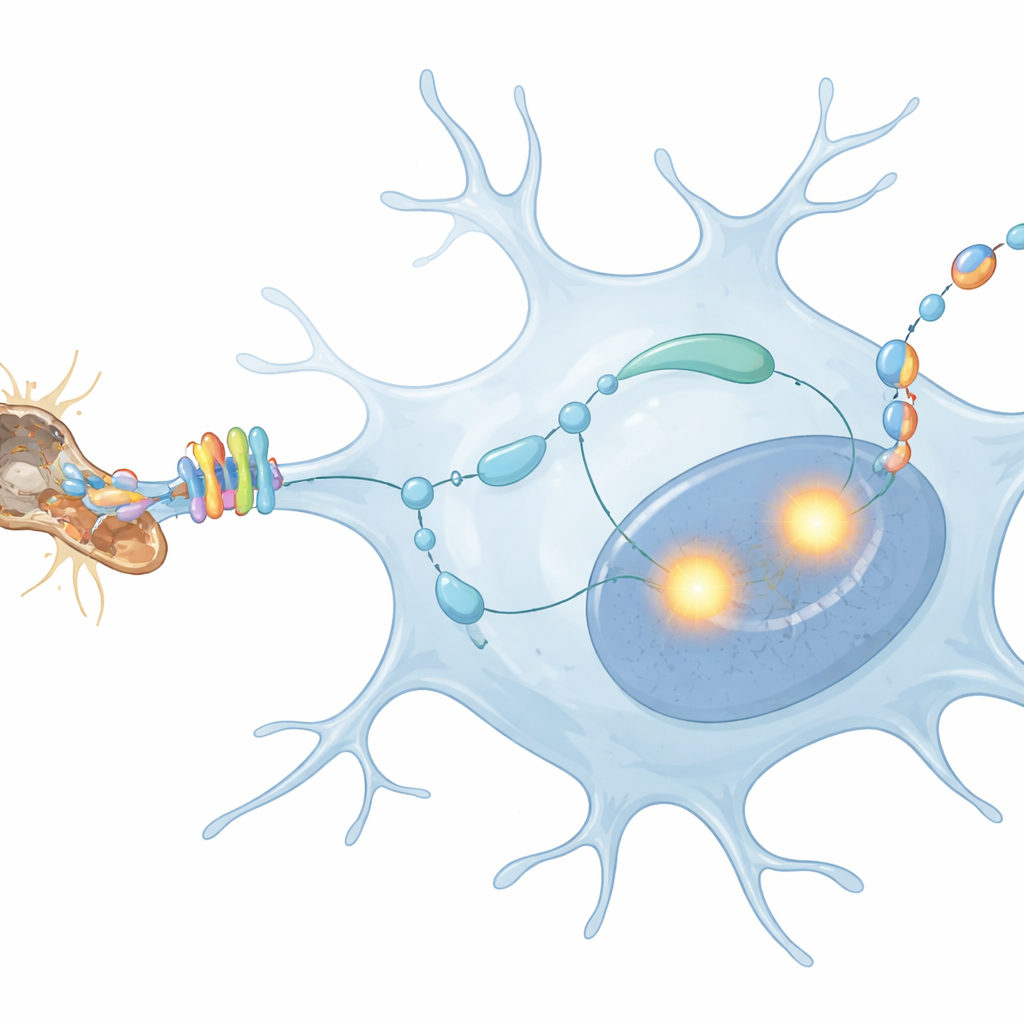
Почему это самопереговоры важны для здоровья мозга
Эта работа раскрывает последовательность событий, в которой обломки дегенерирующих нервных волокон активируют MerTK на микроглии, что затем усиливает PU.1 и IRF8, которые, в свою очередь, побуждают микроглию производить TGFβ1, возвращающийся к самим клеткам. Этот внутренний диалог уточняет и поддерживает их ответ на нейродегенерацию. Для непрофессионала главный вывод таков: уборочные клетки мозга — не просто пассивные чистильщики; они активно прислушиваются к собственным сигналам, и эта петля обратной связи может определять, защитят ли их действия нейроны или приведут к прогрессированию таких заболеваний, как болезнь Альцгеймера. Понимание и возможная тонкая регулировка этой цепочки могли бы открыть новые пути для смягчения вредного воспаления при сохранении полезной уборочной функции микроглии.
Цитирование: Huang, Y., Deng, Z., Zhou, Z. et al. MerTK-triggered TGFβ1 autocrine signal regulates microglial response to neurodegeneration. Nat Commun 17, 2312 (2026). https://doi.org/10.1038/s41467-026-69189-3
Ключевые слова: микроглия, нейродегенерация, болезнь Альцгеймера, воспаление мозга, сигнальная система TGF-бета