Clear Sky Science · ru
Молекулярный фактор низковольтной зависимости инактивации человеческого Nav1.7, выявленный с помощью селективного ингибитора Nav1.7, основанного на эффективности
Уменьшаем громкость болевых сигналов
Почему одни люди испытывают невыносимую боль от легкого прикосновения, а другие почти не чувствуют боли? Большая часть ответа кроется в крошечных белковых «воротах» в наших нервных клетках, которые контролируют электрические сигналы. В этом исследовании показано, как небольшая структурная особенность одного такого «воротца», называемого Nav1.7, делает его особенно важным для запуска болевых сигналов — и как природное соединение Уваригранол D может избирательно его блокировать. Работа указывает на новую стратегию создания обезболивающих, которые подавляют чрезмерно активные болевые нервы, не замедляя работу сердца и не затуманивая мозг. 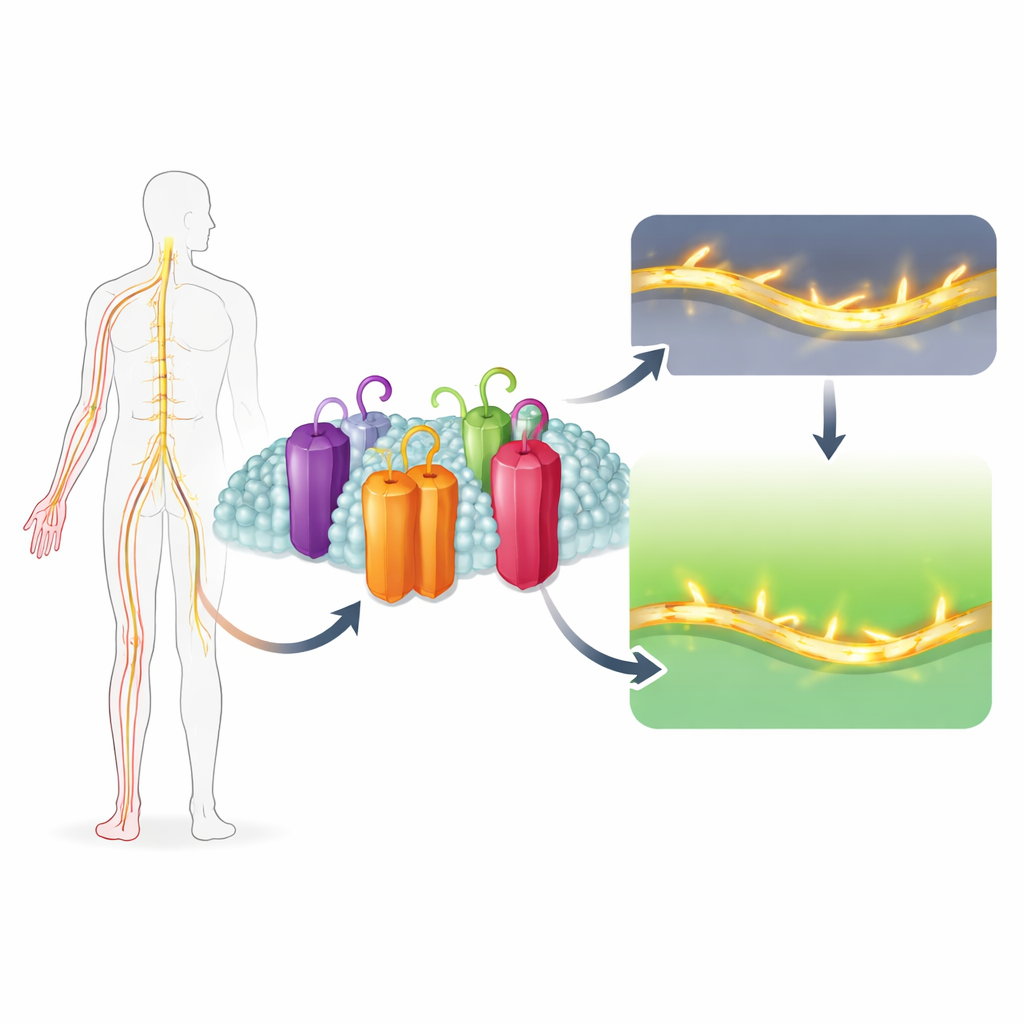
Особый страж боли
Наши нервы генерируют электрические импульсы с помощью натриевых каналов — микроскопических пор, которые кратковременно открываются, позволяя положительно заряженным ионам натрия влиться в клетку. В организме человека существует девять основных вариантов этих каналов, каждый приспособлен к работе в разных тканях — мозге, мышцах, сердце или в ноцицепторах (болевых нервах). Nav1.7 — это вариант, сосредоточенный в периферических болевых волокнах. Он необычен тем, что открывается и закрывается при более низких потенциалах, чем его «родственники», позволяя реагировать даже на очень слабые изменения напряжения. Это делает Nav1.7 мощным усилителем слабых болевых сигналов. Генетические исследования показывают, что гиперактивный Nav1.7 вызывает тяжелые наследственные болевые синдромы, тогда как полностью нефункциональный Nav1.7 делает человека неспособным ощущать боль вовсе.
Поиск селективного блокатора боли
Разработчики лекарств давно надеются нацелиться на Nav1.7 для лечения хронической боли, но он сильно похож на другие натриевые каналы, жизненно важные для работы сердца и мозга. Большинство экспериментальных препаратов связываются с несколькими типами каналов, вызывая побочные эффекты или не давая результатов в клинических испытаниях. Исследователи отобрали более 1500 природных соединений с помощью клеточного теста, отслеживающего изменения мембранного потенциала. Они выделили семейство молекул из растения Uvaria grandiflora, сосредоточившись на соединении, названном Уваригранол D (UGD). UGD ослаблял натриевые токи в нескольких типах каналов, но практически полностью заглушал Nav1.7, тогда как другие натриевые каналы были блокированы лишь наполовину даже при высоких дозах. Это означает, что селективность обусловлена не более сильным связыванием, а гораздо более выраженным эффектом после связывания. 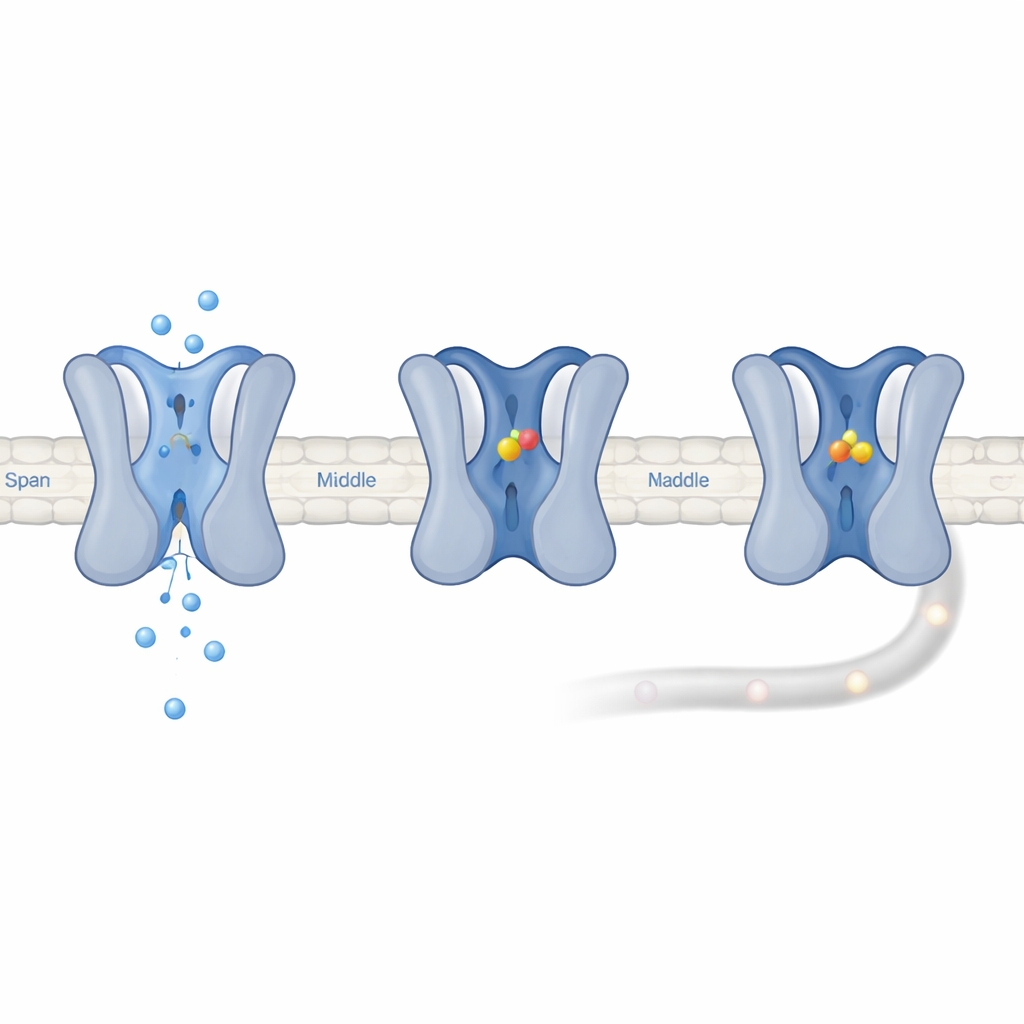
Изменение размером с атом делает Nav1.7 уникальным
Чтобы понять, почему UGD так эффективен в отношении Nav1.7, команда создала химерные каналы, меняя фрагменты между Nav1.7 и близким по структуре мозговым каналом Nav1.2. Это позволило точно локализовать небольшую область у наружного входа поры, между сегментами S5 и S6 в домене III, как ключевой детерминант полного блокирующего действия UGD. Сравнение аминокислотных последовательностей показало, что только в Nav1.7 на позиции 1398 находится треонин, тогда как во всех других человеческих натриевых каналах там стоит более объемный метионин. Когда исследователи заменили треонин в Nav1.7 на метионин, UGD уже не мог полностью закрыть канал; наоборот, замена метионина на треонин в Nav1.2 заставила этот канал вести себя как Nav1.7. Эта одиночная замена также сместила вольтаж активации и инактивации канала: треонин заставлял канал открываться и инактивироваться при более отрицательных потенциалах и делать это быстрее — свойства, которые способствуют тому, что Nav1.7 находится в не-спящем состоянии даже близко к обычному потенциалу покоя ноцицепторов.
Фиксация канала в «пониженном» состоянии
Электрофизиологические записи показали, что UGD не прочно связывается с Nav1.7, когда он закрыт или кратковременно открыт. Напротив, он предпочитает каналы, вошедшие в длительное «медленно инактивированное» состояние, при котором пора закрыта и требуется сотни миллисекунд или больше для восстановления. В присутствии UGD каналы выходили из этого состояния примерно в десять раз дольше, то есть UGD стабилизирует его. Компьютерные моделирования предположили, что UGD устраивается в кармане, образующемся там, где одна петля домена III встречается с α-спиралью домена IV, устанавливая ключевые контакты с пятью аминокислотами. Мутации любого из этих остатоков ослабляли эффект UGD, подтверждая важность этого кармана. Поскольку треонин в Nav1.7 способствует переходу в инактивированные состояния при более низких потенциалах, большая доля его каналов находится в том самом состоянии, к которому UGD предпочитает привязываться, что объясняет, почему функциональное подавление Nav1.7 значительно сильнее, чем у родственных каналов, несмотря на сходную силу связывания.
От ионных пор к облегчению боли
В конечном счете важно то, как эти молекулярные события влияют на реальные клетки. В нейронах дорсального корешкового ганглия крыс, чувствительных к боли, UGD существенно снизил число потенциалов действия — быстрых скачков напряжения, несущих болевую информацию — и в конечном итоге полностью остановил их при низких микромолярных и субмикромолярных концентрациях. Напротив, клетки, напоминающие по свойствам человеческую сердечную ткань и полученные из стволовых клеток, которые в основном используют другой натриевый канал (Nav1.5) и имеют несколько более отрицательный потенциал покоя, были примерно в 60 раз менее чувствительны. Это указывает на то, что «эффикасно-селективный» блокатор, подобный UGD, может сильнее подавлять болевые пути по сравнению с сердечной или другой возбудимой тканью просто из-за того, как часто Nav1.7 находится в своем инактивированном состоянии, благоприятном для связывания препарата.
Что это значит для будущих методов лечения боли
Исследование показывает, что небольшая структурная деталь — одиночный треонин — лежит в основе низковольтного поведения Nav1.7 и его способности генерировать «пороговые токи», те крошечные сигналы, которые решают, выстрелит ли болевая клетка. Связываясь и стабилизируя инактивированную форму этого канала, UGD эксплуатирует это врожденное свойство и подавляет Nav1.7 значительно сильнее, чем другие натриевые каналы. Для неспециалиста вывод ясен: авторы выявили точную уязвимость в «стражнике» боли организма и продемонстрировали способ задействовать ее, не вмешиваясь значительно в работу сердечных или мозговых каналов. Этот инсайт открывает путь к разработке новых обезболивающих, которые умеют «тихо» успокаивать чрезмерно активные болевые нервы, нацеливаясь на поведение напряжения и состояние канала, а не только на более плотное связывание с Nav1.7.
Цитирование: Zhao, F., Xi, C., Li, J. et al. Molecular determinant of low-voltage dependence of human Nav1.7 inactivation revealed by efficacy-based Nav1.7 selective inhibitor. Nat Commun 17, 2559 (2026). https://doi.org/10.1038/s41467-026-69184-8
Ключевые слова: натриевый канал Nav1.7, хроническая боль, Уваригранол D, зависимое от состояния ингибирование, вольт-чувствительные натриевые каналы