Clear Sky Science · ru
Редокс-управляемый механизм Na+-насоса NADH-хинон-оксидазы Vibrio cholerae зависит от динамических конформационных изменений
Как энергетическая установка холеры стала мишенью для лекарств
Бактерия, вызывающая холеру, Vibrio cholerae, выживает и размножается за счёт миниатюрной молекулярной энергетической установки в собственной клеточной мембране. В этом исследовании в беспрецедентных деталях показано, как один из её ключевых «двигателей» — фермент Na⁺-NQR — меняет форму в процессе насасывания ионов натрия изнутри клетки наружу. Понимание этой молекулярной машины не только удовлетворяет фундаментальное любопытство о том, как жизнь превращает питание в пригодную энергию, но и указывает новые пути для проектирования антибиотиков, которые блокируют вредные бактерии, не затрагивая клетки человека.
Двигатель на натриевом топливе в бактериях
Многие морские и патогенные бактерии полагаются на Na⁺-NQR как на первый этап своей дыхательной цепи — серии реакций, извлекающих энергию из питательных веществ. Na⁺-NQR расположен в внутренней мембране и принимает электроны от молекулы топлива NADH, передавая их по цепочке окрашенных «помощников» (коферментов) к хинону, другой малой молекуле в мембране. По мере потока электронов фермент использует эту энергию для выталкивания ионов натрия (Na⁺) изнутри клетки наружу, создавая натриевый градиент. Этот градиент похож на заряженную батарею: он приводит в действие флагеллярный мотор для плавания, помогает синтезировать АТФ (энергетическую валюту клетки) и обеспечивает захват питательных веществ и выведение лекарств. Поскольку Na⁺-NQR встречается только в бактериях и существенно отличается от родственного фермента в наших митохондриях, он является привлекательной мишенью для высокоселективных антибиотиков.
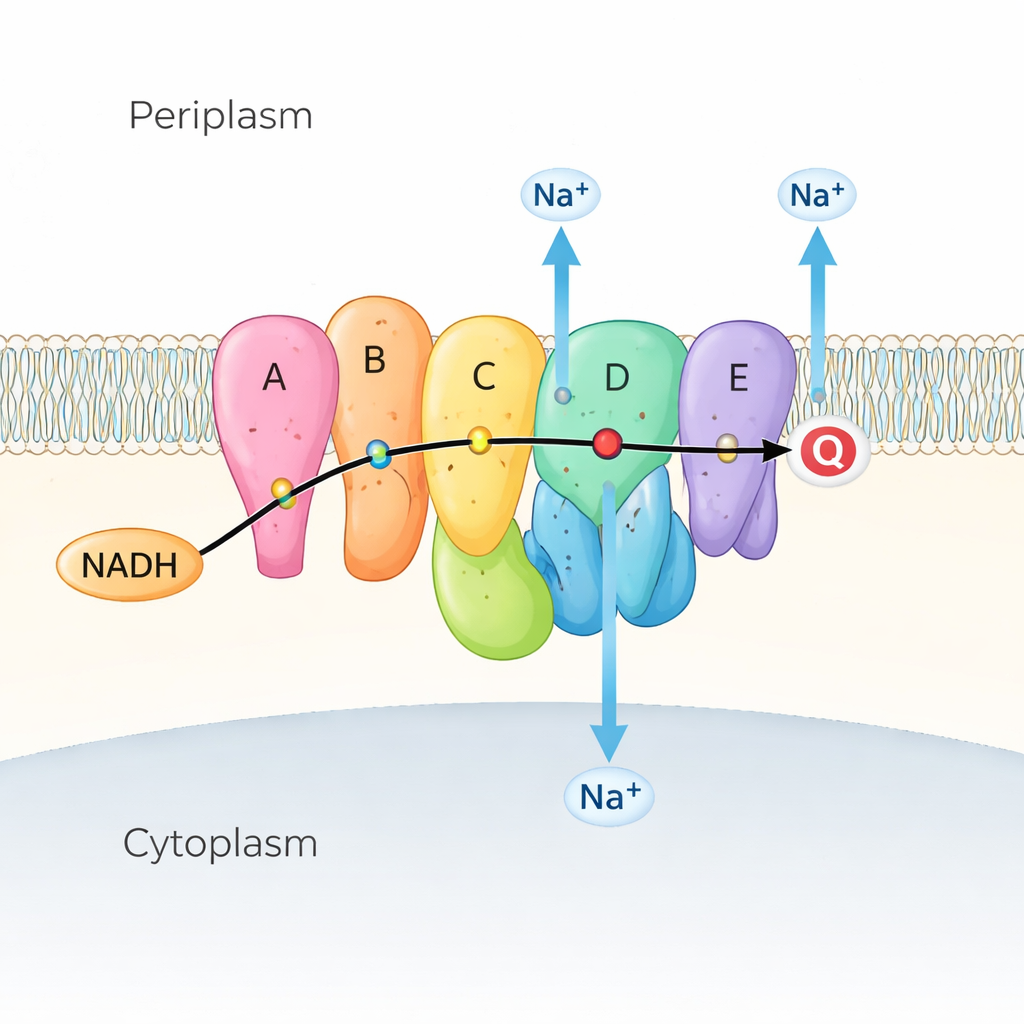
Наблюдая за движением машины
Предыдущие снимки методом рентгеноструктурного анализа и крио-электронной микроскопии показали расположение субъединиц и коферментов Na⁺-NQR, но также выявили загадку: некоторые критические перепрыгивания электронов оказались слишком дальними для эффективной передачи, если белок не меняет свою форму. Авторы решили эту проблему, зафиксировав Na⁺-NQR в множестве слегка различных состояний. Они использовали мутанты, удаляющие конкретные коферменты, препараты, останавливающие реакцию на отдельных стадиях, и растворы с натрием и без него. С помощью крио-ЭМИ высокого разрешения и продвинутого анализа изображений им удалось разделить и реконструировать несколько конформаций одного и того же фермента, фактически превратив статические снимки в фильм рабочего цикла.
Гибкая «рука» и шатающийся зажим
Одно ключевое открытие касается гибкой цитоплазматической субъединицы NqrF, которая удерживает два электронопереносных кофермента. Команда выявила три положения её «ферредоксиноподобного» домена — получившие прозвища «вверх», «среднее» и «вниз». В редком, но критически важном «вниз» состоянии этот малый домен размахивает в карман, образованный двумя мембранными субъединицами, NqrD и NqrE, поднося свой железо–серный кластер достаточно близко для передачи электрона дальше. Тем временем периплазматическая (внешняя) субъединица NqrC ведёт себя как подвижный зажим. В одной конформации («стабильная») она прижимается к другой мембранной субъединице, NqrB, расположенной так, чтобы передавать электроны к конечному хиноновому акцептору. В другой («сдвинутая») конфигурации NqrC смещается к NqrD/E, подводя свой флавиновый кофермент ближе, чтобы принять электрон от их железо–серного центра. Эти перемещения показывают, что NqrF и NqrC действуют как динамичные курьеры, заполняя большие разрывы в цепочке коферментов.
Как изменения формы прокачивают натрий
Сердце натриевого насоса сосредоточено в паре субъединиц NqrD и NqrE, которые образуют центральный пучок спиралей, пронизывающих мембрану. На основе структур и молекулярно-динамических симуляций на атомном уровне авторы показывают, что когда железо–серный кластер в NqrD/E восстанавливается (принимает электрон), появляется отрицательно заряженное место, притягивающее ион Na⁺ и несколько молекул воды с цитоплазматической стороны, образуя временный связывающий карман. Гидрофобные аминокислоты над и под этим карманом ведут себя как внутренние и внешние ворота, контролируя доступ к иону. Когда NqrD/E переходят из «внутренне-открытого» в «внешне-открытое» состояние, Na⁺ смещается в сторону периплазмы и в итоге высвобождается по мере реокисления железо–серного кластера. Симуляции показывают, что Na⁺ остаётся частично гидратированным, но не встречает непрерывного водного туннеля, что указывает на плотную герметизацию фермента против нежелательных утечек протонов.
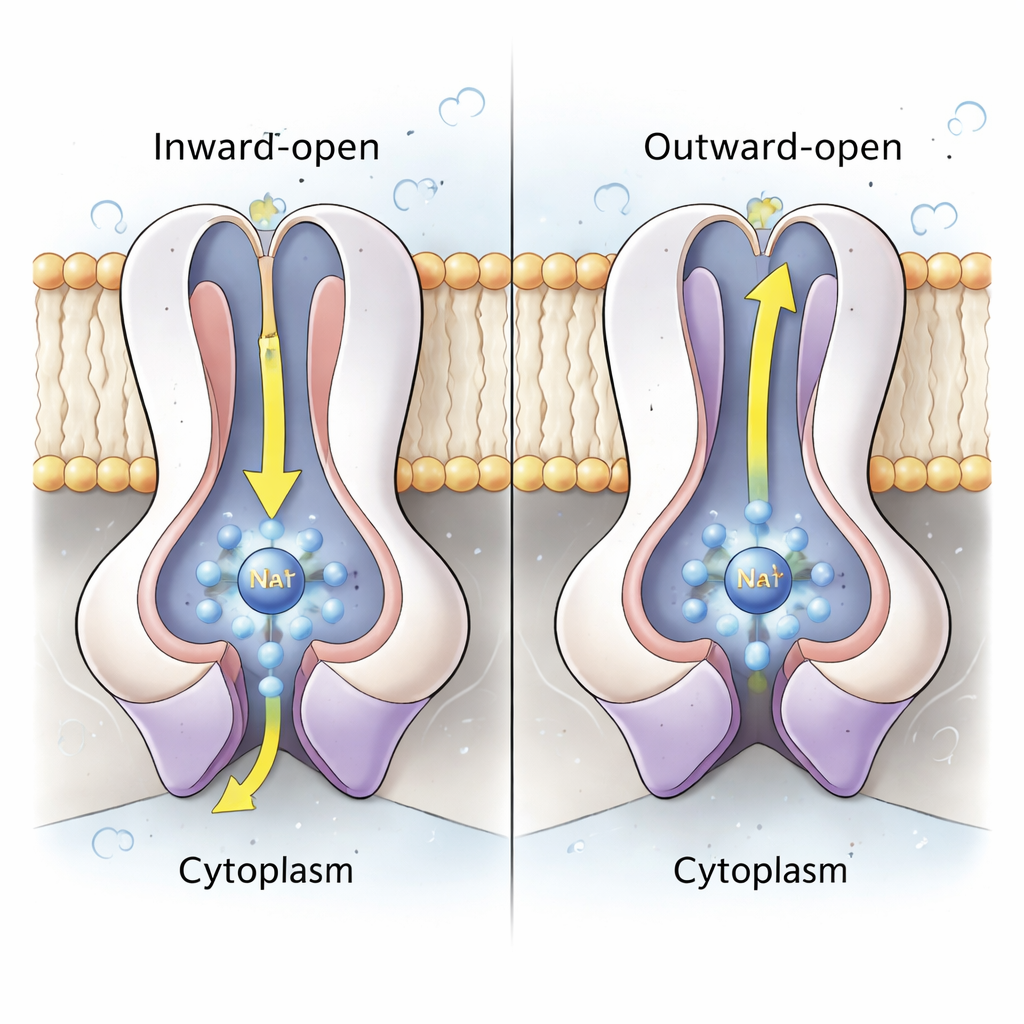
Координированный цикл, который фиксирует направление
Объединив все структурные состояния и симуляции, исследователи предлагают шестиступенчатый цикл. Сначала NADH связывается и отдает электроны NqrF, который затем передаёт один электрон NqrD/E, что запускает захват Na⁺ из цитоплазмы и заполнение центрального кармана. Результирующий конформационный переход NqrD/E в наружне-открытую форму одновременно выталкивает Na⁺ в периплазму и способствует тому, чтобы NqrC перешла в положение для приёма электрона. Последующие шаги передают электроны к конечным флавиновым и рибофлавиновым коферментам и, наконец, к хинону, который должен принять два электрона, чтобы стать хинолом. Важно, что те же изменения формы, что перемещают Na⁺, также попеременно разрыхляют и упрочняют NqrF и NqrC, делая прямой поток электронов вероятным только тогда, когда Na⁺ выкачивается наружу, и предотвращая обратное проскальзывание. Эта связь помогает ферменту прокачивать Na⁺ против существующего градиента, поддерживая батарею бактерии в зарядe.
Почему это важно для медицины и биологии
Для неспециалиста эта работа демонстрирует, как жизнь создаёт тонко скоординированные машины из белков, где крошечные изменения зарядов вызывают большие полезные движения. Для исследований инфекционных болезней она проясняет, что перемещение Na⁺ в Na⁺-NQR происходит в основном через сердцевину NqrD/E, а не через ранее подозреваемую субъединицу NqrB. Это понимание уточняет, где будущие препараты должны связываться, чтобы наиболее эффективно нарушать двигатель Vibrio cholerae и других патогенов, при этом щадя человеческие ферменты. В более широком смысле исследование предоставляет структурный план того, как редокс-реакции могут быть увязаны с ионной перекачкой — принцип проектирования, который природа многократно использует в различных биоэнергетических системах.
Цитирование: Ishikawa-Fukuda, M., Seki, T., Kishikawa, Ji. et al. The redox driven Na+-pumping mechanism in Vibrio cholerae NADH-quinone oxidoreductase relies on dynamic conformational changes. Nat Commun 17, 1394 (2026). https://doi.org/10.1038/s41467-026-69182-w
Ключевые слова: натриевый насос, бактериальное дыхание, Na+-NQR, крио-ЭМИ, мишени для антибиотиков