Clear Sky Science · ru
Синтетическая система для РНК‑чувствительного пироптоза на основе нуклеазы‑протеазы CRISPR типа III‑E
Превращая смертоносные взрывы клеток в целевые инструменты
Наш организм иногда защищается, заставляя инфицированные или повреждённые клетки взрываться в виде воспалительного самоуничтожения. Этот взрыв не только устраняет опасные клетки, но и привлекает иммунную систему. Новое исследование представляет синтетическую генную схему, названную DAMAGE, которая может «читать» РНК‑сообщения внутри клетки и решать, должна ли эта клетка быть уничтожена. Соединив микроорганизмную систему защиты с нашей собственной машинерией гибели клеток, авторы показывают способ выборочно уничтожать инфицированные вирусом, раковые или старые клетки, щадя здоровые соседние клетки. 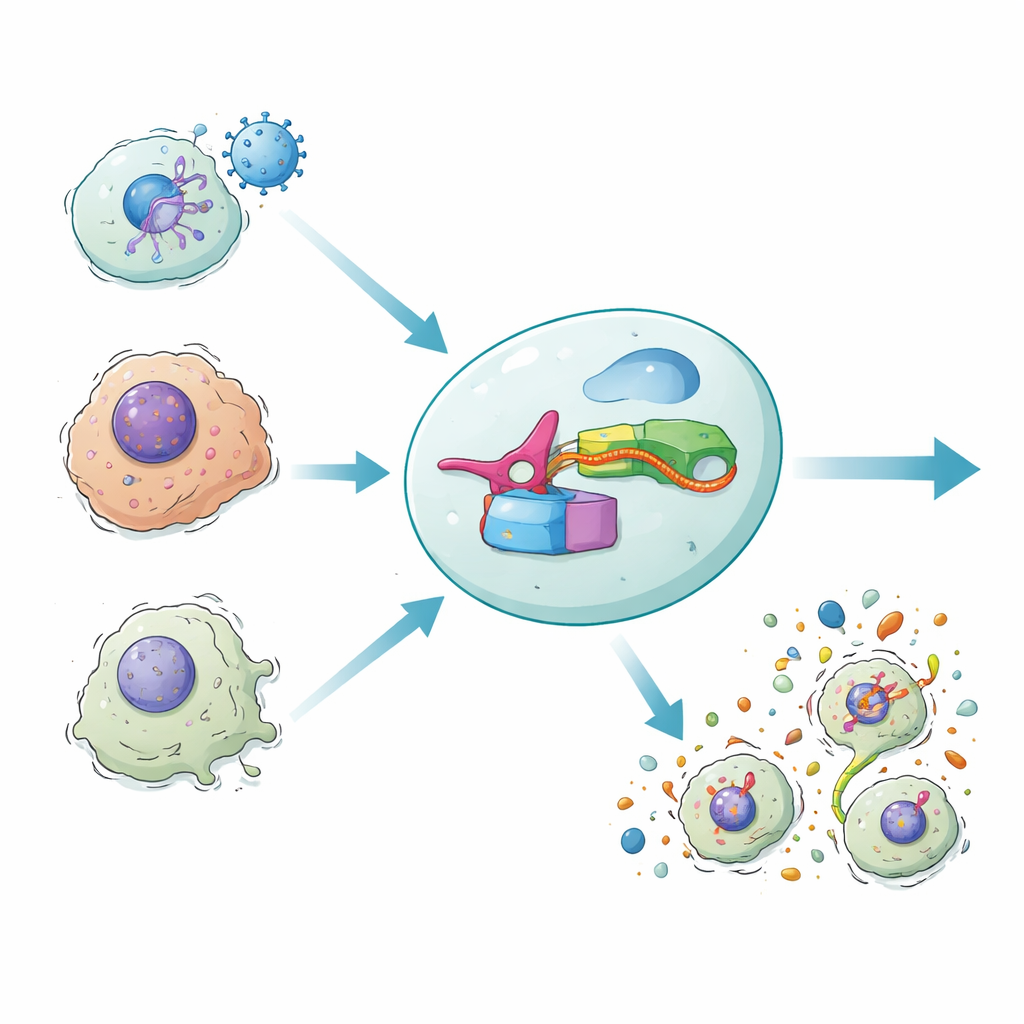
Как клетки обычно взрываются
При воспалительной гибели клеток семейство белков, известных как газдермины, находится внутри клетки подобно заряду. Каждый газдермин имеет «убийственную» переднюю половину, которая может пробивать мембраны, и «запирающую» заднюю половину, которая держит убийцу под контролем. Когда иммунные сенсоры распознают угрозу, ферменты разрезают газдермины пополам, освобождая переднюю часть для сборки пор в плазматической мембране. Клетка разбухает, разрывается и выбрасывает сигнал тревоги, который мобилизует иммунные клетки. Этот мощный ответ помогает бороться с инфекциями и опухолями, но его естественная сеть регулирования сложна и трудно поддаётся перепрограммированию для терапии.
Заимствование бактериальной защиты для чтения РНК
Бактерии развили компактные модули защиты, ныне известные благодаря технологиям CRISPR. Одна из таких систем, типа III‑E, использует белок Cas7‑11, который с помощью короткой направляющей РНК связывается со специфическими РНК‑последовательностями. Когда Cas7‑11 обнаруживает совпадающую мишень, он включает сопряжённый фермент Csx29, который разрезает партнёрный белок Csx30. Авторы поняли, что Csx30 может служить настраиваемым «шарниром» между любыми двумя фрагментами белка. Они встроили этот шарнир между убийственной и запирающей половинами человеческих газдерминов, создав искусственные исполнители, которые расщепляются только тогда, когда сенсор, подобный CRISPR, обнаруживает выбранную РНК внутри клетки.
Программируемый выключатель смерти для больных клеток
Эта конструкция, названная DAMAGE (Death Manipulation Gene), состоит из пяти частей: сенсора Cas7‑11, расcекателя Csx29, фьюз‑белка газдермин–Csx30, направляющей РНК и целевой РНК внутри клетки. Когда появляется нужное РНК‑сообщение, Cas7‑11 связывается с ним, активирует Csx29, и Csx29 разрезает шарнир Csx30 в фьюз‑белке. Убийственная половина газдермина освобождается, формирует поры в мембране, и клетка умирает в воспалительном взрыве. Простым изменением направляющей РНК команда перенаправила DAMAGE на разные клеточные цели. Они показали, что система распознаёт РНК респираторно‑синцитиального вируса, высоко рискованный вирус папилломы человека в клетках шейки матки и несколько ракообразующих мутаций KRAS, отличающихся от нормальной РНК лишь одной буквой. В каждом случае клетки, содержащие подозрительную РНК, были избирательно уничтожены, тогда как соседние контрольные клетки оставались неповреждёнными. 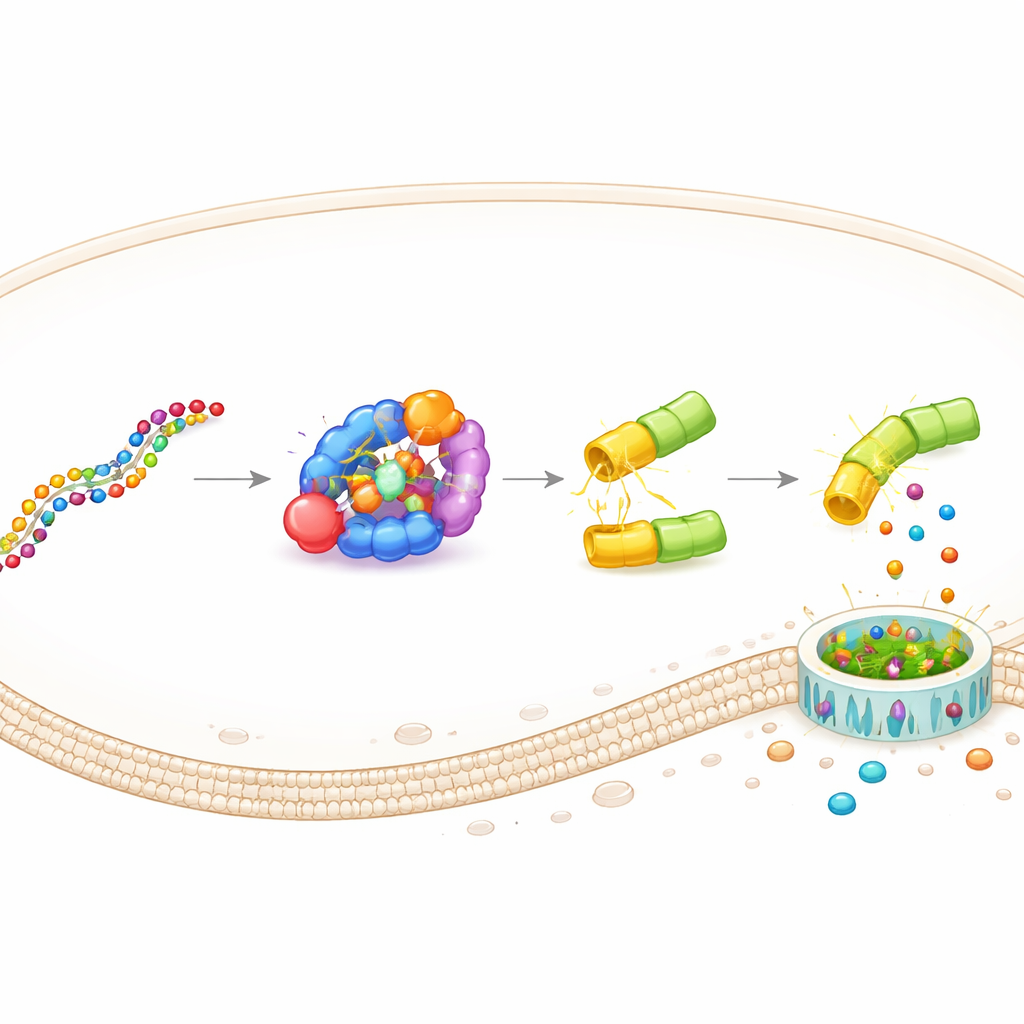
Прицеливание на стареющие клетки
Исследователи также проверили, может ли DAMAGE выслеживать сенесцентные клетки — старые или подвергшиеся стрессу клетки, которые прекращают деление, но накапливаются в тканях и способствуют хрупкости и хроническим заболеваниям. Такие клетки часто повышают синтез двух контрольных белков, p16 и p21. Программируя направляющие против РНК p16 и p21, команда создала версию, названную DAMAGE‑Aging. Эта схема убивала клетки с высоким уровнем этих сообщений, при этом щадя клетки, в которых p16 был генетически удалён, подтверждая, что система считывает текущее содержание РНК, а не фиксированные изменения в ДНК. Лекарственные обработки, повышавшие уровни p16 или p21, делали клетки более уязвимыми к этому целевому самоуничтожению.
Упаковка системы для будущих терапий
Чтобы приблизиться к практическому применению, авторы сжали многочисленные ДНК‑фрагменты DAMAGE в упрощённую конструкцию DAMAGE‑Plus и показали, что она по‑прежнему надёжно функционирует. Затем они транскрибировали эту конструкцию в синтетическую мРНК, упаковали её в липидные наночастицы, похожие на используемые в вакцинах против COVID‑19, и доставили в клетки в культуре. Вариант на мРНК успешно собрал схему и вызвал целевую воспалительную гибель в клетках, несущих вирусные или связанные с раком РНК. Хотя система всё ещё громоздка и протестирована только на клеточных линиях, эти результаты дают надежду, что программируемое, направляемое на РНК уничтожение клеток однажды может быть реализовано через инъекционные мРНК‑формулы.
Новый способ читать и реагировать на клеточные сообщения
Проще говоря, DAMAGE — это молекулярный вышибала, который проверяет внутреннюю РНК‑«ID» каждой клетки и выкидывает только те, что выглядят опасными — инфицированные вирусом, несущие мутации или сенесцентные — заставляя их перейти в взрывную форму самоуничтожения. Работа демонстрирует, что бактериальные РНК‑сенсоры можно с высокой точностью соединять с человеческой машинерией гибели клеток, даже различая однобуквенные различия в генетических посланиях. Хотя до безопасного применения у животных или людей предстоит ещё много инженерной работы, это очерчивает мощную новую стратегию: читать текущую РНК‑переписку внутри клеток и переводить её напрямую в решения о жизни и смерти.
Цитирование: He, M., Wang, W., Zhou, H. et al. A synthetic system for RNA-responsive pyroptosis based on type III-E CRISPR nuclease-protease. Nat Commun 17, 2565 (2026). https://doi.org/10.1038/s41467-026-69179-5
Ключевые слова: пироптоз, CRISPR, терапия, нацеленная на РНК, иммунотерапия рака, клеточное старение