Clear Sky Science · ru
hnRNPM взаимодействует с BCAS2 для регулирования альтернативного сплайсинга в ходе развития ооцитов
Почему важно качество яйцеклетки
Каждая человеческая жизнь начинается с одной яйцеклетки, однако ученые до сих пор выясняют, как эти необычно крупные клетки готовятся к моменту оплодотворения. Задолго до появления сперматозоидов растущие яйцеклетки накапливают тысячи молекул РНК, которые направляют их созревание и первые дни развития эмбриона. В этом исследовании показано, как малоизвестный белок в сотрудничестве с партнером тщательно правит эти сообщения в яйцах мышей — и что происходит, когда эта система редактирования выходит из строя.
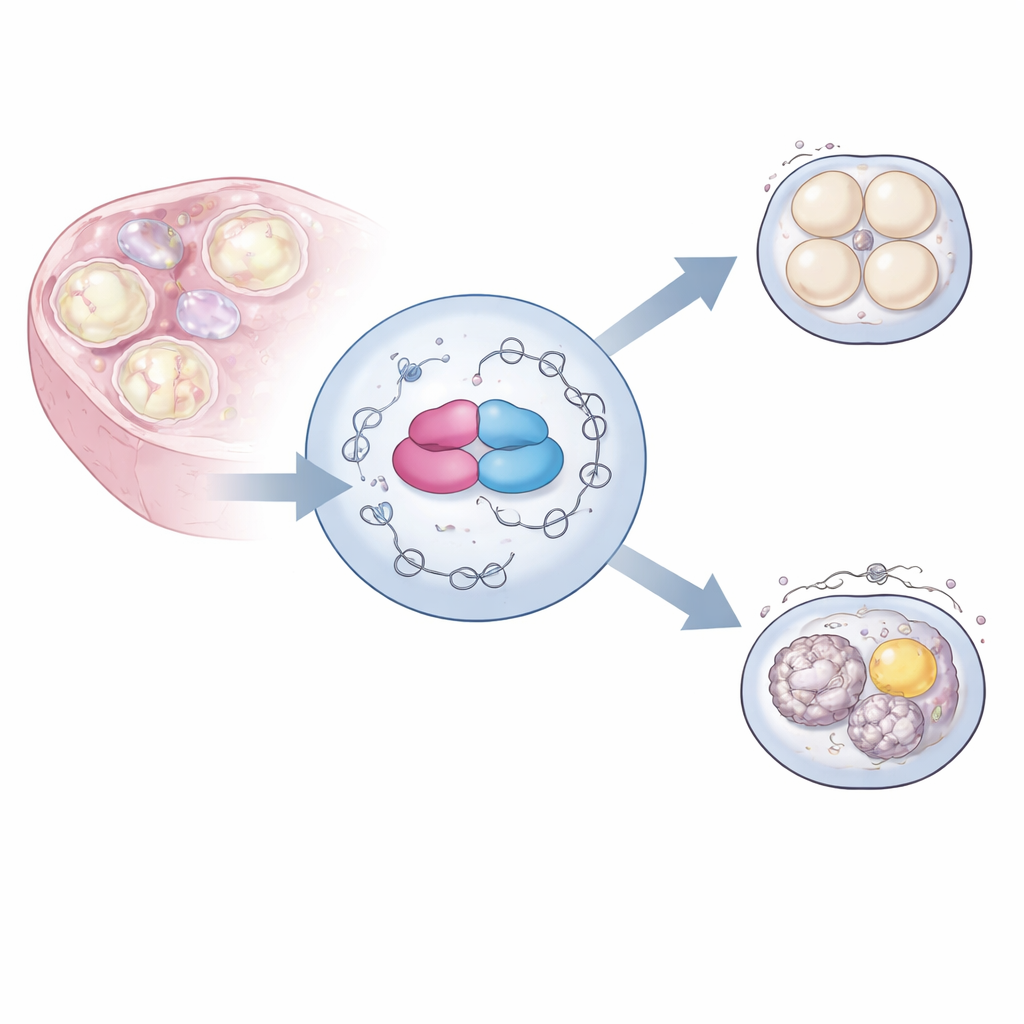
Стражи генетических сообщений
Яйцеклетки растут в яичнике в течение недель, в то время как их ДНК в основном сохраняет молчание. За это время они накапливают обширную библиотеку материнских РНК, скопированных из генома ранее. Эти сообщения необходимо подрезать и «сшивать» по-разному — процесс, называемый альтернативным сплайсингом — чтобы обеспечить нужное сочетание вариантов белков на нужных стадиях. Авторы сосредоточились на белке hnRNPM, который принадлежит к большому семейству РНК-связывающих белков, и на его партнере BCAS2, оба из которых в изобилии присутствуют в женской репродуктивной системе. Ранее наблюдалось, что эти белки связываются со множеством РНК в яйцеклетках, но их точная роль в формировании фертильности оставалась неясной.
Что идет не так без этого «редактора»
Чтобы исследовать функцию hnRNPM, команда применила генную инженерию и удаляла ген Hnrnpm специально в предшественниках яйцеклеток мышей. Яичники у этих самок выглядели нормально и производили сходное число яйцеклеток по сравнению с контрольной группой. Тем не менее при оплодотворении в лаборатории эти яйца почти никогда не развивались дальше первых делений, что делало самок полностью стерильными. При более тщательном обследовании незрелых яйцеклеток были обнаружены тёмные комки в обычно прозрачной цитоплазме. Электронная микроскопия показала, что тонкая внутренняя опора — цитоплазматическая решетка — в значительной степени отсутствовала, а ключевые органеллы, такие как митохондрии и жировые капли, были аномально скупчены, вместо того чтобы быть равномерно распределёнными. Эти изменения указывали на серьёзные нарушения внутренней организации яйцеклетки.
Нарушенный аппарат деления клетки
Те же мутантные яйцеклетки испытывали трудности с завершением мейоза, особой формы деления клетки, при котором уменьшается число хромосом вдвое. Когда исследователи созревали яйца в культуре, они могли инициировать мейоз, но обычно процесс останавливался до его завершения. В микроскопе структуры, отвечающие за разъединение хромосом — веретена деления — были искривлёнными, многополярными или слабо закреплёнными. Белок перицентрин, помогающий организовывать полюса веретена, появлялся поздно и в неправильных местах. В совокупности эти дефекты означали, что яйца не могли надёжно выстраивать и разделять хромосомы, что, вероятно, и приводило к полной неспособности развиваться после оплодотворения.
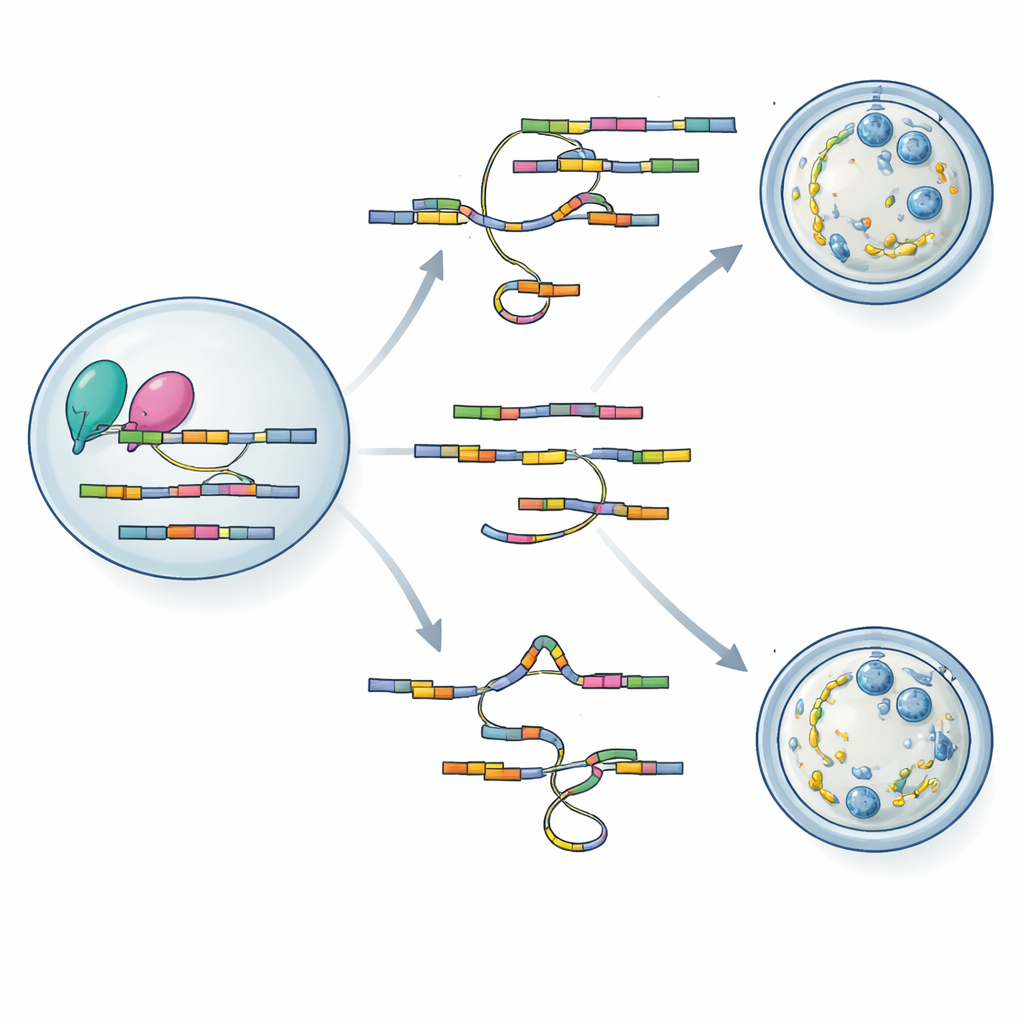
Чтение и переписывание инструкций РНК
Чтобы понять, как потеря hnRNPM приводит к столь широким нарушениям, команда обратилась к двум мощным методам секвенирования, адаптированным для крошечных образцов яйцеклеток. С помощью SCAN-seq, который считывает полноразмерные молекулы РНК из одиночных ооцитов, они обнаружили более тысячи изменений сплайсинга в мутантных яйцеклетках, включая многие ранее неизвестные варианты РНК. Особенно пострадали гены, участвующие в построении цитоплазматической решетки, контроле поведения веретёна и регуляции мейотического клеточного цикла. Второй метод, LACE-seq, показал точные места связывания hnRNPM на РНК, выявив предпочтение к GU-обогащённым участкам внутри экзонов. Наложив два набора данных, авторы продемонстрировали, что hnRNPM непосредственно связывается со многими сообщениями, сплайсинг которых изменяется при отсутствии белка, связывая его связывательную активность с точностью сплайсинга.
Модель командной работы в контроле яйцеклетки
Исследования белковых взаимодействий показали, что hnRNPM физически ассоциирует с BCAS2 и с основными компонентами сплайсингового аппарата. Оба партнёра связываются со многими одними и теми же мишенями РНК и часто изменяют их схожим образом при нарушении работы любого из белков. Любопытно, что потеря hnRNPM уменьшала уровни белка BCAS2 и ослабляла его связывание с общими РНК-мишенями, что наводит на мысль, что hnRNPM не только редактирует сообщения, но и помогает стабилизировать партнёра на этих сообщениях. Авторы предлагают модель, в которой hnRNPM и BCAS2 формируют кооперативный комплекс, приспосабливающий ключевые материнские РНК в период роста ооцита, обеспечивая правильную сборку цитоплазматической решётки и надёжный мейотический дележ.
Что это означает для фертильности
Проще говоря, эта работа показывает, что молекулярная «редакторская» команда — hnRNPM и BCAS2 — действует за кулисами, подготавливая яйцеклетки к жизни после оплодотворения. Когда эта команда отсутствует, внутренняя опора яйцеклетки рушится, механизм сортировки хромосом даёт сбои, и хотя яйцеклетки вырабатываются в нормальном количестве, они не способны поддержать развитие эмбриона. Поскольку hnRNPM сильно сходен у мышей и людей, эти результаты указывают на консервативную систему контроля качества, которая может лежать в основе некоторых форм неясного женского бесплодия и открывать новые пути для диагностики или лечения.
Цитирование: Zhou, S., Liu, D., Gan, S. et al. hnRNPM cooperates with BCAS2 to modulate alternative splicing during oocyte development. Nat Commun 17, 2681 (2026). https://doi.org/10.1038/s41467-026-69176-8
Ключевые слова: развитие ооцита, альтернативный сплайсинг, женское бесплодие, белки, связывающие РНК, цитоплазматическая решетка