Clear Sky Science · ru
Ансамбли с атомным разрешением для внезкономентированных белков с помощью AlphaFold
Почему формоизменяющиеся белки важны
В наших клетках полно белков, которые никогда не закрепляются в одной жесткой форме. Эти «внутренне неупорядоченные» белки больше похожи на гибкие вермишели, чем на аккуратно свернутые машины, однако они играют ключевую роль в процессах от клеточной сигнализации до нейродегенеративных заболеваний. Поскольку они постоянно двигаются и изгибаются, зафиксировать весь их спектр форм с атомной точностью крайне сложно и обычно требует долгих экспериментов и затратных вычислений. В этой статье представлен новый способ сочетать искусственный интеллект и физику, чтобы гораздо эффективнее картировать эти непоседливые молекулы.
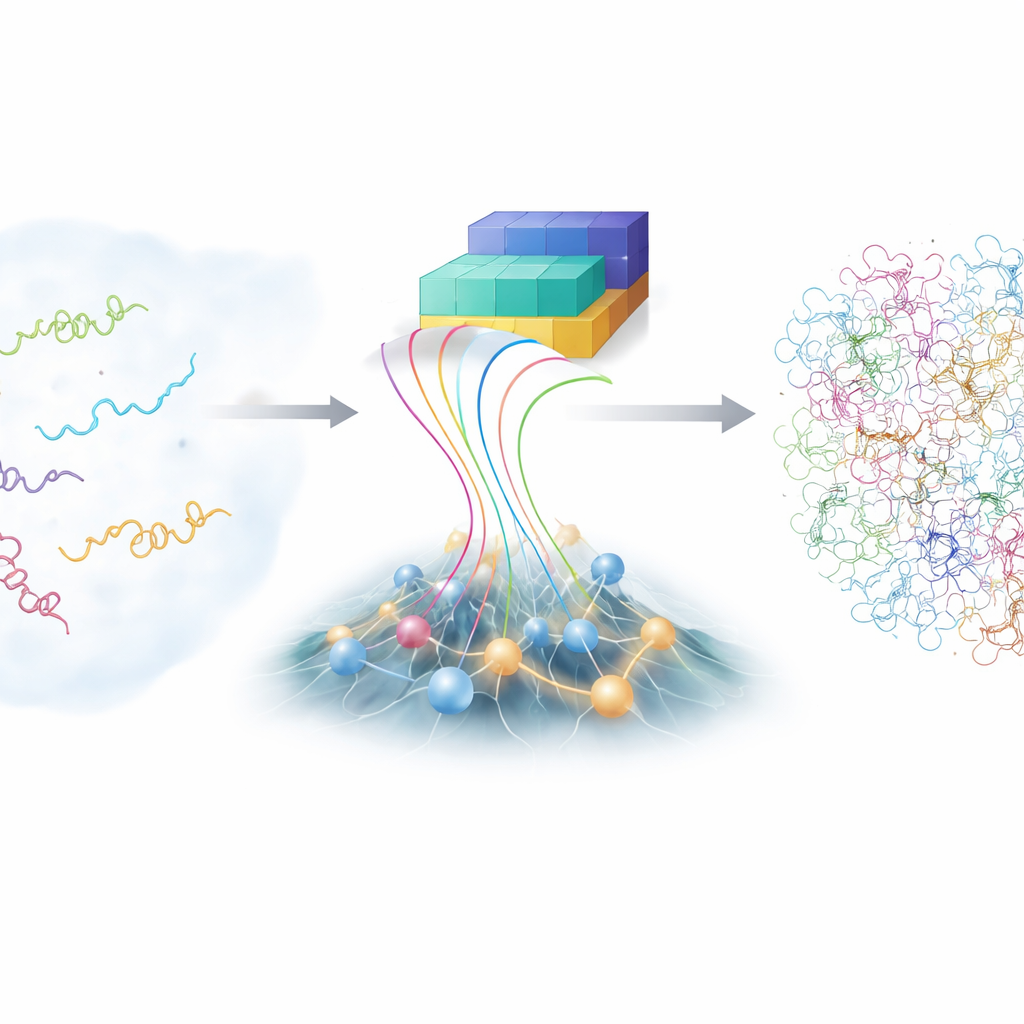
Проблема непоседливых молекул
В отличие от учебных моделей белков, которые показывают одну аккуратную структуру, внутренне неупорядоченные белки (IDP) блуждают по обширному ландшафту возможных форм. Такая гибкость помогает им распознавать разных партнёров, но одновременно делает их крайне трудными для изучения. Традиционные лабораторные методы, такие как продвинутая ядерная магнитно‑резонансная спектроскопия и рентгеновское рассеяние, дают сведения об усреднённых по множеству форм величинах, но не о каждой отдельной конформации. Компьютерные симуляции с полным атомным представлением, в принципе, могут отслеживать каждый атом при извивающемся IDP, но они чрезвычайно дорогие и зависят от тонко настроенных физических моделей. В результате научное сообщество располагает лишь ограниченной коллекцией точных подробных ансамблей IDP для анализа.
Сочетание разумных предположений с физическими законами
В последние годы семейство глубоких сетей AlphaFold поразило биологов способностью предсказывать структуры белков по последовательностям аминокислот. Для неупорядоченных белков привычная сильная сторона AlphaFold — выбор одной «лучшей» формы — менее полезна, потому что у IDP нет единственной структуры. Зато AlphaFold даёт богатую информацию о том, какие участки цепи с большей вероятностью оказываются ближе или дальше друг от друга. Авторы построили новую систему, названную bAIes, которая рассматривает эту информацию, полученную ИИ, как мягкое руководство и смешивает её с быстрым физическим моделем, намеренно стартующим от представления «случайной спирали», где цепь исследует все возможные изгибы и кручения без предпочтения какой‑то конкретной формы.
От случайных спутанностей к реалистичным ансамблям
Сначала исследователи сконструировали эффективную физическую модель, воспроизводящую поведение полностью неструктурированной белковой цепи, опираясь на статистику, извлечённую из тысяч известных белковых структур. Эта модель служит «априорой» — базовым ожиданием того, как ведёт себя IDP, если о нём ничего больше не известно. Затем bAIes считывает предсказания AlphaFold о том, пары каких остатков склонны сближаться. Вместо того чтобы принуждать белок к единой конфигурации, система преобразует эти подсказки в мягкие пространственные ограничения с учётом неопределённости, позволяя цепи удовлетворять предложениям ИИ лишь тогда, когда они согласуются с общей физической картиной.
Тестирование на реальных экспериментах
Чтобы проверить работоспособность подхода, команда применила bAIes к набору из 21 белка — от почти полностью случайных спиралей до более сложных систем с временными спиральными фрагментами и несколькими доменами. Для каждого белка полученные компьютерные ансамбли сравнивали с широким набором экспериментальных измерений, которые исследуют как локальные детали, так и глобальные размер и форму. Для очень гибких белков, таких как пептид Aβ40, связанный с болезнью Альцгеймера, простая модель случайной спирали уже была близка к реальности, и bAIes сохранил это хорошее соответствие. Для частично структурированных белков bAIes улучшал согласие с экспериментами, правильно отражая появление и исчезновение коротких спиральных сегментов и компактных участков. Важно, что метод оставался устойчивым даже когда AlphaFold был чрезмерно уверенным и ошибочно предсказывал стабильные фолды там, где эксперименты в растворе показывали беспорядок, потому что bAIes явно допускает ошибки во входных данных от ИИ.
Превосходство или сопоставимость с существующими методами
Авторы затем сравнили bAIes с тяжёлыми всемолекулярными симуляциями на специализированных суперкомпьютерах, продвинутыми грубо‑гранулярными моделями, упрощающими белки до бусин, и новыми генераторами глубокого обучения, обученными на данных симуляций. По множеству тестов bAIes последовательно соответствовал или превосходил эти подходы в воспроизведении экспериментальных данных, при этом требуя гораздо меньше вычислительных ресурсов по сравнению с полноформатными симуляциями. Он также работал не только для простых IDP, но и для белков с несколькими жёсткими доменами, связанными гибкими звеньями, восстанавливая их общие формы в растворе. Когда исследователи дополнительно подгоняли ансамбли bAIes с использованием экспериментальных данных, согласие улучшалось ещё больше, показывая, что метод может служить мощной отправной точкой для интегративного моделирования.
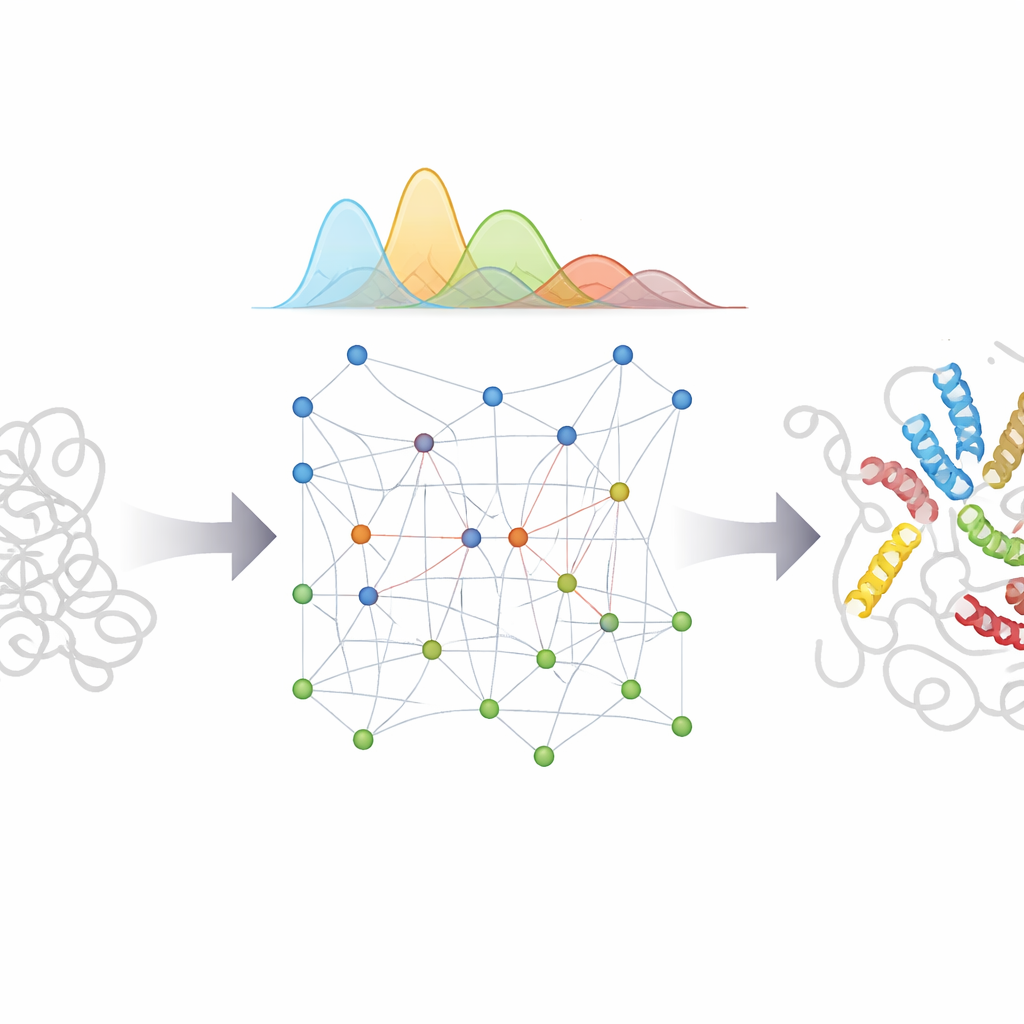
Что это значит для биологии и медицины
Объединив силу распознавания закономерностей AlphaFold с продуманной физической моделью и байесовской обработкой неопределённости, bAIes предлагает практический путь к детализированным «фильмам» о неупорядоченных белках вместо одиночных снимков. Эти ансамбли с атомной детализацией помогут учёным понять, как гибкие участки распознают партнёров, как начинаются неправильная свёртка и агрегация при таких заболеваниях, как болезнь Паркинсона и Альцгеймера, и как малые молекулы могут связываться с неуловимыми, меняющимися мишенями. Поскольку метод эффективен и реализован в программном обеспечении с открытым исходным кодом, его можно широко применять для генерации реалистичных ансамблей множества неупорядоченных белков, направляя эксперименты и поддерживая будущие системы ИИ, которые будут стремиться предсказывать не одну структуру, а полный спектр форм, доступных наиболее гибким молекулам жизни.
Цитирование: Schnapka, V., Morozova, T.I., Sen, S. et al. Atomic resolution ensembles of intrinsically disordered proteins with Alphafold. Nat Commun 17, 2399 (2026). https://doi.org/10.1038/s41467-026-69172-y
Ключевые слова: внутренне неупорядоченные белки, AlphaFold, байесовское моделирование, ансамбли белков, структурная биология