Clear Sky Science · ru
Молекулярный механизм ввода фосфата бактериальным транспортером PstSCAB
Почему мелкие питательные вещества важны для нас
Каждая живая клетка, от человеческих нейронов до почвенных бактерий, «питается» фосфором. Этот элемент участвует в запасании энергии, построении ДНК и поддержании целостности клеточных мембран. Однако в природе доступный фосфат — форма фосфора, которую клетки действительно могут импортировать — часто встречается в дефиците. Многие патогенные бактерии полагаются на сверхэффективный молекулярный механизм, называемый транспортером PstSCAB, чтобы выуживать фосфат при его нехватке. Понимание точного принципа работы этого аппарата важно не только для фундаментальной науки; оно может открыть пути к новым способам обезвреживания инфекций за счёт «голодания» бактерий по этому жизненно важному элементу.
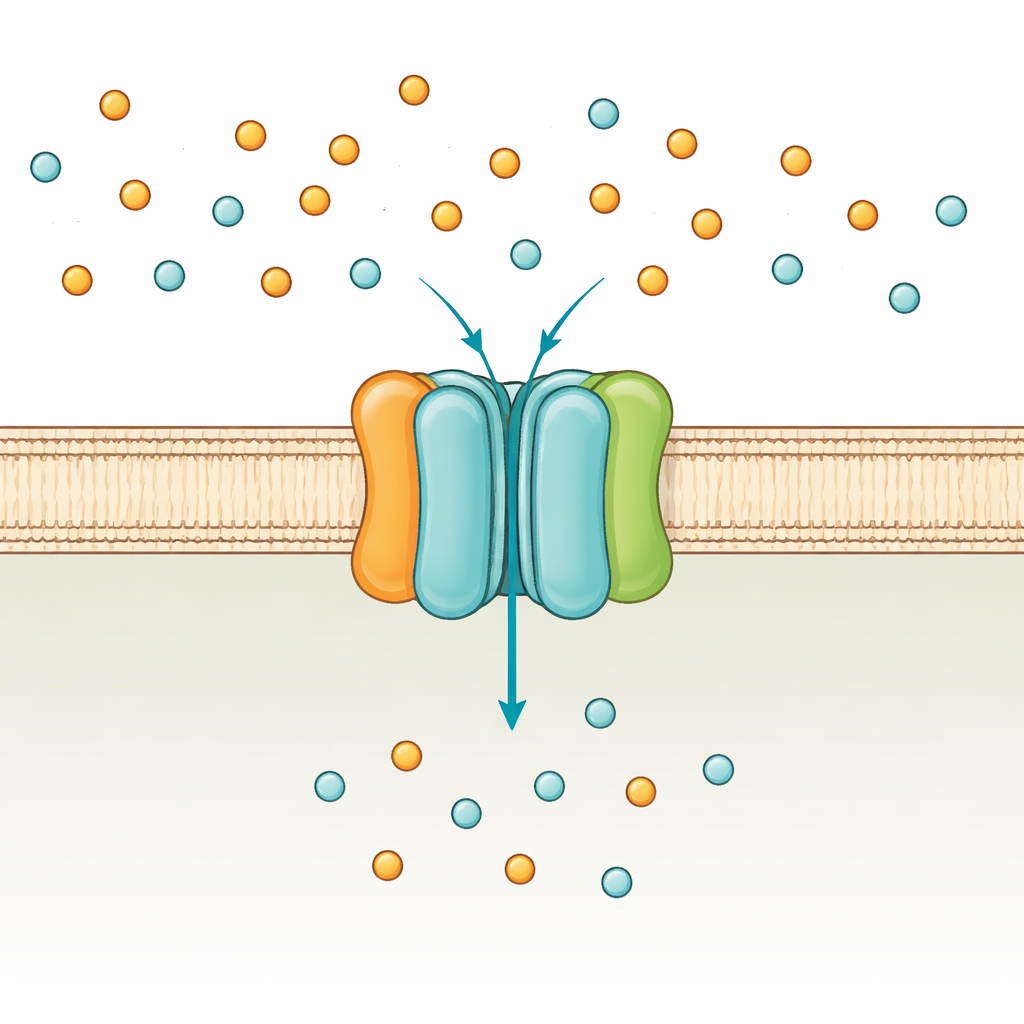
Фосфатный привратник клетки
Бактерии, такие как Escherichia coli, используют два основных пути для захвата фосфата: низкоаффинную систему, работающую при высокой концентрации фосфата, и высокоаффинный комплекс PstSCAB, включающийся при дефиците. PstSCAB находится в клеточной мембране и приводится в действие ATP — универсальной валютой энергии в клетке. Он собран из пяти частей: двух интегральных субъединиц (PstA и PstC), образующих проход, растворимой «ловящей» белковой субъединицы снаружи мембраны (PstS), и пары внутренних субъединиц (PstB), которые расходуют ATP для транспорта. Поскольку эта система также участвует в регуляции множества генов, связанных с вирулентностью бактерий, мутации в PstSCAB могут ослаблять патогены, вызывающие инфекции мочевых путей, сепсис у сельскохозяйственных животных и туберкулёз.
Запечатление механизма в действии
До настоящего времени учёные имели лишь фрагментарные представления о PstSCAB, в основном о «ловце» PstS в отдельности. В этой работе исследователи использовали высокоразрешающую криоэлектронную микроскопию, чтобы визуализировать весь транспортер на ключевых этапах его рабочего цикла. Они реконситуировали бактериальные белки в искусственных мембранных «нанодисках» и замораживали их настолько быстро, что молекулы оказывались застигнутыми в середине движения. Тонко варьируя белки и добавляя или исключая ATP, они получили структуры трёх основных состояний: спокойную внутренне-ориентированную форму без присоединённого «ловца», предтранслокационное состояние, где PstS, несущий фосфат, пристыковывается к мембранному комплексу, и ATP-связанный каталитический интермедиат, в котором фосфат удерживается внутри транспортёра.
Как изменение формы перемещает фосфат
Изображения показывают, как скоординированные конформационные изменения переносят фосфат снаружи внутрь клетки. В состоянии покоя проход, образованный PstA и PstC, открыт только в сторону внутренней части клетки; внешняя сторона закрыта набором «шлюзовых» остатков, поэтому фосфат ещё не может войти снаружи. Когда к предтранслокационному состоянию пристыковывается фосфатно-нагруженный PstS, он встраивается между гибкими петлями PstA и PstC, но, что примечательно, мембранные субъединицы почти не меняют форму. Настоящая перестановка происходит, когда PstS начинает раскрываться — его две доли расходятся, освобождая фосфат, — и одновременно две субъединицы PstB сближаются, связывая ATP. Это связывание ATP формирует димер PstB и натягивает соединительные спирали в PstA и PstC, переворачивая весь канал в наружно-ориентированную конформацию и выставляя наружу специфический карман для связывания фосфата.
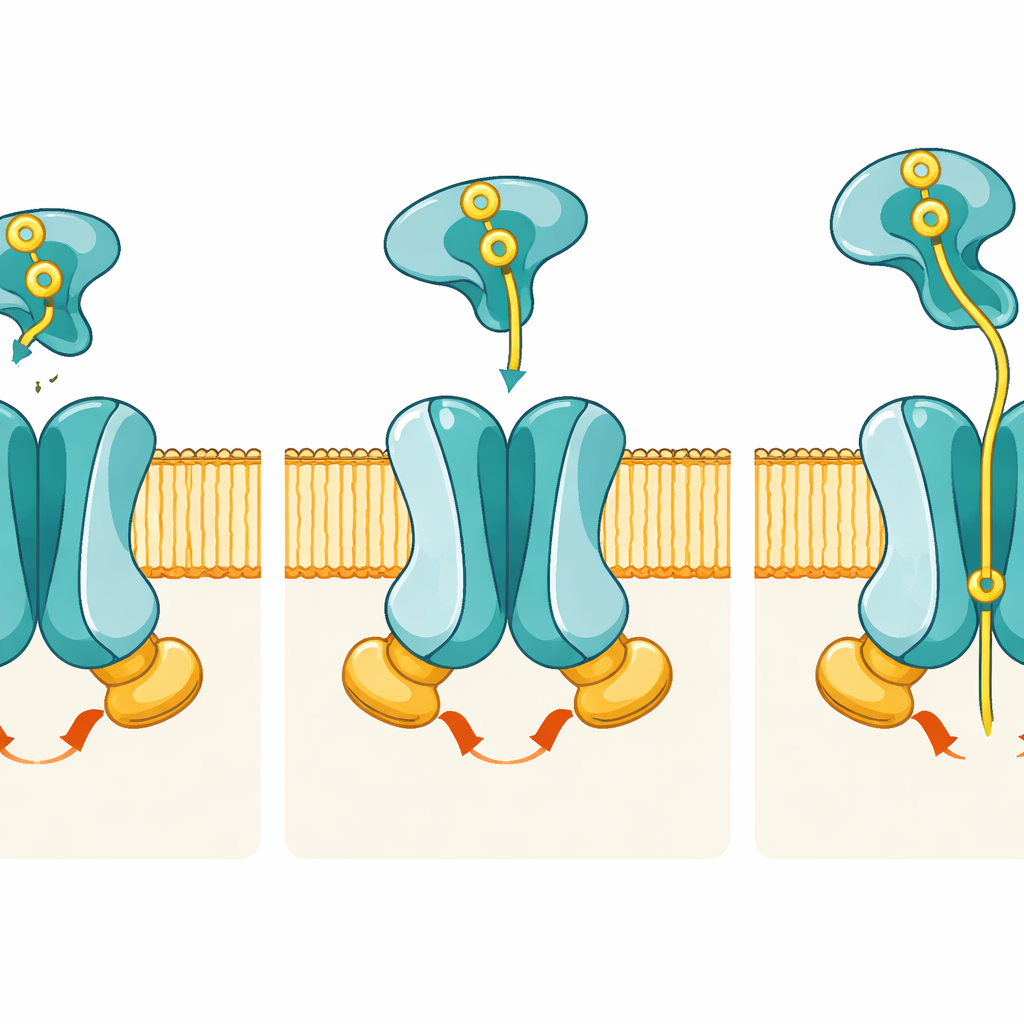
Специальный карман для фосфата
В наружно-ориентированной ATP-связанной структуре авторы обнаруживают плотность в средней части мембранного региона, соответствующую иону фосфата. Этот ион удерживается положительно заряженными аминокислотами — особенно двумя аргининами, по одному от PstA и PstC — которые действуют как молекулярные «кончики пальцев», захватывающие отрицательно заряженный фосфат. Компьютерные моделирования показывают, что фосфат остаётся стабильно связанным в этом кармане на микросекундных временных масштабах, а генетические эксперименты подтверждают его значимость: при замене этих ключевых остатков транспортер продолжает гидролизовать ATP, но практически не импортирует фосфат. Такое разделение «где тратится энергия» и «где распознаётся груз» подчёркивает, насколько тонко настроен этот механизм под фосфат.
От структурных снимков к медицинским перспективам
В совокупности полученные структуры и сопутствующие биохимические тесты очерчивают полный цикл: PstS захватывает фосфат снаружи, пристыковывается к внутренне-ориентированной форме транспортёра, затем — в паре со связыванием и гидролизом ATP субъединицами PstB — вызывает переворот, который перемещает фосфат в мембранный карман и далее во внутреннюю часть клетки. После гидролиза ATP машина возвращается в состояние покоя, готовая к следующему циклу. Для непрофессионала ключевая идея такова: теперь у нас есть атомно-точная схема того, как многие бактерии выживают в условиях низкого содержания фосфата и как они регулируют свою вирулентность. Эта подробная карта может направлять разработку лекарств, антител или пептидов, которые блокируют транспортер или его «ловца», потенциально превращая жизненно важные ворота для питательного вещества в уязвимую терапевтическую мишень.
Цитирование: Xiao, H., Li, S., Qi, R. et al. Molecular mechanism of phosphate import by the bacterial PstSCAB transporter. Nat Commun 17, 2294 (2026). https://doi.org/10.1038/s41467-026-69153-1
Ключевые слова: транспорт фосфата, поглощение питательных веществ бактериями, ABC-транспортер, PstSCAB, антибактериальные мишени