Clear Sky Science · ru
Молекулярные сведения о транспортере капсульного полисахарида комплекса Wza-Wzc
Как бактерии носят невидимую броню
Бактерии, вызывающие болезни, часто укрываются сахаристым покровом, или капсулой, которая помогает им ускользать от нашей иммунной системы и выдерживать неблагоприятные условия. В этом исследовании в атомных деталях показано, как ключевой машинный комплекс в распространённых кишечных бактериях собирает и экспортирует эту сахаристую броню. Понимание этого процесса может указать путь к новым антибиотикам и вакцинам, которые лишают патогены защитного щита, а не просто пытаются убить их.
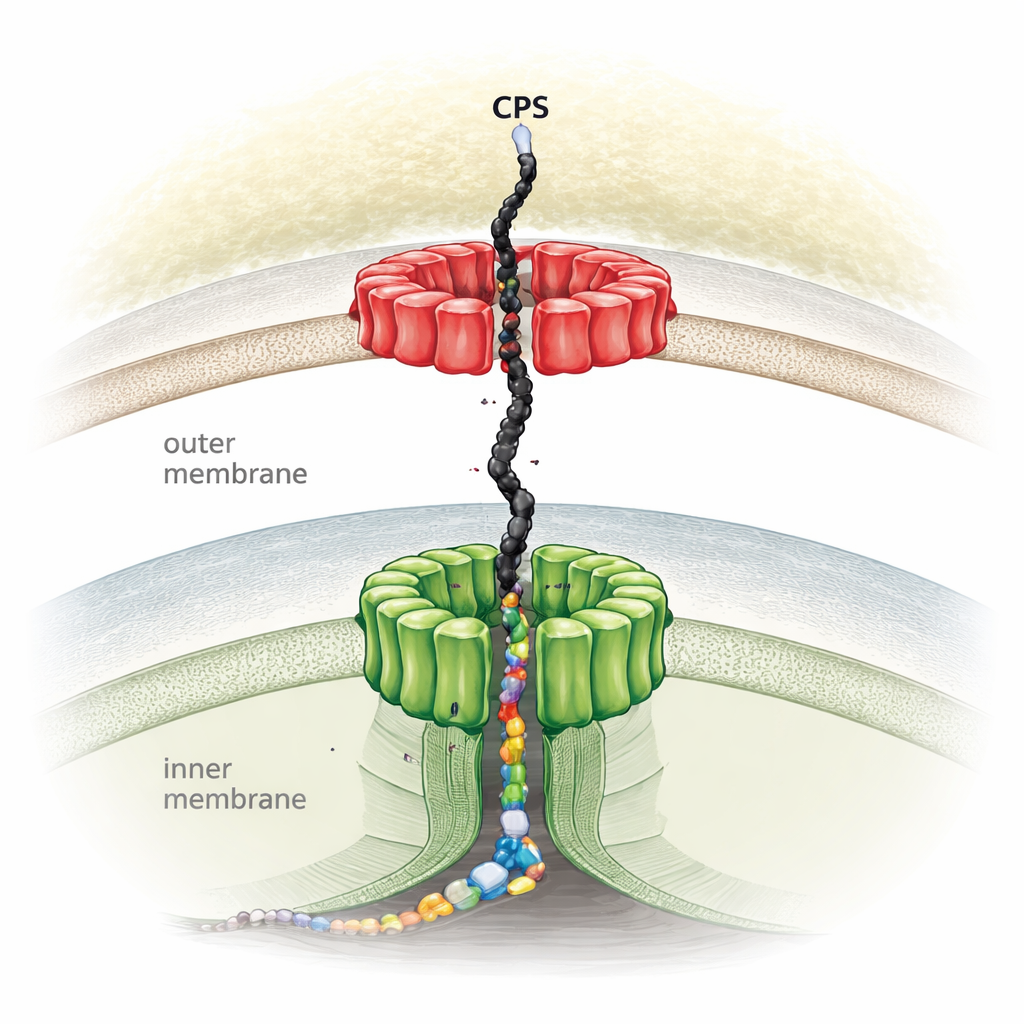
Сахарный щит вокруг опасных микробов
Многие патогенные бактерии окружают себя капсульными полисахаридами — длинными, разветвлёнными цепями сахаров, формирующими толстый внешний слой. Эта капсула помогает им уклоняться от иммунной атаки, противостоять антибиотикам и формировать устойчивые биоплёнки. Работа сосредоточена на Escherichia coli, хорошо изученном модельном организме, который использует широко распространённый путь, называемый Wzx/Wzy-зависимым, для сборки этих сахарных цепей. В этом пути небольшие повторяющиеся сахарные блоки сначала собираются внутри клетки, переворачиваются через внутреннюю мембрану, связываются в длинные полимеры и в конце концов выводятся наружу, формируя капсулу. Хотя исследователи знали названия основных белковых участников, им не хватало целостной картины того, как они собираются в единую машину, пересекающую всю бактериальную оболочку.
Открытие полноценного молекулярного туннеля
С помощью высокоразрешающей криоэлектронной микроскопии авторы решили полную трёхмерную структуру комплекса Wza-Wzc — основного механизма экспорта капсульных сахаров у E. coli K12. Они обнаружили, что восемь копий каждого белка собираются в высокий, непрерывный канал, проходящий от внутренней мембраны к наружной, мостя водную полость между ними. Wza располагается в наружной мембране в виде жёсткого кольцеобразного выходного порта, тогда как Wzc формирует гибкую башню, закреплённую во внутренней мембране. Вместе они создают туннель длиной примерно 250–360 ангстрем, достаточно широкий, чтобы направлять большой гибкий сахарный полимер от места его синтеза у внутренней мембраны до поверхности клетки, не позволяя ему диффундировать или протекать. Мутации в ключевых точках контакта между Wza и Wzc полностью останавливают образование капсулы, подтверждая, что этот совместный комплекс необходим для экспорта.
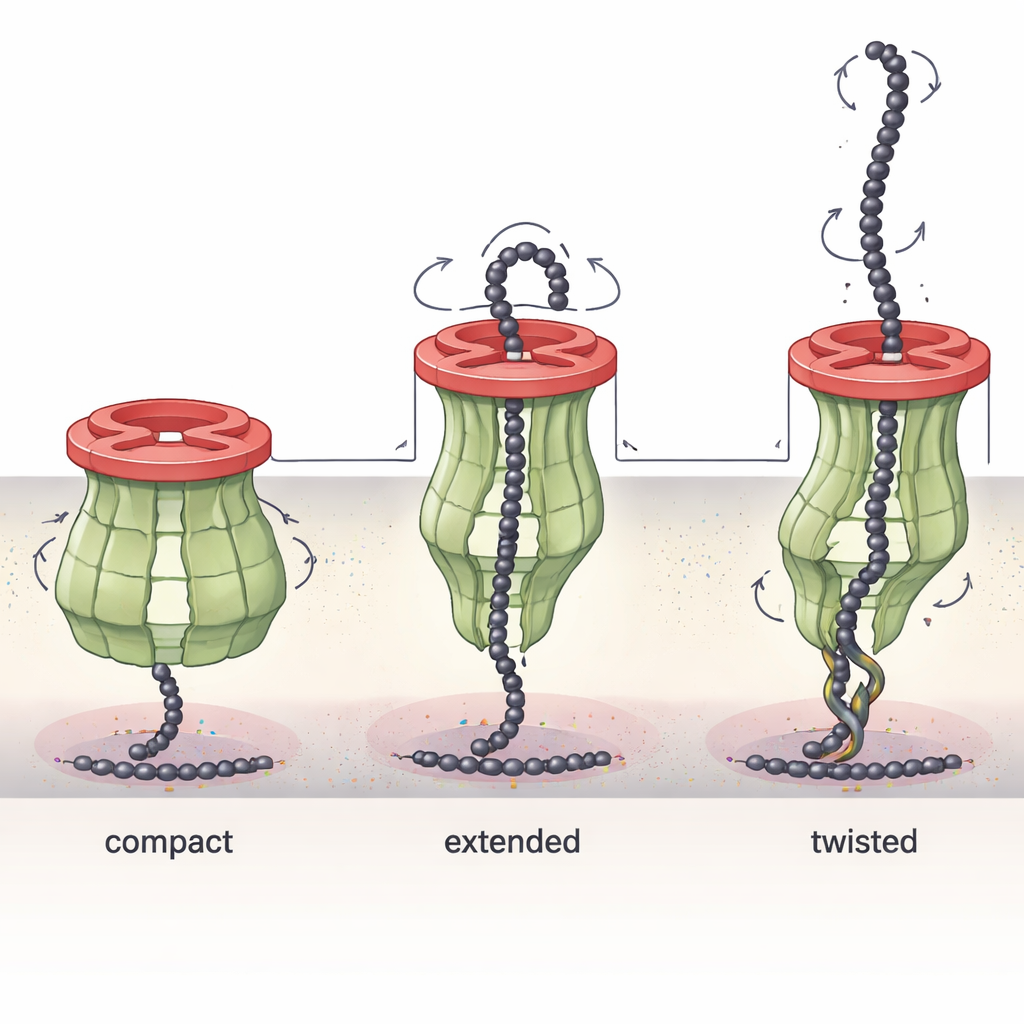
Машина‑трансформер, которая вытягивает сахара
Часть комплекса Wzc оказалась удивительно подвижной. Захватив несколько структурных «моментов» в разных химических состояниях, исследователи показали, что длинные периплазматические «руки» Wzc могут сгибаться, вращаться и вытягиваться подобно механическим рычагам. В одном состоянии канал компактен и плотно закрыт; в других Wzc поворачивается и растягивается, деликатно изменяя ширину и форму туннеля. В определённых конформациях «руки» частично блокируют канал или ослабляют контакт с Wza, а в крайних случаях одно кольцо Wzc может одновременно взаимодействовать с двумя кольцами Wza. Эти наблюдения поддерживают модель, в которой Wzc действует подобно молекулярной лебёдке: его крутящие и удлиняющие движения помогают вытягивать растущую сахарную цепь от внутренней мембраны и подавать её в пору наружной мембраны, одновременно координируя сборку и разборку всей машины.
Площадка посадки, распознающая сахар
Другой загадкой было то, как механизм распознаёт правильные сахарные строительные блоки среди множества углеводов в и вокруг клетки. Wzc содержит «джеллиролл»-домен, расположенный непосредственно над внутренней мембраной, роль которого была неясна. Сравнение структуры с известными белками, связывающими сахара, в сочетании с биохимическими тестами на панелях очищенных углеводов показали, что этот домен может распознавать специфические сахарные мотивы, похожие на те, что встречаются в капсуле E. coli. Удаление джеллиролл-региона резко снижало, но не полностью устраняло, образование капсулы, что указывает на его роль посадочной площадки, захватывающей недавно перевёрнутые сахарные единицы и направляющей их в платформу полимеризации, сформированную Wzc вместе с ферментом Wzy, который сшивает эти единицы в длинную цепь.
Координация роста, экспорта и сброса
Наконец, исследование связывает эти структурные особенности с биохимической системой контроля, основанной на фосфорилировании — обратимом присоединении фосфатных групп к богатому тирозином хвосту Wzc. Когда Wzc сильно фосфорилирован, он в основном существует в виде рыхлых отдельных единиц. По мере удаления фосфатов партнерским ферментом киназные домены Wzc собираются в октамер, перестраивая его «руки» так, чтобы они могли взаимодействовать с Wza и окружать полимеразу Wzy. По мере роста капсульной цепи и её протяжки через туннель дальнейшее скручивание и растяжение Wzc, вероятно, помогает высвободить готовый полимер в Wza для экспорта. После завершения секреции Wzc повторно фосфорилирует себя, что приводит к распаду комплекса и сбрасыванию системы для следующего цикла синтеза капсулы.
Почему это важно в борьбе с инфекциями
Проще говоря, эта работа показывает почти винтик за винтиком, как бактерии строят молекулярный трубопровод, протягивающий длинные сахарные цепи изнутри клетки наружу, где они формируют защитный плащ. Карта структуры и движений комплекса Wza-Wzc, а также выявление элементов распознавания сахара и контроля, выделяют несколько уязвимых мест, которые могут стать мишенями будущих препаратов или вакцин. Нарушение этой машины экспорта не обязательно убьёт бактерии напрямую, но может лишить их брони, сделав их гораздо более уязвимыми для нашей иммунной системы и существующих антибиотиков.
Цитирование: Yuan, B., Sieben, C., Raj, P. et al. Molecular insights into the capsular polysaccharide transporter Wza-Wzc complex. Nat Commun 17, 1436 (2026). https://doi.org/10.1038/s41467-026-69136-2
Ключевые слова: бактериальная капсула, секреция полисахаридов, комплекс Wza-Wzc, структура крио-ЭМ, антибактериальные мишени