Clear Sky Science · ru
Консенсусный аллерген, доставляемый с помощью мРНК, индуцирует нейтрализующий ответ IgG против пищевых и пыльцевых аллергенов
Почему многие аллергии можно лечить одновременно
Для людей, которые реагируют не на один продукт или пыльцу, а на множество родственных источников, повседневная жизнь может напоминать прохождение минного поля. Укус персика, горсть орехов или весенний ветер с пыльцой могут вызвать один и тот же опасный ответ. В этом исследовании изучается новый подход к успокоению таких перекрестных аллергий с помощью одного сконструированного белка, доставляемого посредством мРНК — той же базовой технологии, что используется в некоторых вакцинах против COVID-19 — чтобы перенастроить иммунную систему и блокировать целое семейство родственных аллергенов одновременно.
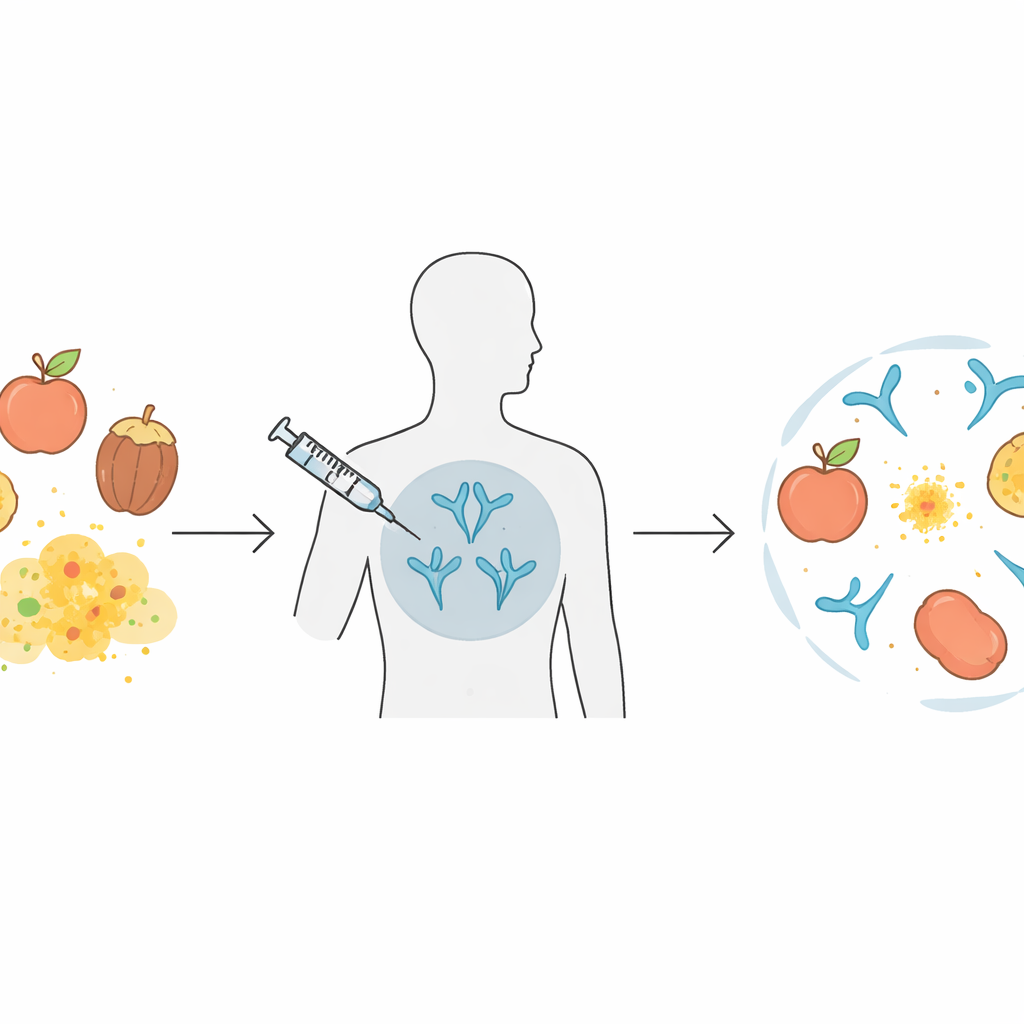
Как одна аллергия превращается во многие
Многие люди с пищевой аллергией реагируют не на что-то одно. Они могут испытывать реакции на несколько фруктов, орехов, овощей и даже на пыльцу, потому что эти источники содержат похожие белки. В этой работе внимание сосредоточено на семействе растительных белков, называемых неспецифическими белками переноса липидов (nsLTPs), которые распространены в продуктах, таких как персики, яблоки, орехи, а также в пыльце некоторых деревьев и сорняков. В странах Средиземноморья так называемый «LTP-синдром» может заставлять пациентов реагировать на широкий список продуктов, иногда с жизнеугрожающим анафилактическим шоком. Существующие иммунотерапии обычно нацелены на экстракты из одного источника и могут не охватывать всех перекрестно реактивных «родственников», что означает длительное лечение и неполную защиту.
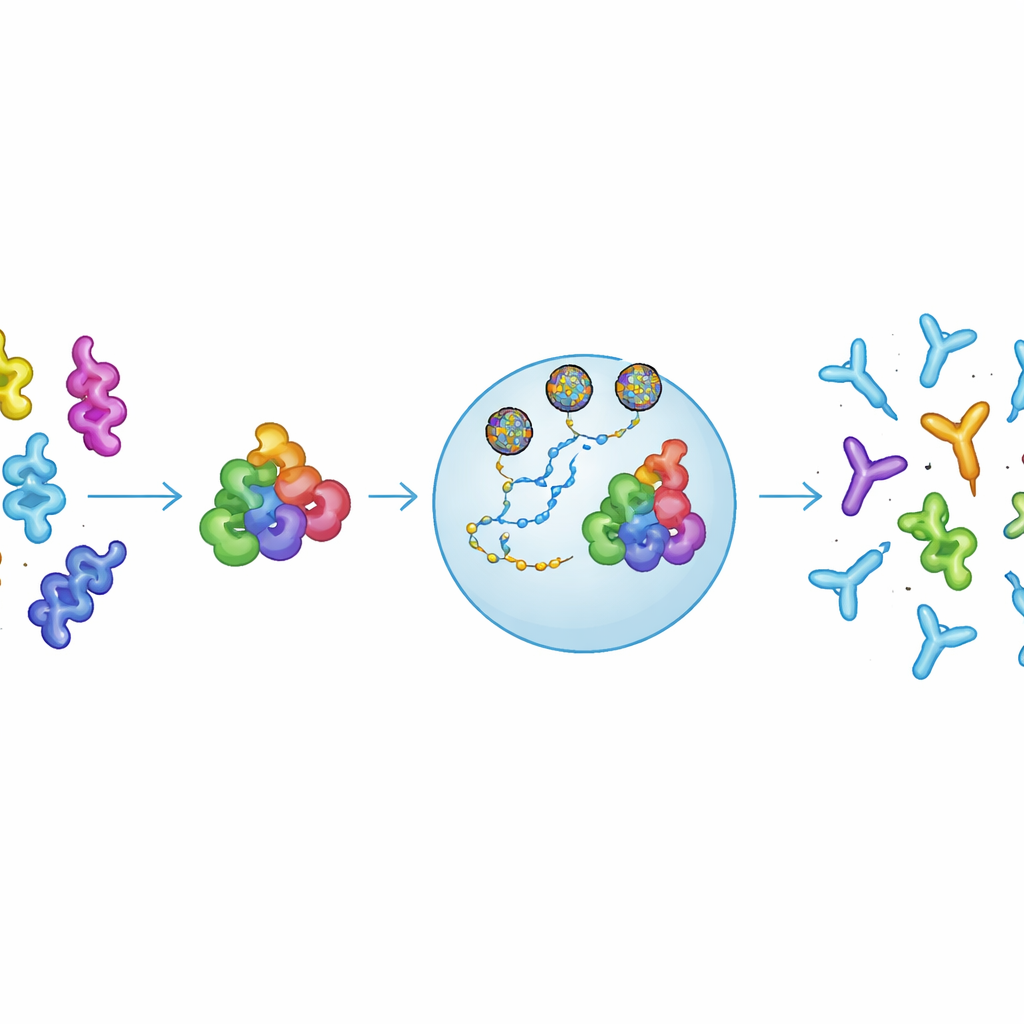
Проектирование «консенсусного» аллергена
Исследователи поставили цель разработать один белок, который имитировал бы сразу множество различных аллергенов nsLTP. Они сравнили аминокислотные последовательности nsLTP, найденных в продуктах и пыльце, и создали консенсусную версию, названную cnsLTP1, которая не копирует ни один природный белок, но улавливает общие структурные черты семейства. Лабораторные тесты показали, что этот сконструированный белок сворачивается как натуральные nsLTP, устойчив к нагреванию и охлаждению и, что важно, распознается IgE-антителами пациентов, уже аллергичных к nsLTP. Это распознавание указывает, что cnsLTP1 демонстрирует те же ключевые «триггерные участки», что и природные аллергены, что необходимо для перенастройки иммунного ответа.
Обучение иммунной системы с помощью мРНК- и белковых вакцин
Дальше команда протестировала cnsLTP1 на мышах, используя два способа доставки: традиционную белковую вакцину с адъювантами и мРНК-вакцину, упакованную в липидные наночастицы, по составу схожую с лицензированными мРНК-вакцинами. У неопытных мышей оба подхода вызвали сильный антительный ответ против cnsLTP1, особенно подклассов IgG, известных у мышей как выполняющие защитную, блокирующую аллергию роль. МРНК-вакцина склонялась к выработке большего количества определённого типа IgG и делала это после меньшего числа доз. Антитела, индуцированные против cnsLTP1, связывались не только с сконструированным белком, но и с широким панелем различных пищевых и пыльцевых nsLTP, часто более широко, чем антитела против одиночных природных аллергенов, таких как персиковый или лептринный nsLTP. Это означает, что консенсусный дизайн успешно научил иммунную систему распознавать множество родственных аллергенов.
Блокирование аллергических реакций в лаборатории и тестирование на аллергичных мышах
Чтобы проверить, могут ли эти антитела реально мешать аллергическим реакциям, исследователи смешали сыворотку мышей с аллергенами, а затем добавили человеческую сыворотку от пациентов с тяжёлыми аллергиями на nsLTP. Они обнаружили, что антитела, вызванные cnsLTP1, могли блокировать связывание IgE с несколькими nsLTP и снижали дегрануляцию гуманизированных базофилоподобных клеток — клеточной модели аллергической активации. В более требовательном испытании команда использовала модель мыши, уже сенсибилизированной к персиковому nsLTP и склонной к анафилаксии. МРНК-вакцина хорошо переносилась и усиливала уровень IgG против нескольких nsLTP, но в условиях конкретного теста она явно не уменьшила анафилактические симптомы, такие как падение температуры тела или маркеры активации тучных клеток. Это говорит о том, что хотя иммунная система и была перестроена, режим лечения ещё не был достаточно сильным или точно настроенным, чтобы полностью предотвратить тяжёлые реакции.
Что это может значить для будущего лечения аллергий
Исследование даёт доказательство концепции, что один сконструированный «консенсусный» аллерген, доставляемый с помощью мРНК, может индуцировать широкий, перекрестно-реактивный и функционально блокирующий ответ IgG против целого семейства родственных пищевых и пыльцевых белков. Хотя текущий протокол ещё не защитил аллергичных мышей от анафилаксии, результаты указывают на гибкую платформу, которую можно улучшить путём корректировки дозы, адъювантов или пути введения. В перспективе такие основанные на консенсусе мРНК-терапии могут позволить лечить кластеры родственных аллергий — например, вызванных nsLTP, другими семействами растительных белков или даже быстро мутирующими патогенами — более короткими, более точными и более широко защищающими протоколами.
Цитирование: Møiniche, M., Johansen, K.H., Parrón-Ballesteros, J. et al. An mRNA-delivered consensus allergen induces a neutralizing IgG response against food and pollen allergens. Nat Commun 17, 2402 (2026). https://doi.org/10.1038/s41467-026-69134-4
Ключевые слова: пищевая аллергия, пыльцевая аллергия, мРНК-иммунотерапия, перекрестная реактивность, белки переноса липидов