Clear Sky Science · ru
Селективная на поздней стадии N‑Me алкенилизация и алкинилизация лекарств и неактивированных третичных аминов с использованием фоторедокс‑катализа
Почему важно улучшать устаревшие лекарства
Многие современные препараты действуют эффективно, но оставляют пространство для улучшений в безопасности, профиле побочных эффектов или точности воздействия на биологические мишени. Химики всё больше интересуются мягкой «доработкой» уже существующих лекарств на поздних стадиях разработки, вместо того чтобы создавать совершенно новые молекулы с нуля. В этой работе показано, как лучи видимого света можно использовать, чтобы прикреплять новые фрагменты к распространённому строительному блоку лекарств, получая улучшенные кандидаты в антидепрессанты и открывая более быстрый путь к оптимизированным препаратам.
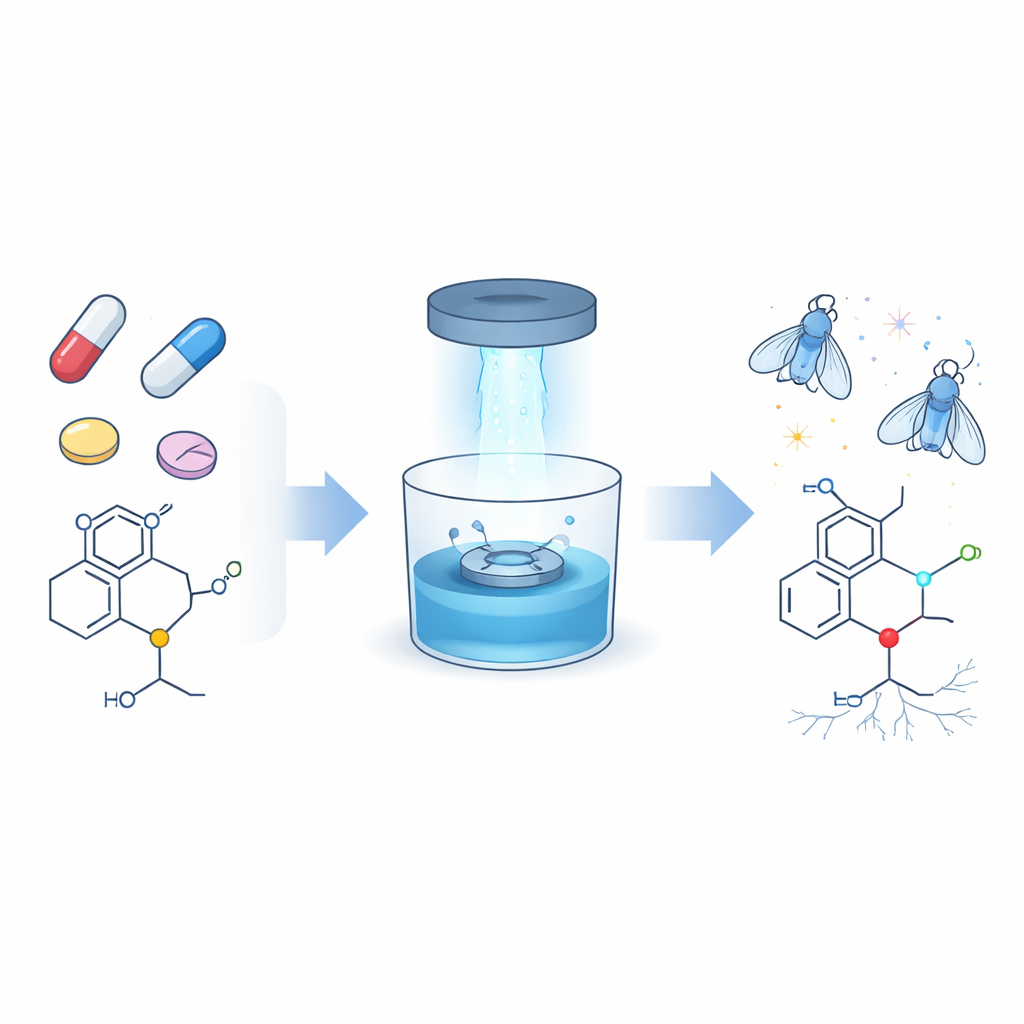
Модернизация распространённой части во многих лекарствах
Удивительно большая доля современных лекарств — более двух из пяти — содержит фрагменты, богатые азотом, называемые аминами, и большинство из них принадлежат к подтипу третичных аминов. Они встречаются в антибиотиках, противораковых препаратах, антигистаминных средствах, болеутоляющих и антидепрессантах. До сих пор химикам было трудно селективно модифицировать лишь одну крошечную часть этих групп — N‑метильную единицу — когда она находится среди нескольких практически одинаковых связей углерод–водород. Авторы поставили цель разработать мягкий, надёжный способ присоединять новые «ручки», а именно двойные связи углерод–углерод (алкены) и тройные связи (алкины), к этой N‑метильной позиции, не нарушая остальную часть молекулы лекарства.
Использование света для перестройки одной связи за раз
Команда обратилась к фоторедокс‑катализу — технологии, которая использует видимый свет и светочувствительный катализатор для перемещения одиночных электронов и запуска реакций в мягких условиях. В их системе синий свет возбуждает органический катализатор, который временно оттягивает электрон от третичного амина. Этот шаг создаёт кратковременный радикал на N‑метильной позиции, который может присоединяться к тщательно подобранным партнёрным молекулам, несущим винил- или алкинильные группы. Тонкая настройка условий реакции — выбор растворителя, основания и добавок — позволила исследователям добиться высоких выходов и отличного контроля, так что новая группа почти исключительно прикрепляется к N‑метилу, даже при наличии нескольких похожих участков. Метод продемонстрировали на широкой панораме простых аминов, а затем на реальных лекарствах, включая антигистаминные средства, препараты для сердца, антиинфекционные лекарства и несколько антидепрессантов.
От химической корректировки к более сильному антидепрессантному эффекту
Чтобы проверить, могут ли эти структурные изменения иметь медицинское значение, авторы сосредоточились на имипрамине — давно применяемом трициклическом антидепрессанте. Они разработали и промоделировали более двадцати вариантов имипрамина, в которых новое виниловое или алкинильное удлинение несло ароматические кольца, способные плотно войти в гидрофобный карман человеческого транспортёра серотонина — белка, контролирующего уровни серотонина, важного нейромедиатора настроения. Компьютерное докирование показало, что многие из модифицированных молекул должны связываться не хуже, а в ряде случаев лучше исходного препарата. Наиболее перспективные кандидаты затем синтезировали с помощью нового метода на свету и протестировали в живых системах: на модели депрессии у дрозофил, основанной на социальной изоляции, и для двух лучших соединений — в нервных клетках мыши, активно транспортирующих серотонин.
Как мухи и клетки показали более сильные препараты
У изолированных самцов плодовой мухи депрессивноподобное поведение проявляется в повышенной агрессии. Кормление имипрамином снижает эту агрессию, что отражает его антидепрессантное действие у человека. Поразительно, что несколько производных имипрамина, полученных новым методом, снижали агрессию не хуже, а четыре кандидата оказались ещё эффективнее самого имипрамина. В культивируемых гиппокампальных клетках мыши два ведущих соединения сильнее блокировали обратный захват серотонина, чем имипрамин — это подтвердили как прямые химические измерения серотонина, так и флуоресцентный краситель, светящийся при попадании в клетки. Эти тесты указывают, что тонкие позднесценарные изменения в N‑метильной позиции действительно могут повысить антидепрессантную силу, а не просто изменить молекулу «на бумаге».
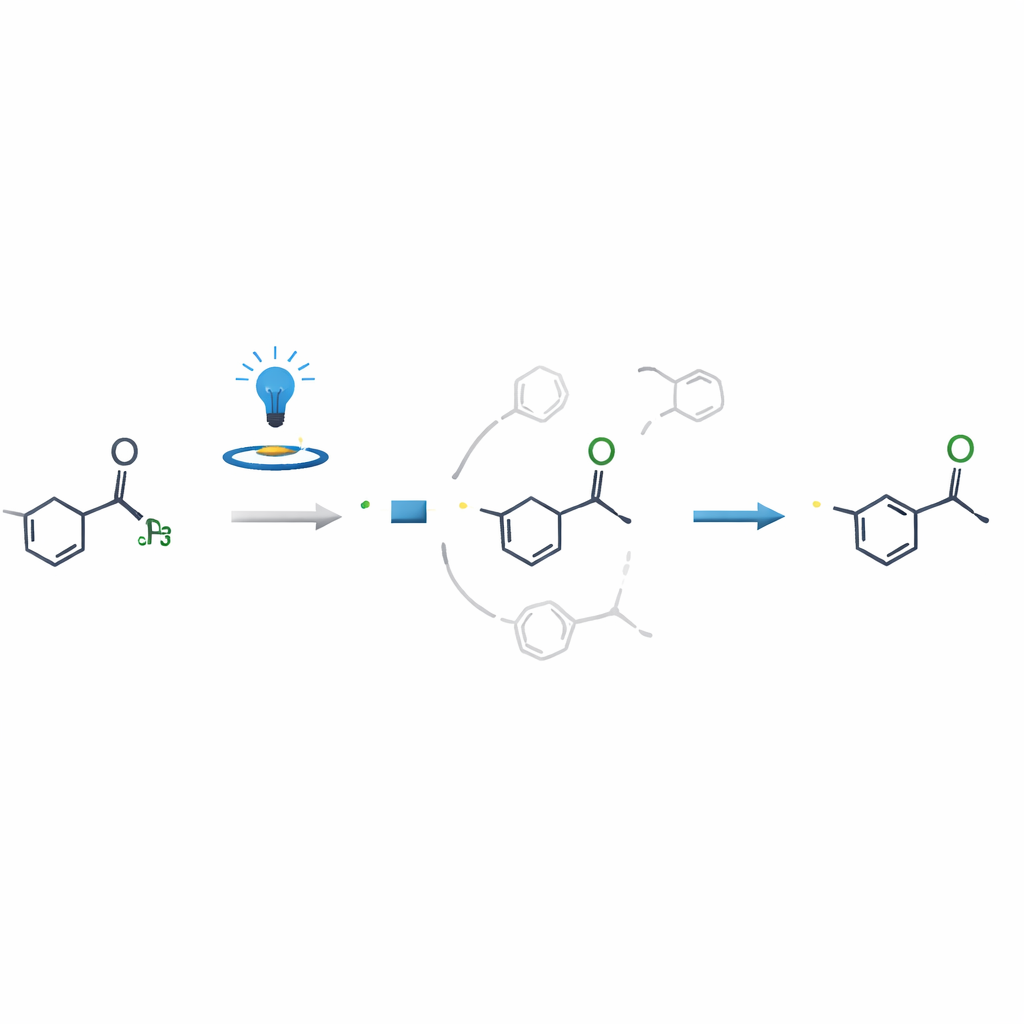
Почему реакция так селективна
Ключевой научный вопрос заключался в том, почему реакция так чисто модифицирует N‑метил, тогда как другие соседние позиции выглядят так же реактивными. Через контрольные эксперименты, измерения спин‑полей электронов и подробные компьютерные расчёты авторы показали, что критический момент решения происходит не при первичном образовании радикала, а при присоединении этого радикала к виниловому или алкинильному партнёру. Путь, ведущий от N‑метильного радикала к конечному продукту, как энергетически проще, так и гораздо быстрее, чем конкурирующие маршруты, что эффективно направляет реакцию к одному результату. Это понимание помогает объяснить высокую селективность и может направлять аналогичные стратегии для других сложных молекул.
Что это означает для будущих лекарств
В целом исследование представляет практичный способ «хирургической» модернизации существующих лекарств, содержащих третичные амины, добавляя компактные химические «ручки», которые могут настраивать их взаимодействие с биологическими мишенями или связывать с другими компонентами. Показав, что такие позднесценарные модификации способны превратить хорошо знакомый антидепрессант в ещё более эффективные варианты в простых животных и клеточных моделях, работа указывает на мощное сочетание современной синтетической химии, вычислительной химии и биологии. По мере расширения подхода на другие лекарства он может ускорить оптимизацию кандидатов в препараты и помочь обновить старые терапии с улучшенной эффективностью и безопасностью.
Цитирование: Paul, S., Mahato, S., Mahapatra, S.K. et al. Late-stage N-Me selective alkenylation and alkynylation of drugs and unactivated tertiary amines using photoredox catalysis. Nat Commun 17, 2695 (2026). https://doi.org/10.1038/s41467-026-69131-7
Ключевые слова: фоторедокс‑катализ, поздняя стадия функционализации, третичные амины, дизайн антидепрессантов, транспортёр серотонина