Clear Sky Science · ru
Изолируемый фосфоалуменен(3), способный активировать малые молекулы через уникальные режимы реактивности
Разрыв прочных связей новым химическим инструментом
Химики постоянно ищут способы заставить инертные молекулы реагировать. Многие повседневные вещества, от водорода до диоксида углерода, обладают высокой устойчивостью, что затрудняет их превращение в полезные продукты. В этой статье описан специально разработанный молекулярный фрагмент на основе алюминия и фосфора, который способен захватывать такие «неохотные» партнёры и разрывать их связи. Понимание и контроль подобных процессов активации связей однажды может помочь превращать отходящие газы в исходные материалы или предлагать более мягкие, экономящие металлы маршруты для синтеза тонких химикатов и материалов.
Дизайнерская связь между алюминием и фосфором
В центре исследования — редкий тип связи между двумя элементами главной подгруппы: алюминием и фосфором. Исследователи синтезировали молекулу, обозначенную в статье как «3», в которой эти два атома связаны плотной двойной связью. Чтобы предотвратить распад этой реакционноспособной пары, её «завернули» в объёмный органический каркас, защищающий от случайных реакций. Двумя разными синтетическими маршрутами авторы получили это соединение в изолируемой форме и вырастили одиночные кристаллы, пригодные для рентгеновского дифракционного анализа, что подтвердило короткую, напоминающую двойную связь связь между фосфором и алюминием, при том что оба атома окружены нитрогенсодержащими лигандами. Расчёты показали, что электроны неравномерно распределены между алюминием и фосфором, делая связь поляризованной и подготовленной к атакам со стороны других молекул.
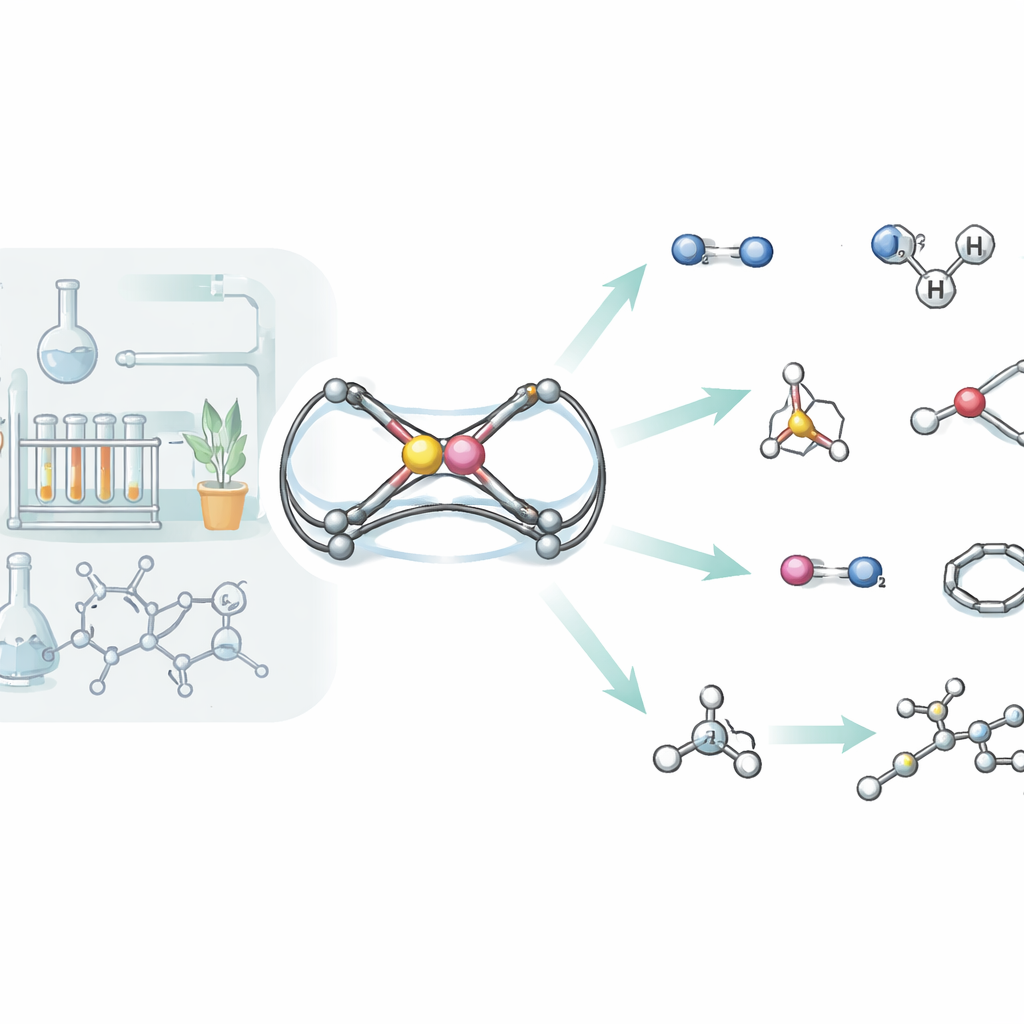
Как новая молекула взаимодействует с водородом
Водородный газ традиционно трудно разрывать без использования благородных металлов, однако новая алюминиево‑фосфорная единица справляется с этим. При контакте с водородом в мягких условиях комплекс реагирует двумя различными путями. В одном из них H–H связь просто присоединяется через Al=P, превращая её в две одинарные связи и прикрепляя по одному атому водорода к каждому центру. В другом случае молекула водорода разрывается кооперативно алюминием и соседним атомом азота — поведение, напоминающее так называемые «фрустрированные пары Льюиса», которые активируют водород без традиционных металлических катализаторов. Детальные компьютерные моделирования проследили оба пути, показав сопоставимые энергетические барьеры, что объясняет образование обоих продуктов бок о бок.
Разборка целой серии малых молекул
Водород — лишь начало. Команда систематически протестировала реактивность своей алюминиево‑фосфорной «шаблонной» структуры с широким набором малых молекул, включая белый фосфор, изоцианиды, диоксид углерода, закись азота, азид триметилсильного, селеновые димеры, силаны, амины, стирол и простые алкины. Во многих реакциях исходная связь Al=P полностью разрушается, и два атома оказываются вовлечены в крупные клеточные или циклические фрагменты, включающие фрагменты вступающей молекулы. Так, белый фосфор (P4) расщепляется и перестраивается в алюминиево‑фосфорную каркасную структуру, а диоксид углерода вставляется дважды, формируя шестичленный цикл, связывающий алюминий и фосфор через две новые углеродно‑кислородные мостики. В реакциях с силанами и аминами молекула ведёт себя скорее как классическая двойная связь: входящая единица Si–H или N–H аккуратно присоединяется через Al=P, вновь демонстрируя «π‑характер» этой необычной связи.
Почему важен окружающий каркас
Один из ключевых выводов работы состоит в том, что объёмный, богатый азотом каркас вокруг единицы Al=P — это не просто подложка; он направляет, как и где протекают реакции. Сравнивая свои результаты с предыдущими, более краткоживущими системами алюминий‑фосфор, авторы показывают, что небольшие изменения в поддерживающих лигандах меняют баланс между различными путями — например, простым присоединением через двойную связь и более сложным разрывом связей с образованием колец. Сложные анализы распределения электронов выявили сильную поляризацию связи Al=P и подчеркнули, как соседние атомы азота могут сотрудничать с алюминием, особенно при активации водорода. Стерические факторы — физическая загруженность большими группами — также направляют входящие молекулы к одному или другому реактивному центру.
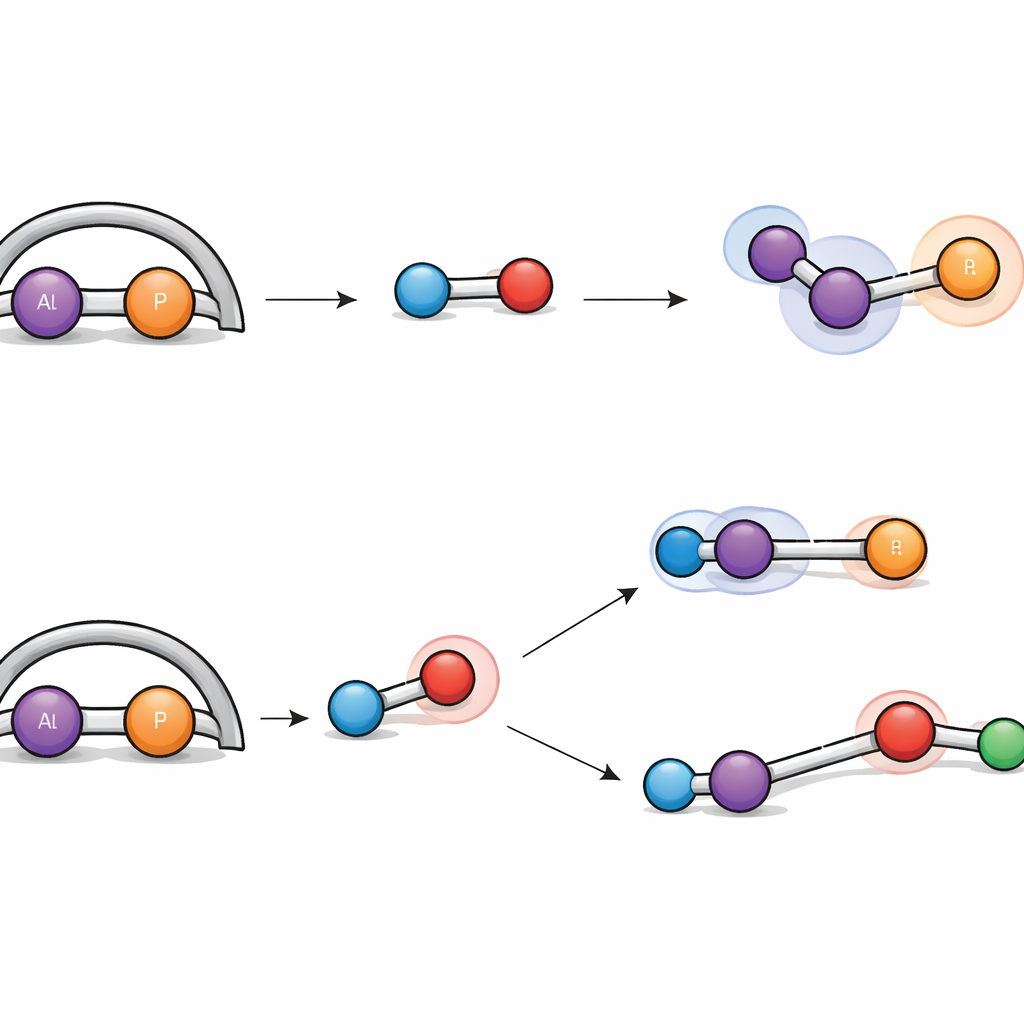
Что это значит для будущей химии
Неспециалисту перечень реагентов в этом исследовании может показаться отдалённым, но основная мысль ясна: точная настройка как связей, так и формы вокруг элементов главной подгруппы позволяет химикам создавать гибкие инструменты, соперничающие или дополняющие традиционные металлические катализаторы. Этот изолируемый алюминиево‑фосфорный комплекс не просто сохраняется в флаконе, он работает с широким набором трудных малых молекул в мягких условиях — разрывает водород, реконструирует белый фосфор и захватывает диоксид углерода. Работа показывает, что тонкие изменения в «ручке» молекулы могут кардинально перенаправлять её реактивность, предлагая план действий для проектирования будущих катализаторов, которые помогут преобразовывать простые, стабильные молекулы в более ценные продукты точно и эффективно.
Цитирование: Cha, Y., Yang, Z., Zhuang, X. et al. An isolable phosphaalumene(3) capable of small molecule activation via unique modes of reactivity. Nat Commun 17, 2390 (2026). https://doi.org/10.1038/s41467-026-69118-4
Ключевые слова: активация малых молекул, химия главной подгруппы, двойная связь алюминий‑фосфор, фрустрированная пара Льюиса, механизмы разрыва связей