Clear Sky Science · ru
Механизм ингибирования грибковых β−1,3-глюкансинтаз тритерпеноидными противогрибковыми препаратами
Почему важно останавливать грибковые инфекции
Грибковые инфекции тихо уносят более миллиона жизней в год и угрожают урожаям и экосистемам по всему миру. Врачам доступны лишь немногие противогрибковые средства, и некоторые опасные грибы эволюционируют, чтобы обходить их. В этом исследовании в молекулярных подробностях показано, как новый класс противогрибковых препаратов прикрепляется к ключевому ферменту, необходимому грибам для построения защитной клеточной стенки, и отключает его. Понимание этого процесса дает дорожную карту для разработки более эффективных средств, способных опередить устойчивые штаммы.
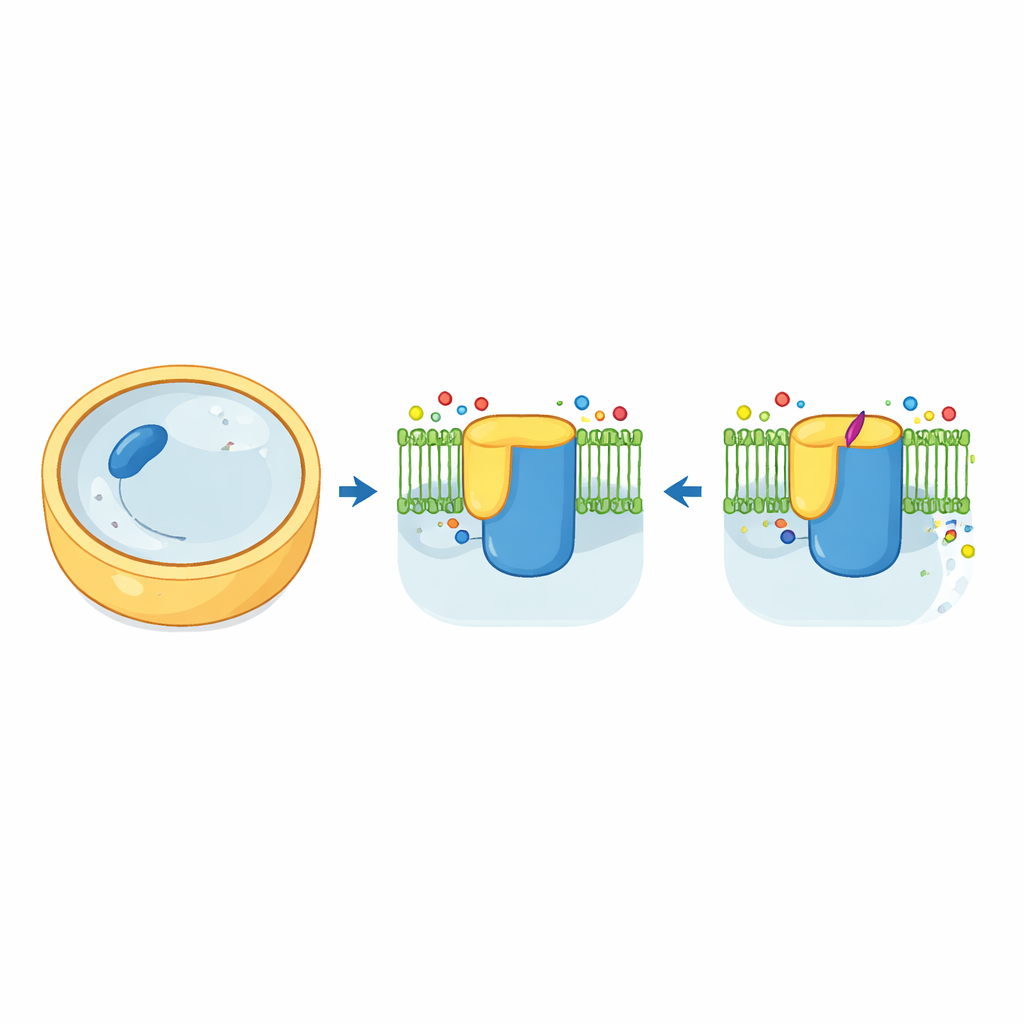
«Кирпичник» клеточной стенки грибов
Клетки грибов окружены прочной стенкой, главным образом состоящей из полимера на основе сахара — бета-1,3-глюкана. Фермент, который синтезирует и экспортирует этот полимер — β-1,3-глюкансинтаза — работает как сочетание кирпичного мастерского цеха и конвейера. В пекарских дрожжах этот комплекс состоит из двух очень похожих вариантов, Fks1 и Fks2, каждый встроен в мембрану клетки и управляется небольшим вспомогательным белком Rho1. С помощью криоэлектронной микроскопии авторы получили трехмерные снимки высокого разрешения как Fks1, так и Fks2 в их естественной форме. Структуры показывают большую цитозольную «рабочую поверхность», связанную с «лесом» мембрано-пронзающих спиралей, с центральной полостью, которая, по-видимому, служит туннелем, через который растущая цепочка глюкана выходит из клетки.
Как природный препарат хватается за фермент
Клинически важные тритерпеноидные препараты, включая пероральный ибрексафунгерп, происходят от природного соединения энфумафунгина. До сих пор не было ясно, где именно на глюкансинтазе эти препараты связываются. Исследователи решили структуры Fks1 и Fks2, связанные с энфумафунгином. Удивительно, но препарат не вклинивается в активный сайт, где соединяются сахарные звенья. Вместо этого он располагается на наружной стороне одной мембранной спирали, называемой TM5, сидя в мембране примерно в трех нанометрах от каталитического центра и рядом с вероятным каналом выхода глюкана. Ключевые аминокислоты в этом участке поддерживают гидрофобное ядро препарата и контактируют с его кислотным хвостом, тогда как сахарная добавка препарата почти не касается белка — что объясняет, почему химики могли модифицировать эту часть, не теряя активности.
Препараты, которые застывают движущуюся машину
На первый взгляд общая форма фермента с энфумафунгином и без него выглядит почти неизменной. Решающее различие заключается в организации окружающих липидов и гибкости некоторых спиралей. При связывании препарата соседняя ароматическая боковая цепь поворачивается, чтобы зажать энфумафунгин на месте и вместе с другим остатком стабилизирует упорядоченный липид рядом с препаратом. Дополнительные стеролоподобные липиды аккуратно располагаются вокруг набора горизонтальных спиралей, которые помогают определять путь экспорта глюкана. Эти липиды действуют как клинья и подпорки, фиксируя спирали и вход в канал в определенном «базальном» положении. Генетические испытания показывают, что изменение многих точек контакта для препарата или этих стеролов ослабляет связывание препарата или разрушает функцию фермента, и мутации в этих участках соответствуют известным мутациям, дающим резистентность, у патогенов человека и растений.
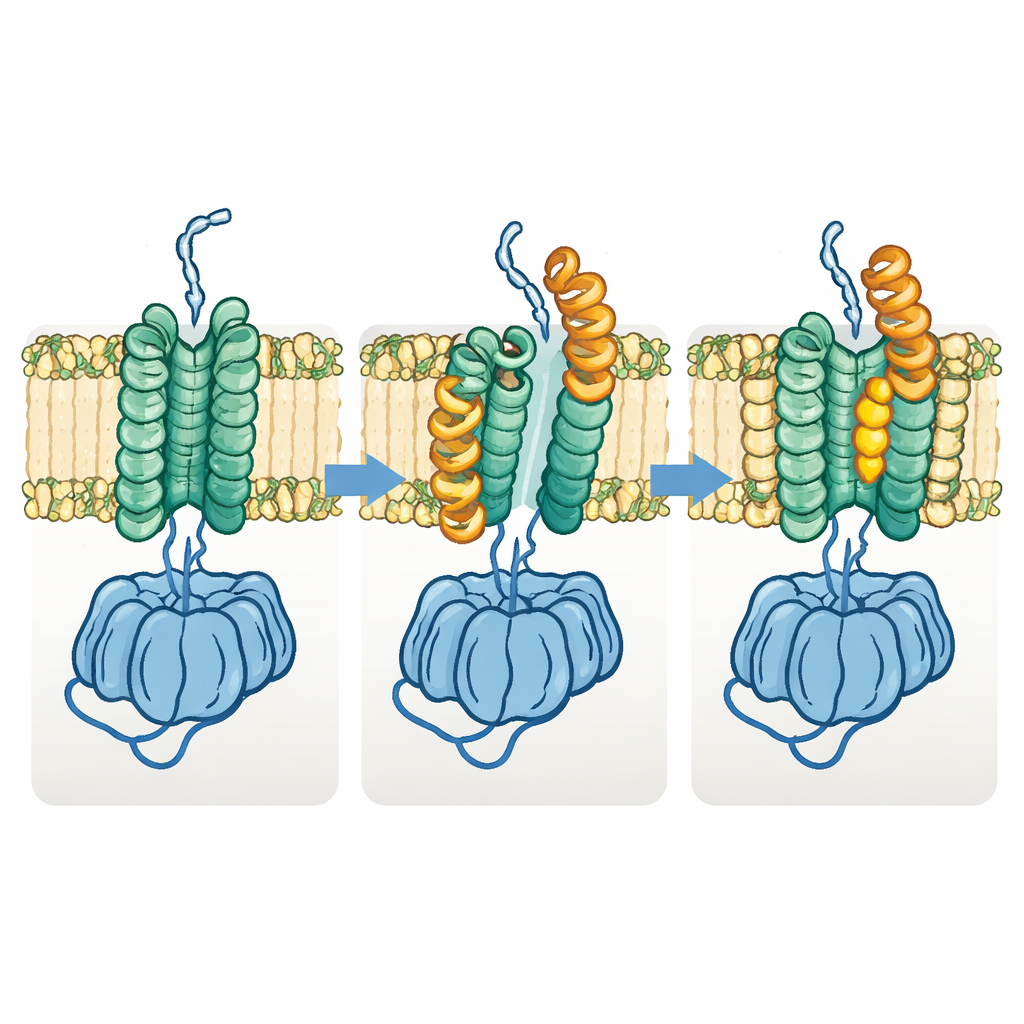
Необходимое изменение формы для транспорта полимера
Команда также обнаружила отличную «открытую» форму Fks1. В этом состоянии одна половина мембранной области смещается вбок, а ключевые горизонтальные спирали отводятся наружу, раздвигая пространство между двумя мембранными пучками и расширяя видимый туннель для глюкана. Сравнение множества структур указывает на то, что фермент циклично переключается между базальным и открытым состояниями во время нормальной работы: базальное состояние подготавливает и инициирует формирование полимера, тогда как открытое позволяет растущей цепочке латерально перемещаться через мембрану наружу. Когда авторы конструировали дисульфидные связи, предназначенные для постоянной фиксации фермента в одном из состояний, обе варианты в значительной мере утратили активность, что подтверждает идею о том, что это изменение формы необходимо для функции.
Что это значит для будущих противогрибковых препаратов
Показав, что энфумафунгин и родственные препараты действуют не блокированием каталитического кармана, а перестроением локальной мембранной среды и «замораживанием» глюкансинтазы в базальном состоянии, это исследование выявляет нетрадиционный механизм действия лекарства. Оно также демонстрирует, что Fks1 и Fks2 имеют почти идентичные структуры и ответ на препараты, объясняя, почему оба необходимо учитывать при борьбе с резистентностью. В более широком смысле работа подчеркивает, как малые молекулы могут контролировать «нелекарственные» мембранные белки, связываясь с неглубокими поверхностями и рекрутируя липиды, предлагая концептуальный план для разработки противогрибковых средств следующего поколения, сохраняющих эффективность по мере эволюции грибов.
Цитирование: You, ZL., Sun, L., Wang, LX. et al. Inhibition mechanism of the fungal β−1,3-glucan synthases by triterpenoid antifungal drugs. Nat Commun 17, 2347 (2026). https://doi.org/10.1038/s41467-026-69114-8
Ключевые слова: противогрибковые препараты, клеточная стенка грибов, глюкансинтаза, резистентность к препаратам, криоэлектронная микроскопия