Clear Sky Science · ru
Острый перитонит индуцирует адипоЗные CD127+ ILC1, экспрессирующие PD-L1 и смягчающие воспаление у мышей
Почему жировая ткань живота помогает бороться со смертельной инфекцией
Когда бактерии просачиваются из повреждённого кишечника в брюшную полость, организм может впасть в угрожающее жизни состояние — сепсис. В этом исследовании выявлен неожиданный союзник: особая популяция иммунных клеток, скрывающихся в брюшном жире, которая мигрирует в ранней стадии инфекции и служит встроенным тормозом для неукротимого воспаления. Понимание механизмов их работы может подсказать новые подходы к лечению, убаюкивающие опасное воспаление, но не подавляющие полностью иммунную систему.
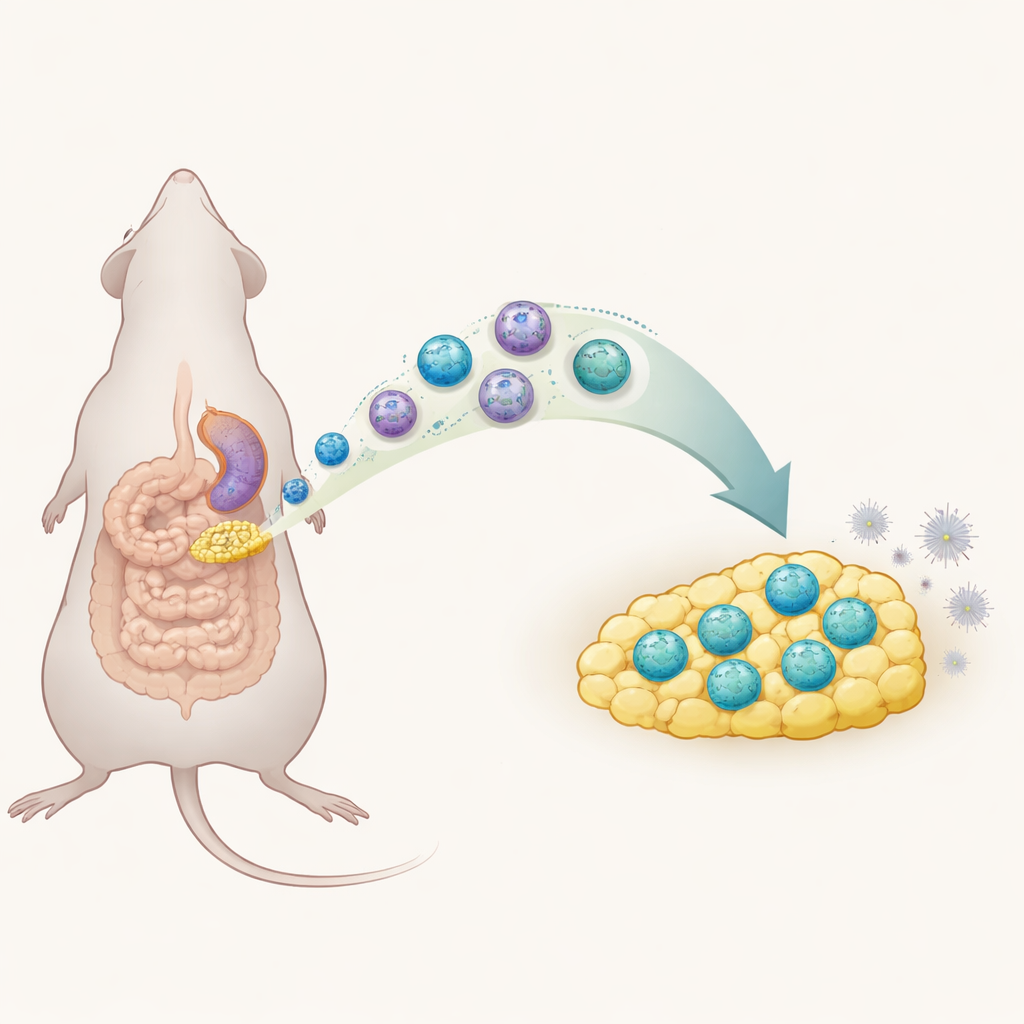
Опасная утечка в брюшной полости
Перитонит возникает, когда воспаляется оболочка брюшной полости, чаще всего из‑за выхода бактерий из перфорированного кишечника. Если начальную бурю воспаления не сдержать, у пациентов может развиться сепсис, который, несмотря на современную помощь, по‑прежнему уносит примерно каждого пятого заболевшего. Врачи могут бороться с источником инфекции хирургически и антибиотиками, но у них мало средств, чтобы перенастроить собственный иммунный ответ организма так, чтобы он не скатывался в вредный гиперответ. Жировая ткань, покрывающая кишечник — мезентериальная жировая ткань — известна тем, что стягивается к очагам повреждения кишки, что намекает на её активную роль в раннем иммунном ответе.
Скрытые стражи в жировой ткани живота
В последние годы учёные открыли «врожденные лимфоидные клетки» — быстро реагирующие иммунные дозорные, обитающие во многих тканях. Один подтип, называемый группой 1 ILC, обычно помогает запускать сильные воспалительные реакции. В этой работе на мышах исследователи использовали стандартную хирургическую модель перитонита, чтобы выяснить, как эти клетки ведут себя в мезентериальном жире. Они обнаружили, что через шесть часов после повреждения в этой жировой ткани усилились воспалительные сигналы и произошёл всплеск ILC1, тогда как другие родственники этих клеток почти не изменились. Это время совпадало с пиком тяжести заболевания у животных, что указывает на тесную связь ILC1 с ранней фазой воспаления в брюшной полости.
Путешествующие клетки, меняющие свою природу
Углубив анализ, команда применила методы одно‑клеточного профилирования и разделила популяцию ILC1 на подклассы. При нормальных условиях большинство ILC1 в брюшном жире не несли на поверхности молекулу CD127. Однако при остром перитоните появилась новая группа CD127‑положительных ILC1, которая расширилась. Эти новички вырабатывали меньше мощного провоспалительного сигнала интерферона‑гамма по сравнению с CD127‑отрицательными сородичами, что делало их относительно сдержанными. Учёные показали, что многие из этих клеток не просто делились на месте: ILC1 из селезёнки мигрировали через кровоток в мезентериальную жировую ткань, чему отчасти способствовал химический «гоминг»-сигнал CXCL10 и его рецептор CXCR3. Оказавшись в жире, они изменяли маркеры на поверхности, приобретая CD127 и принимая более спокойную, регуляторную роль.
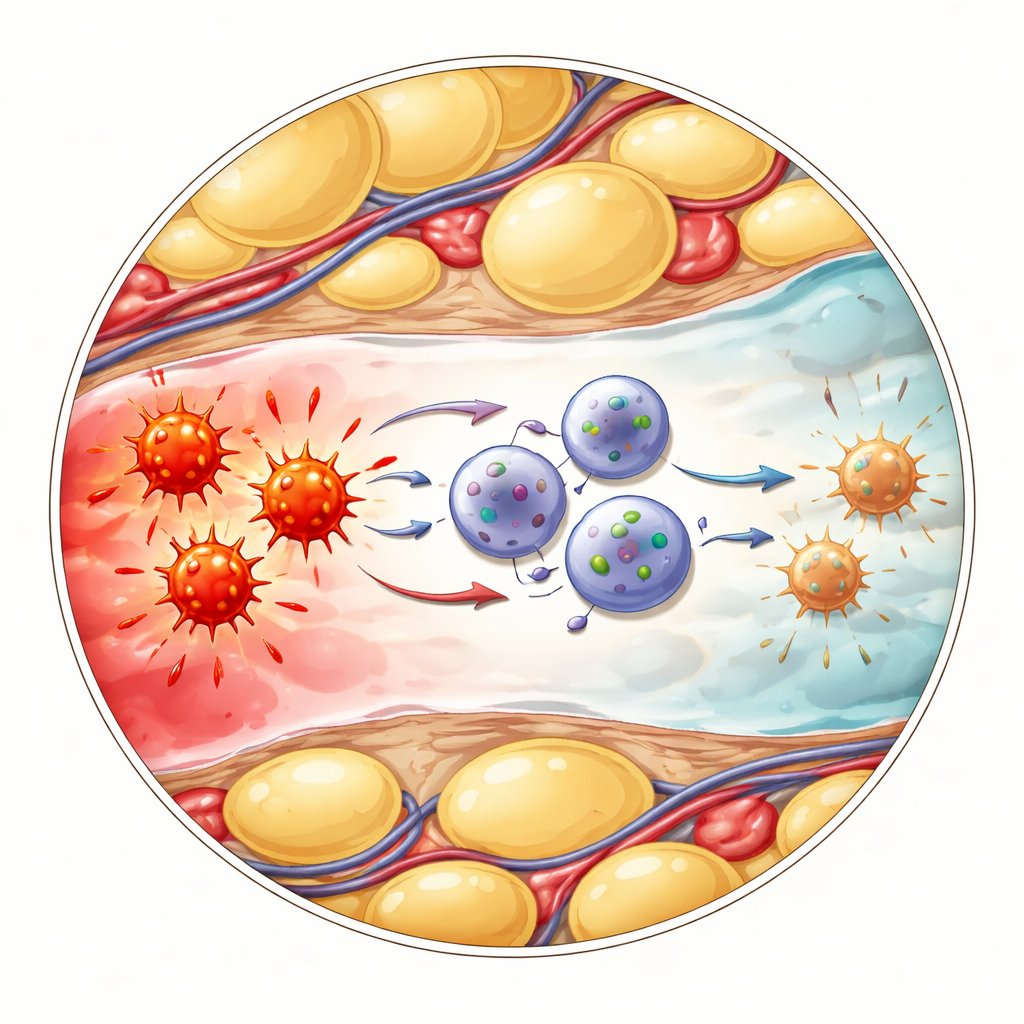
Как успокаивающие клетки общаются с «огненными» клетками
Следующий вопрос — как именно эти изменённые ILC1 охлаждают воспаление. Исследователи сосредоточились на другой иммунной группе — γδ T-клетках, которые быстро реагируют на опасность и способны выделять большие количества молекулы‑тревоги TNF. Анализ на уровне отдельных клеток показал, что CD127‑положительные ILC1 и γδ T-клетки взаимодействуют через хорошо известный тормозной путь с участием поверхностных белков PD‑L1 и PD‑1. В воспалённом брюшном жире недавно прибывшие ILC1 сильно увеличивали экспрессию PD‑L1, а соседние γδ T‑клетки демонстрировали высокий уровень PD‑1. Когда команда блокировала PD‑1 антителами, γδ T‑клетки выделяли больше TNF, что подтвердило: контакт по этой оси обычно сдерживает их провоспалительную активность. Аналогично, мыши, генетически лишённые ILC1, переносили более тяжёлое заболевание, имели повышенные маркеры воспаления и больше TNF от γδ T‑клеток — эффекты, которые можно было ослабить прямой блокадой TNF.
Что это означает для будущих лечений
Собрав воедино результаты, авторы предлагают концепцию «селезёнка→брюшной жир»: вскоре после того, как бактерии попадают в брюшную полость, ILC1 покидают селезёнку, направляются в мезентериальную жировую ткань и там трансформируются в клетки, богатые CD127 и PD‑L1, которые подавляют продукцию TNF γδ T‑клетками. Вместо того чтобы подливать масло в огонь, эти специализированные ILC1 выступают локальными миротворцами, не давая воспалению выйти из‑под контроля и, возможно, помогая предотвратить прогрессирование перитонита в смертельный сепсис. В перспективе препараты, усиливающие или имитирующие этот регуляторный контур в брюшном жире, могли бы стать новым способом лечения тяжёлых инфекций — тонко настраивая иммунный ответ так, чтобы он оставался достаточным для борьбы с микробами, но не опасным для пациента.
Цитирование: Nagata, R., Akama, Y., Goncalves, P. et al. Acute peritonitis-induced adipose CD127+ ILC1s express PD-L1 and ameliorate inflammation in mice. Nat Commun 17, 2391 (2026). https://doi.org/10.1038/s41467-026-69100-0
Ключевые слова: перитонит, врожденные лимфоидные клетки, мезентериальная жировая ткань, иммунная регуляция, сепсис