Clear Sky Science · ru
Комбинаторная синтетическая стратегия для разработки агентов доставки белков для редактирования генома, нацеленных на сетчатку мыши
Новая надежда в лечении наследственной слепоты
Многие формы наследственной слепоты начинаются с одной дефектной копии гена в светочувствительных клетках на задней стороне глаза. Современные инструменты редактирования генов, такие как CRISPR, теоретически могут исправить эти ошибки, но безопасная доставка машин редактирования в нужные клетки остаётся серьёзным препятствием. В этом исследовании описан новый способ транспортировки мощных редакторов генов прямо в сетчатку мыши с помощью специально разработанных жиро-подобных частиц, что открывает перспективу одноразовых лечений, восстанавливающих зрение при наследственных заболеваниях глаза.
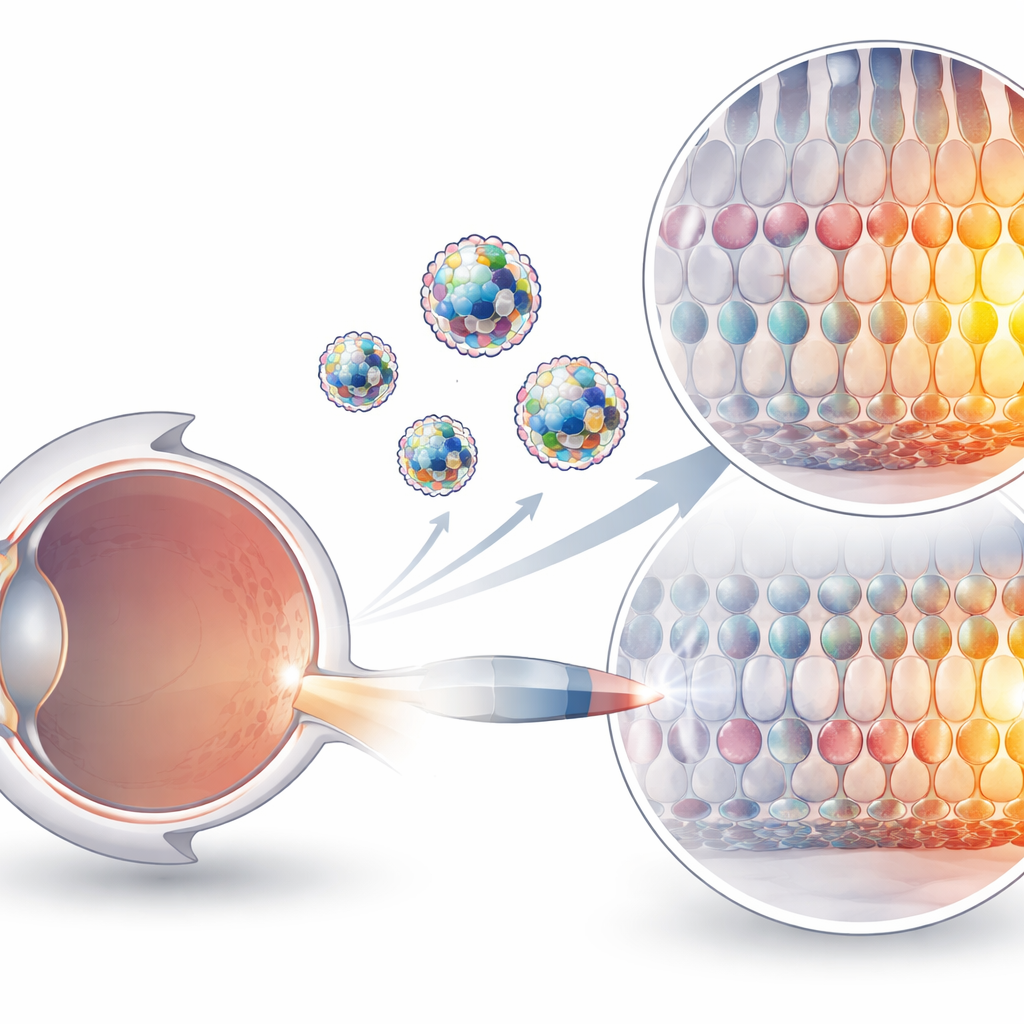
Почему доставить редакторы генов так сложно
Инструменты на базе CRISPR теперь могут менять отдельные буквы ДНК без разрезания обеих нитей — это достижение делает их привлекательными для лечения генетических нарушений. Но эти инструменты представляют собой громоздкие комплексы белок–РНК, которые заряжены и хрупки в организме. Современные методы доставки в основном опираются на модифицированные вирусы или на частицы, несущие генетические инструкции для редактора, а не сам редактор. Вирусы могут вызывать иммунные реакции и имеют строгие ограничения по размеру, тогда как доставка матричной РНК хорошо работает в печени, но остаётся неэффективной во многих других тканях, включая глаз. Прямая инъекция предварительно собранных комплексов белок–РНК концептуально чище и безопаснее, однако им не хватало подходящего носителя, который помог бы им пересечь клеточные мембраны и добраться до целей.
Шаттл для белков, вдохновлённый красителем
Исследователи обратились к неожиданной отправной точке: Коомассие Бриллиантовый Синий, тёмно-синий краситель, широко используемый в лабораториях и уже одобренный для некоторых офтальмологических операций. Этот краситель плотно связывается со многими белками. Команда химически связала «головки» Коомассие с жиро-подобными «хвостами», создав семейство новых молекул, названных липидоидами. В воде эти липидоиды склонны к образованию кластеров — частиц, в которых масляные части скрыты внутри, а группы Коомассие выступают наружу и могут захватывать белки. Меняя длину, разветвлённость и заряд хвостов, учёные создали десятки кандидатных соединений, предназначенных связывать белки-редакторы с одной стороны и взаимодействовать с клеточными мембранами с другой.
Тестирование доставки белков в клетки глаза
Чтобы понять, какие конструкции действительно работают, группа сначала использовала простой тестовый белок — Cre-рекомбинезу, который переключает генетический маркер с зелёного на красный или наоборот в модифицированных клетках и мышах. Несколько липидоидов Коомассие эффективно переносили Cre в культивируемые клетки, переводя значительную долю клеток из зелёного в красный цвет. При инъекции под сетчатку у сообщающих об экспрессии мышей выбранные соединения вызывали впечатляющие цветовые изменения как в пигментном слое, поддерживающем зрение, так и в светочувствительных фоторецепторах, что демонстрировало попадание белков в те клетки, которые затронуты при многих слепящих болезнях. Эти ранние эксперименты также показали, что тонкие изменения в структуре липидоида могут смещать направленность на разные типы клеток, указывая на возможность будущей настройки для конкретных слоёв сетчатки.
Усиление редактирования генов и восстановление зрения
Далее команда загрузила систему адениновым базовым редактором, усовершенствованным вариантом CRISPR, который может исправить конкретную однобуквенную мутацию, вызывающую потерю зрения у мышей rd12, модели тяжёлой детской слепоты. Сам по себе комплекс белок–РНК плохо проникал в клетки. Один липидоид, названный CBB11, улучшал доставку, но имел склонность к агрегации в растворе. Чтобы стабилизировать его, исследователи встроили CBB11 в мелкие, чётко определённые липосомы — полые сферы из нескольких типов липидов, включающих клинически используемые компоненты из вакцин на основе мРНК. В этих составах CBB11 на поверхности липосомы захватывал белковую часть редактора, в то время как другие липиды помогали связывать направляющую РНК, создавая кооперативную оболочку, которая удерживала весь комплекс на внешней поверхности частицы.
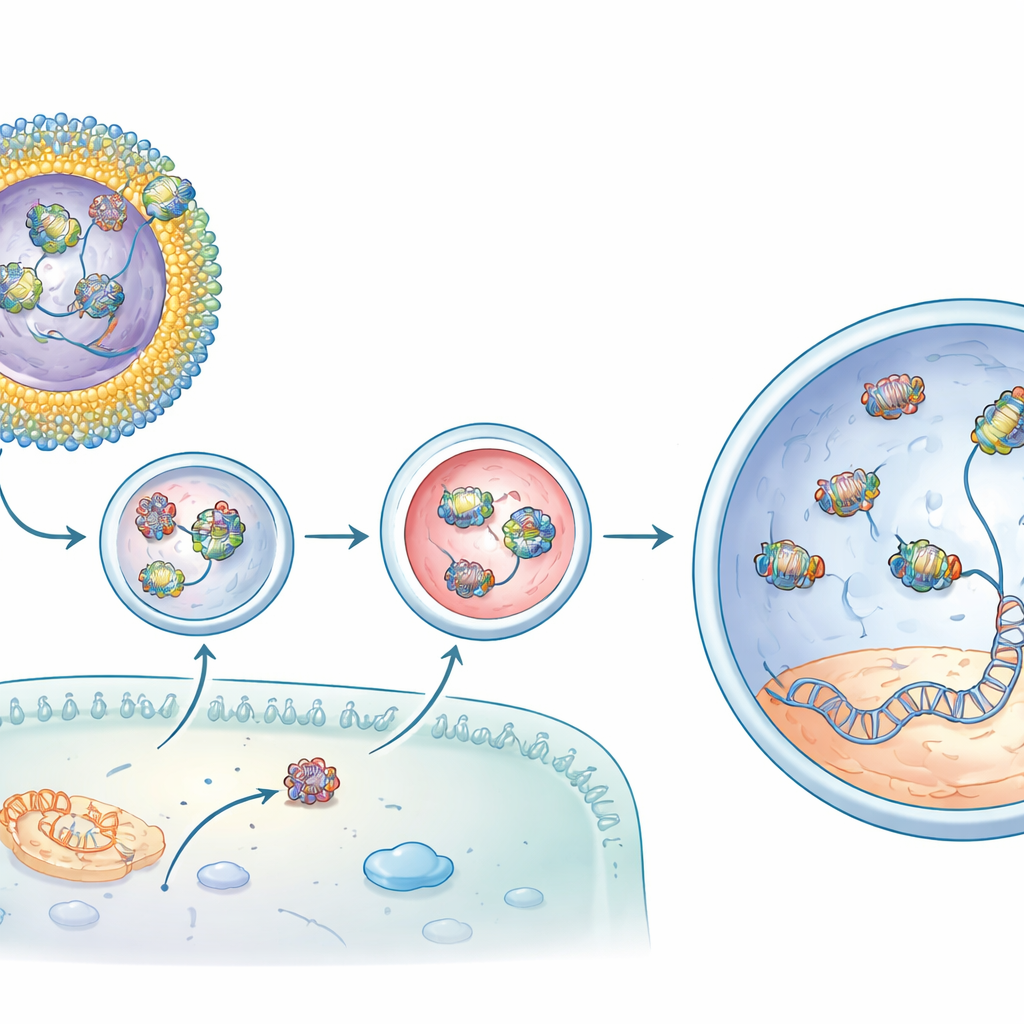
От молекулярного ремонта к восстановлению светочувствительности
Когда такие липосомы, содержащие CBB11 и несущие базовый редактор, вводили под сетчатку мышей rd12, результаты были впечатляющими. По сравнению с редактором, введённым в одиночку, оптимизированная формула увеличивала желаемую коррекцию ДНК в целевом гене более чем на порядок и давала ещё более высокие уровни скорректированной матричной РНК. Химический анализ показал восстановление светочувствительного пигмента сетчатки, который отсутствует при заболевании. Наиболее убедительно — электрические записи из глаз животных показали, что их палочковые клетки восстановили большую часть способности реагировать на тусклый свет — в лучших случаях до примерно трёх четвертей сигнала нормальной мыши. Внецелевые изменения в других участках генома находились на уровне фоновых значений, что указывает на высокую эффективность и точность редактирования.
Что это может значить для будущих терапий глаза
Для неспециалиста ключевой вывод заключается в том, что авторы создали многоразовый «шаттл» для белков-редакторов генов, который работает прямо в живом глазу. Украшая безопасные, напоминающие вакцину жиро-подобные частицы белко‑захватывающим красителем, они создали систему, способную захватывать разные редакторы на своей поверхности, доставлять их в клетки сетчатки, исправлять мутации, вызывающие болезнь, и заметно восстанавливать зрение у мышей после однократного лечения. Хотя потребуется дополнительная работа для полной оценки безопасности, улучшения таргетинга и адаптации метода для человека, эта платформа указывает путь к будущим одноразовым точным лекарствам при наследственных заболеваниях сетчатки и, возможно, при других генетических состояниях, где аккуратный локализованный ремонт ДНК может решить разницу между слепотой и зрением.
Цитирование: Zhang, J., Hołubowicz, R., Smidak, R. et al. A combinatorial synthetic strategy for developing genome-editing protein-delivery agents targeting mouse retina. Nat Commun 17, 2479 (2026). https://doi.org/10.1038/s41467-026-69077-w
Ключевые слова: терапия генов сетчатки, аддитивное редактирование CRISPR, липосомы, доставка белков, наследственная слепота