Clear Sky Science · ru
Взгляд на структуру и модуляцию человеческого TWIK-2
Почему этот крошечный «затвор» в наших клетках важен
Глубоко внутри наших клеток микроскопические ворота из белка контролируют поток заряженных атомов, формируя то, как нервные клетки генерируют импульсы, как сокращаются кровеносные сосуды и как реагирует иммунная система. Один из таких ворот — называемый TWIK-2 — связан с повышенным давлением в лёгочных сосудах и вредным воспалением, но до настоящего времени учёные знали очень мало о его строении и о том, как управлять им с помощью лекарств. В этом исследовании показана детальная структура человеческого TWIK-2, продемонстрированы его электрические свойства и наметены пути для целевой разработки новых противовоспалительных препаратов.
«Тихий» канал с большими последствиями для здоровья
TWIK-2 принадлежит к широкой семейству «утечечных» калиевых каналов, которые помогают устанавливать покоящееся напряжение клетки, позволяя ионам калия перемещаться через мембрану. В то время как другие представители этого семейства, например TREK и TASK, подробно изучены и связаны с болью и настроением, TWIK-2 оставался малоизученным, потому что его трудно регистрировать и он плохо экспрессируется в стандартных лабораторных системах. Тем не менее исследования на животных и клеточных моделях связывают TWIK-2 с лёгочной гипертензией, острым повреждением лёгких, потерей слуха и активацией иммунного комплекса NLRP3, который вызывает разрушительное воспаление при сепсисе и других заболеваниях. Понимание работы TWIK-2 поэтому важно и для фундаментальной биологии, и для разработки направленных терапий.
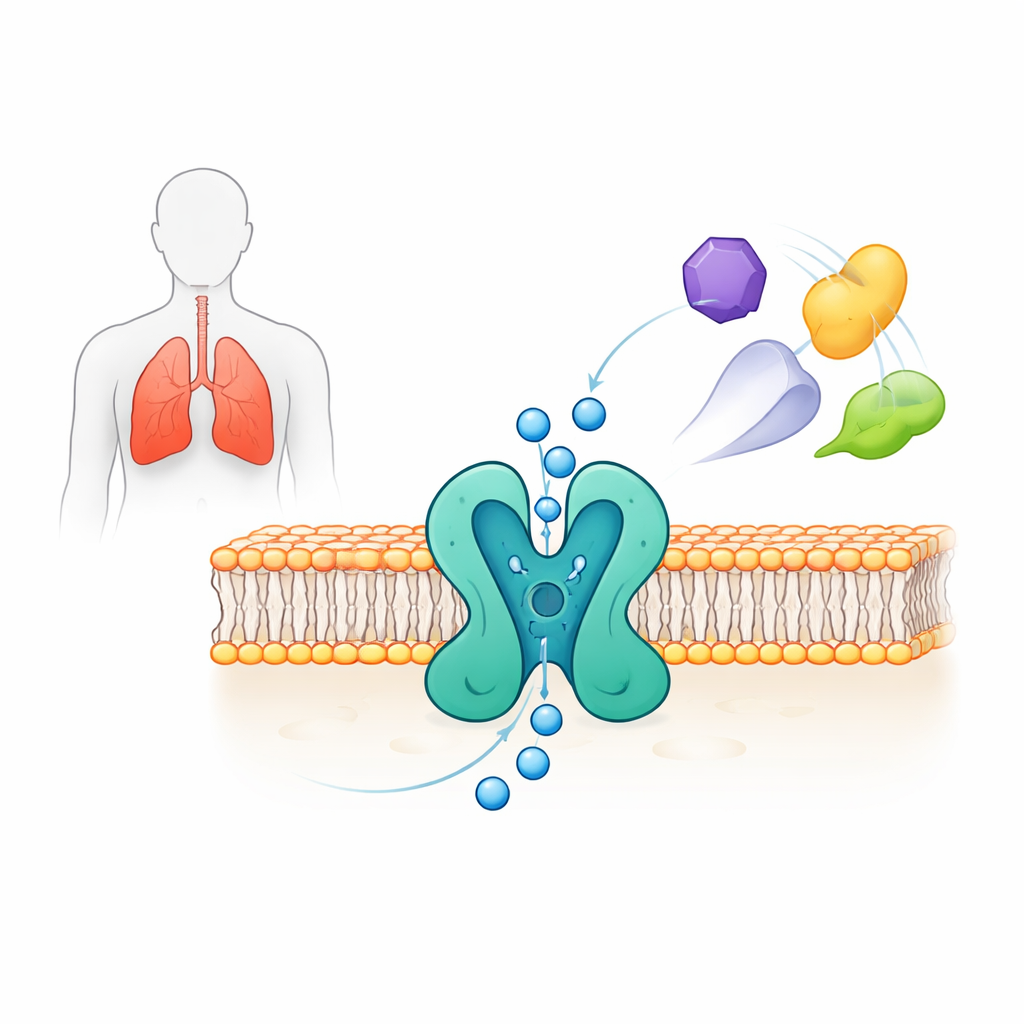
Наблюдение «затвора» с атомной точностью
Исследователи экспрессировали полный человеческий TWIK-2 в клеточных линиях человека и использовали сингл-парттикл крио‑электронную микроскопию для определения трёхмерной структуры с разрешением около 3,7 ангстрема. Канал образует сборку из двух частей, которые вместе создают центральную пору для прохождения ионов калия. Каждая половина содержит четыре трансмембранных сегмента и две «поровые» спирали, формирующие узкую область, называемую селективным фильтром, где калий отделяется от других ионов. Над порой две аркообразные «крышки» создают две отдельные входные траектории для ионов с внешней стороны клетки. Структура также выявляет тонкие асимметрии между двумя сторонами поры, придающие TWIK-2 псевдо‑четырёхчастную организацию — характерную черту этого семейства каналов.
Скрытые липиды и тонко настроенный путь для ионов
Вдоль проводящего пути исследователи проследили, как ионы калия движутся из внутренней части клетки через гидрофобный «манжет», поднимаются через селективный фильтр и выходят под крышкой. Самая узкая точка по-прежнему достаточно широка, чтобы калий мог проходить в один ряд. Хотя белок очищали без добавления липидов, карты крио‑ЭМ показали трубчатые плотности, расположенные в нижней части поры и в боковых карманах между спиралями. Эти плотности, вероятно, соответствуют липидам или хвостам детергентов, прилипшим к TWIK-2 во время очистки, что указывает на то, что природные мембранные жиры могут занимать эти борозды и слегка сдвигать форму соседних спиралей. Такие сдвиги, особенно в спирали M4 и в петлях селективного фильтра, считаются ключевыми для настройки состояний канала — открытого, закрытого или промежуточного.
Изучение «затвора» с помощью мутаций и блокаторов
Чтобы связать структуру с функцией, учёные использовали автоматизированную систему патч‑клампа для измерения токов в клетках, экспрессирующих либо нормальный TWIK-2, либо варианты с изменёнными аминокислотами. Они обнаружили, что TWIK-2 сильно зависит от напряжения, но, в отличие от своего сородича TWIK-1, в значительной степени нечувствителен к изменениям внешней кислотности. Мутации в двух консервативных треонинах у основания селективного фильтра сделали канал открывающимся быстрее и пропускающим больший ток, что свидетельствует о том, что эти участки действуют как ключевые «шарниры», стабилизирующие закрытое состояние. Изменения на входе и выходе поры влияли на скорость включения и выключения канала, показывая, насколько тщательно регулируется путь для ионов. Затем команда протестировала четыре известных малых молекулы, модифицирующие родственные каналы. Две из них, ML365 и NPBA, мощно блокировали TWIK-2, тогда как другие не оказывали эффекта. Сопоставляя, как различные мутации меняли чувствительность к препаратам, авторы пришли к выводу, что эти соединения, вероятно, связываются прямо под селективным фильтром и в соседних полостях, причём разные лекарства используют частично перекрывающиеся, но различные режимы связывания.
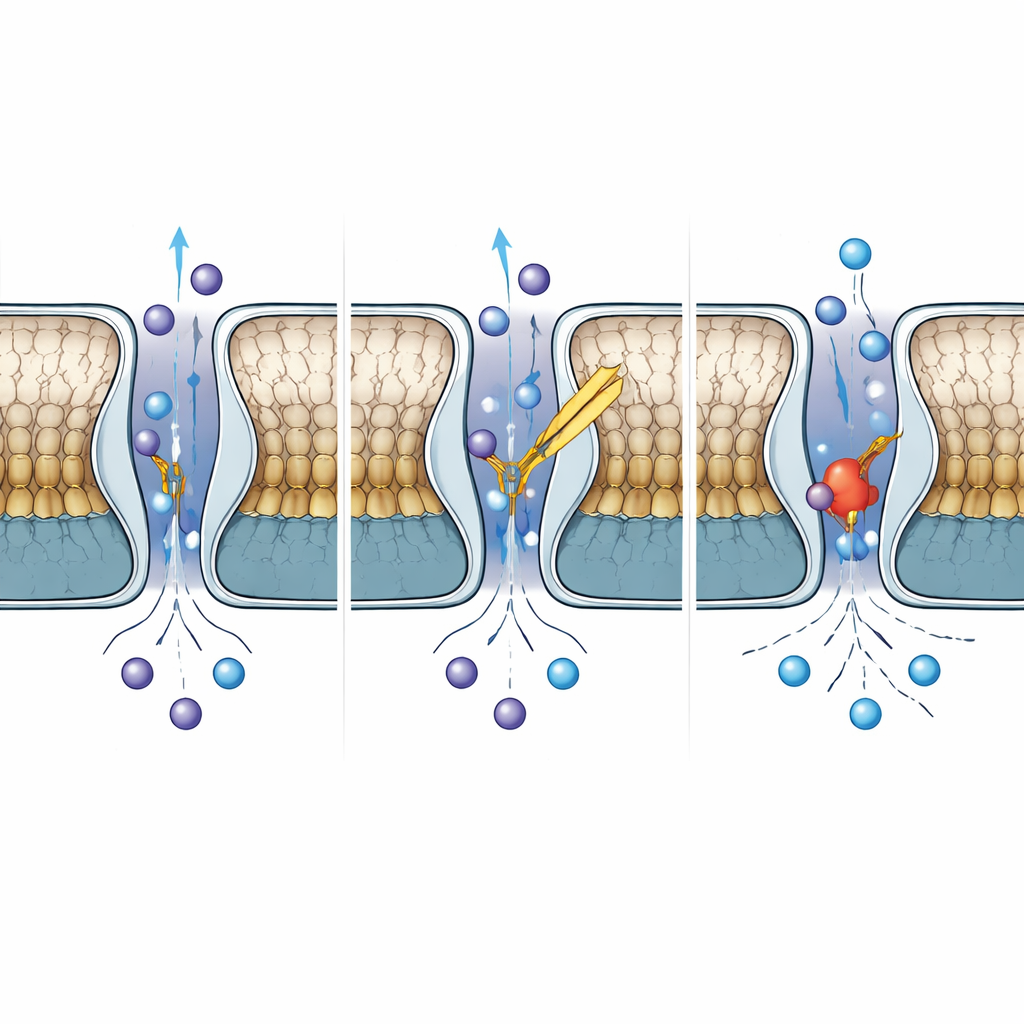
Чем TWIK-2 отличается от ближайших родственников
Хотя TWIK-2 разделяет более половины последовательности с TWIK-1, их поведение расходится по важным параметрам. Сопоставляя TWIK-2 с опубликованными структурами TWIK-1 при нейтральном и кислой pH, авторы обнаружили, что регион «крышки» TWIK-2 напоминает кислотно‑ингибированную форму TWIK-1, в то время как селективный фильтр остаётся организованным как проводящая, открытая форма. Одна гистидиновая аминокислота в TWIK-1, известная как сенсор протонов, при низком pH входит в пору и блокирует поток ионов, в TWIK-2 заменена на тирозин. Даже при обратном введении гистидина в эту позицию в TWIK-2 канал не стал pH‑чувствительным, что показывает: pH‑регуляция в этих каналах опирается на более широкую сеть остатков и движений, а не только на одну «переключающую» аминокислоту.
От структуры к будущим терапиям
В сумме эта работа даёт первое высокоразрешающее представление о человеческом TWIK-2 и показывает, как конкретные структурные особенности формируют его ионный поток, реакцию на напряжение и уязвимость к ингибиторам малой молекулы. Открытие того, что существующие соединения могут селективно ингибировать TWIK-2, в сочетании с надёжной платформой для автоматизированного скрининга, открывает путь к масштабному поиску безопасных и более эффективных лекарств. Поскольку активность TWIK-2 в иммунных клетках связана с неконтролируемым воспалением, особенно в лёгких, такие препараты могут лечь в основу новых противовоспалительных средств, действующих путём мягкого «приглушения» этого крошечного, но мощного воротного механизма в клеточной мембране.
Цитирование: Ma, Q., Hernandez, C.C., Navratna, V. et al. Insights into the structure and modulation of human TWIK-2. Nat Commun 17, 2201 (2026). https://doi.org/10.1038/s41467-026-69072-1
Ключевые слова: калиевый канал TWIK-2, каналы K2P с двумя поровыми доменами, структура ионного канала методом крио-ЭМ, модуляторы калиевых каналов, легочное воспаление