Clear Sky Science · ru
Пространственная одно-клеточная протеомика толстой кишки и мышиные модели связывают дисфункцию митохондрий с дефицитом димерного секреторного IgA-выделяющих плазматических клеток при болезни Крона
Почему антитела в кишечнике важны при болезни Крона
Болезнь Крона прежде всего известна болезненными обострениями воспаления кишечника, но задолго до появления явных симптомов в работе иммунной системы, защищающей кишку, могут происходить тонкие изменения. В этом исследовании поставлен простой, но важный вопрос: производят ли люди с болезнью Крона в ремиссии по‑прежнему нужный тип антител, который удерживает микробов в кишечнике в спокойном состоянии? Объединив образцы пациентов, высокоразрешающее профильное картирование тканей, метаболический анализ и модели на мышах, авторы выявили скрытую уязвимость в антительной защите кишечника, связанную с клеточным энергетическим обменом.
Защитное покрытие, которого не хватает
Наш кишечник полагается на особое антитело — секреторный IgA, который выделяется в слизистую оболочку. IgA, особенно в «двойной» форме — димерный IgA, покрывает бактерии и другие микробы, помогая удерживать их на поверхности, а не глубоко в ткани. В этой работе исследователи изучали биоптаты толстой кишки, кровь и стул у людей с болезнью Крона в ремиссии и у не воспалённых контролей. В ткани толстой кишки у пациентов с Крона фактически было больше В‑клеток и клеток, продуцирующих антитела, а также более высокий уровень генов и белков, связанных с IgA. Тем не менее при измерениях IgA в стуле было обнаружено противоположное тому, чего можно было ожидать: секреторный IgA в просвете кишечника был значительно снижен. 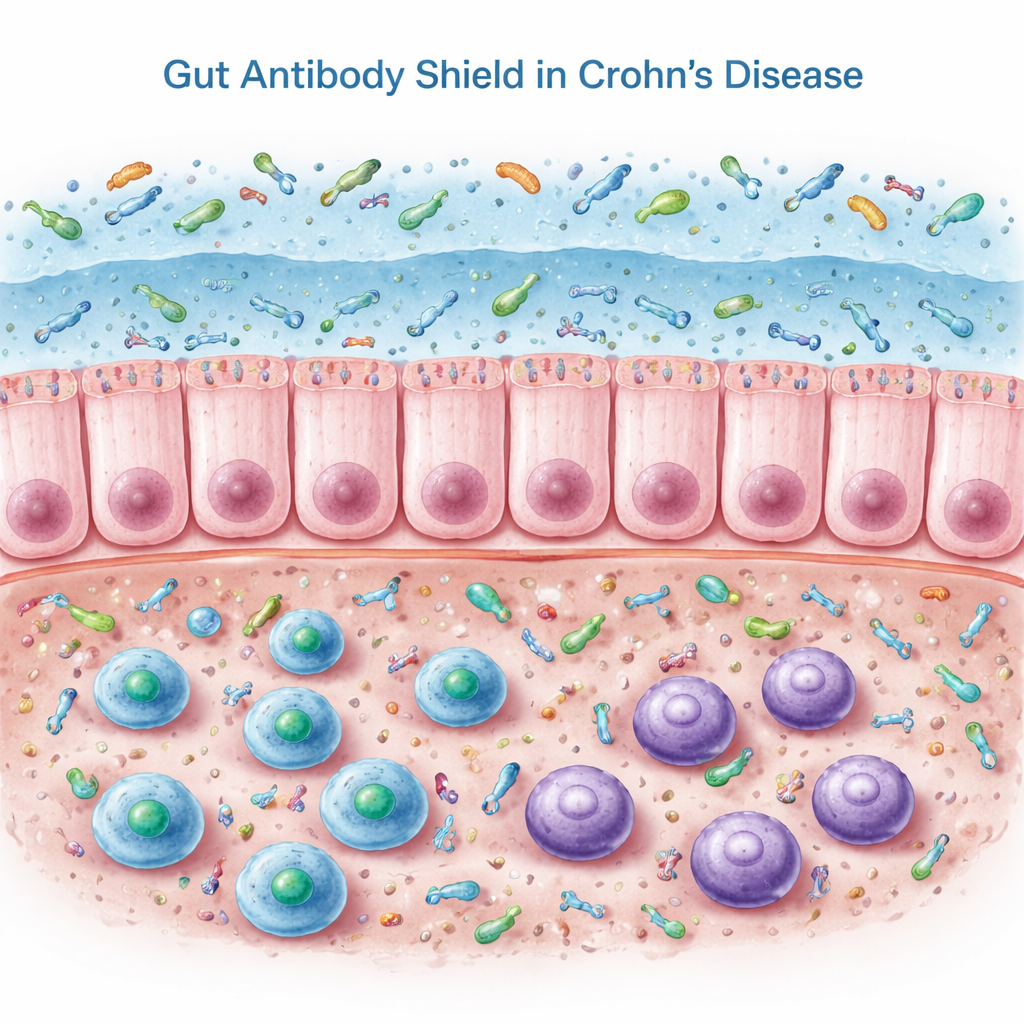
Застряли на полпути: антителопродуцирующие клетки, которые не полностью созревают
Клетки, выделяющие IgA — плазматические клетки — обычно созревают через определённые стадии: от активных короткоживущих предшественников до долгоживущих специализированных клеток, которые вырабатывают большие количества димерного IgA. С помощью пространственной одно‑клеточной протеомики, которая картирует множество белков в отдельных клетках в целой ткани, авторы смогли различить подтипы незрелых и полностью зрелых плазматических клеток в толстой кишке. У пациентов с Крона увеличивалось число ранних плазмобластов и незрелых плазматических клеток, тогда как наиболее зрелые плазматические клетки были сокращены. Биохимический анализ подтвердил, что соотношение димерного и мономерного IgA было ниже в толстой кишке при Крона, и каждая антителопродуцирующая клетка в среднем секретировала меньше димерного IgA. Когда команда выделяла переключённые В‑клетки памяти из толстой кишки и стимулировала их созревание в плазматические клетки в культуре, клетки от пациентов с Крона не смогли повысить экспрессию ключевых маркёров созревания и выработали меньше общего и димерного IgA, хотя продукция IgG оставалась в основном нормальной. Это указывает на внутренний блок в программе созревания, специфичный для IgA‑секретирующих плазматических клеток.
Энергетические фабрики под нагрузкой
Чтобы понять, что вызывает этот блок, исследователи обратились к метаболизму клеток. Они обнаружили, что плазматические клетки в тканях Крона экспрессировали более высокий уровень CD38 — фермента на поверхности клетки, который потребляет NAD+, центральный субстрат для митохондриального производства энергии. Гены, участвующие в митохондриальном окислительном фосфорилировании — основном пути образования АТФ из питательных веществ — в целом были понижены в ткани толстой кишки у пациентов с Крона, а профиль плазменных метаболитов соответствовал смещению в сторону менее эффективного митохондриального дыхания. В ex vivo экспериментах плазматические клетки, полученные от пациентов с Крона, потребляли мало глюкозы, выделяли меньше лактата и показывали снижение экспрессии генов митохондриальной энергетики, указывая на метаболически «тихое» или ослабленное состояние. 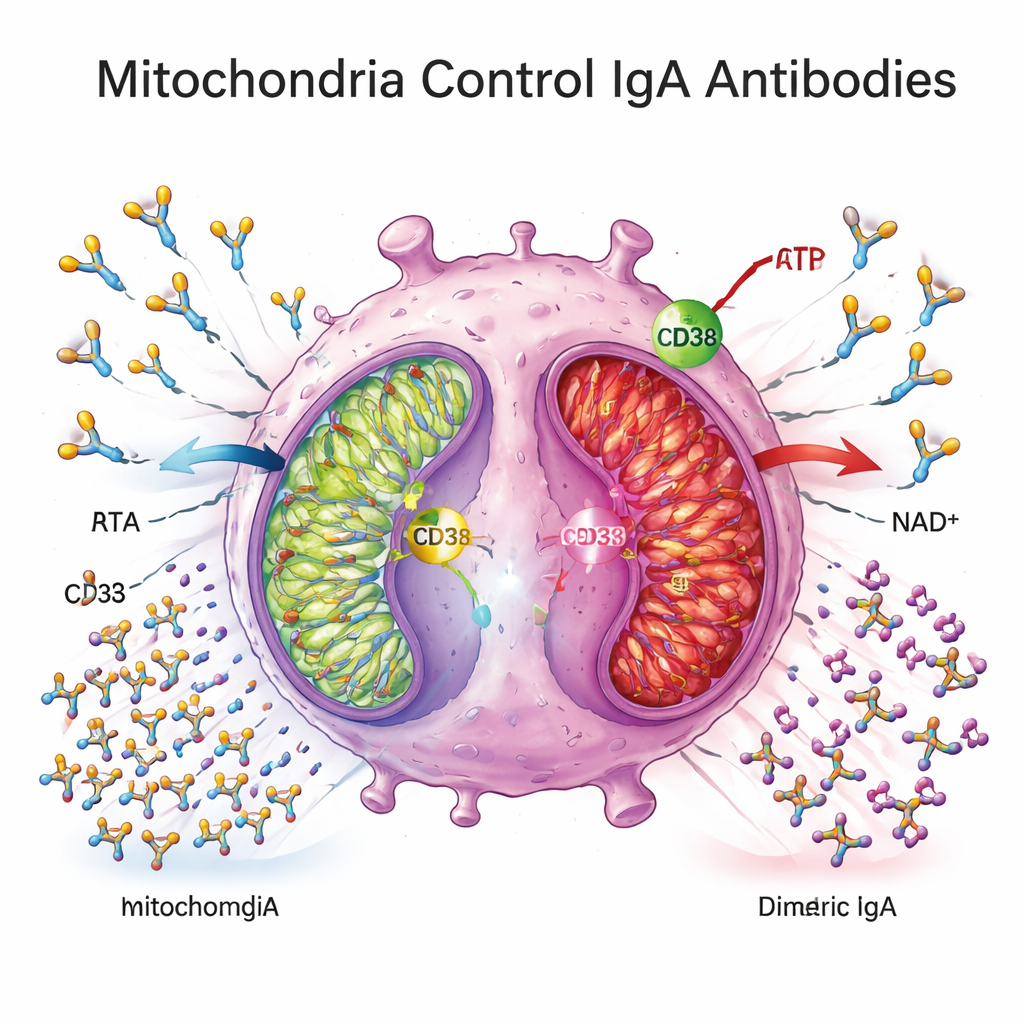
Подсказки от мышиных моделей и диеты
Мышиные модели дали дополнительную поддержку. У мышей с определённой митохондриальной мутацией, которая нарушает работу ферментного комплекса V, производящего АТФ, было меньше зрелых плазматических клеток в лимфоидных тканях, связанных с кишечником, снижена экспрессия маркёров плазматических клеток в толстой кишке и уменьшены уровни как мономерного, так и димерного IgA в ткани толстой кишки. Напротив, здоровые мыши, получавшие безглюкозную высокобелковую диету, повышающую митохондриальную активность в кишечнике, развивали больше IgA‑продуцирующих клеток и имели более высокий уровень фекального IgA. Эти комплементарные эксперименты напрямую связывают работу митохондрий со способностью плазматических клеток созревать и поддерживать прочный барьер IgA в кишечнике.
Что это значит для людей с болезнью Крона
В совокупности исследование рисует картину, в которой болезнь Крона, даже во время клинической ремиссии, связана с избытком незрелых клеток В‑линии в толстой кишке и дефицитом полностью зрелых, требовательных к энергии плазматических клеток, которые секретируют димерный IgA в слизь. Кишечник может казаться спокойным, но его антительный щит тоньше и менее эффективен. Связав этот дефект с дисфункцией митохондрий — возможно, отчасти вызванной повышенной активностью CD38 — работа предполагает, что терапия, направленная на восстановление клеточного энергетического метаболизма или тонкую настройку сигнования CD38, может помочь восстановить слизистый барьер IgA. Для пациентов это открывает перспективу того, что будущие методы лечения смогут не только подавлять воспаление при его появлении, но и укреплять передовую антительную защиту кишечника, чтобы предотвращать возникновение обострений.» }
Цитирование: Raschdorf, A., de Almeida, L.N., Solbach, P. et al. Colonic spatial single-cell proteomics and murine models link mitochondrial dysfunction to dimeric IgA-secreting plasma cell deficiency in Crohn’s disease. Nat Commun 17, 1590 (2026). https://doi.org/10.1038/s41467-026-69069-w
Ключевые слова: Болезнь Крона, антигены кишечника, IgA, митохондрии, кишечный иммунитет