Clear Sky Science · ru
FLASH-MM: быстрый и масштабируемый анализ дифференциальной экспрессии на уровне одиночной клетки с использованием линейных моделей со смешанными эффектами
Почему крошечным клеткам нужна большая вычислительная помощь
Современная биология теперь может считывать активность тысяч генов в сотнях тысяч отдельных клеток одновременно. Такой взгляд на одиночные клетки обещает более чёткое понимание того, как наши тела борются с инфекциями, чем отличаются мужчины и женщины или как развивается заболевание. Но превращение этих огромных, шумных наборов данных в надёжные открытия идёт мучительно медленно и, при наивном подходе, может вводить в заблуждение. В этой статье представлена FLASH-MM — новый способ обработки данных одиночных клеток, который сохраняет корректность статистики и при этом делает вычисления достаточно быстрыми для крупнейших современных исследований.
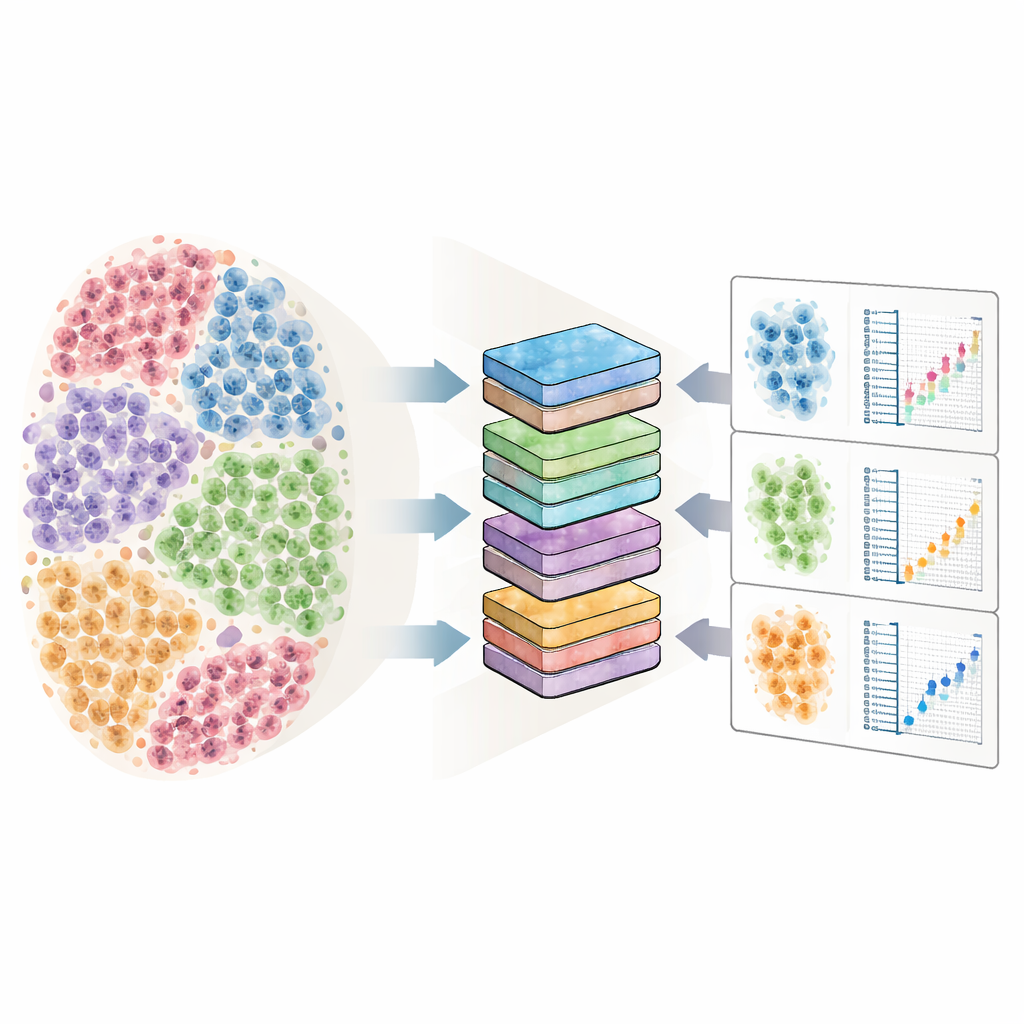
Задача: шумные и переполненные данные по клеткам
Секвенирование РНК одиночных клеток измеряет, какие гены «включены» или «выключены» в каждой клетке, в выборках от многих людей и при разных условиях. Клетки от одного и того же человека обычно похожи друг на друга, поскольку они разделяют генетический и жизненный фон, тогда как разные люди сильно отличаются между собой. Это создаёт многоуровневую структуру данных: множество клеток внутри каждого донора и множество доноров в каждой группе, например больные versus здоровые. Если эти взаимосвязи игнорировать, стандартные методы могут ошибочно пометить тысячи генов как изменённые, просто потому что они рассматривают каждую клетку как независимую точку данных. В то же время объёмы наборов одиночных клеток взорвались и сейчас включают сотни субъектов и до миллионов клеток, что выводит традиционные статистические инструменты за пределы их возможностей по времени выполнения и по памяти.
Более умная модель для людей и клеток
Чтобы справиться с этой сложностью, статистики часто используют линейные модели со смешанными эффектами, которые явно разделяют устойчивые различия между условиями (например, статус туберкулёза или пол) и случайные различия между индивидуумами. В принципе эти модели идеальны для исследований одиночных клеток, поскольку они учитывают как сходство клеток от одного человека, так и вариацию между людьми. На практике же широко используемое программное обеспечение для таких моделей тормозит или исчерпывает память на крупных экспериментах одиночных клеток. Исследователи часто вынуждены прибегать к упрощениям, например усреднению счётчиков по всем клеткам одного типа в каждом пациенте, что теряет большую часть тонкой клеточной информации, делающей данные одиночных клеток ценными.
Как FLASH-MM ускоряет тяжёлую работу
FLASH-MM сохраняет преимущества моделей со смешанными эффектами, перестраивая способ выполнения вычислений. Вместо многократного прохода по гигантским таблицам клетка–ген, FLASH-MM сначала сводит каждый набор данных к компактному набору суммарных величин, которые отражают, как клетки соотносятся с известными характеристиками, такими как размер библиотеки, тип клетки, лечение или донор. Основной алгоритм затем работает только с этими меньшими матрицами, сокращая вычислительную нагрузку с масштабирования по числу клеток до масштабирования по гораздо меньшему числу компонентов модели. Авторы также корректируют представление вариативности модели так, чтобы стандартные статистические тесты оставались валидными, что позволяет использовать простые t- и z-статистики для оценки как основных эффектов интереса, так и добавочной ценности учёта межиндивидуальной вариации. Моделирование с реалистичными искусственными данными показывает, что результаты FLASH-MM совпадают с результатами эталонного программного обеспечения до нескольких знаков после запятой, при этом работая примерно в 50–140 раз быстрее и требуя значительно меньше памяти.
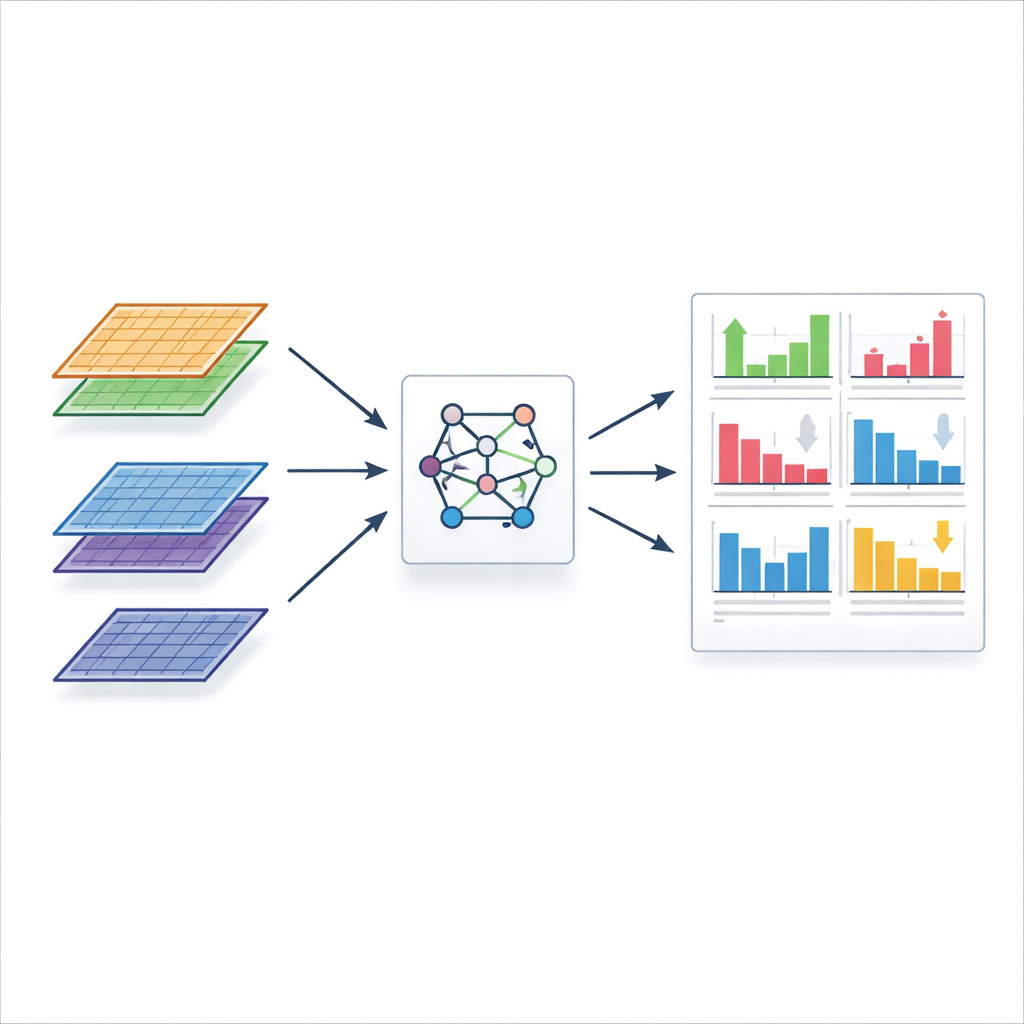
Применение метода к реальным тканям
Чтобы продемонстрировать практическое влияние, команда применила FLASH-MM к двум сложным наборам данных одиночных клеток. В карте более чем 27 000 здоровых клеток почки человека от 19 доноров FLASH-MM искал различия в активности генов между мужскими и женскими донорами внутри каждого типа клеток, учитывая каждого человека как случайный фактор, чтобы избежать излишней уверенности. Наиболее сильные сигналы, связанные с полом, были обнаружены в конкретном типе клеток почечных канальцев: у мужчин преобладали пути, связанные с регуляцией кислотности и кровяного давления, а у женщин — процессы сигнализации и переработки рецепторов. FLASH-MM выполнил этот анализ примерно за минуту, тогда как стандартный инструмент занял почти два часа. Метод также проанализировал около полумиллиона клеток памяти T от 259 человек в когорте по туберкулёзу, выявив наборы генов и путей, связанных со статусом заболевания в разных активированных состояниях T-клеток. Здесь FLASH-MM завершил работу менее чем за полтора часа, по сравнению с более чем двумя днями у традиционного подхода.
Что это означает для будущих исследований на уровне отдельных клеток
Говоря доступным языком, теперь мы можем лучше использовать поток данных одиночных клеток, не идя на компромиссы по корректности. FLASH-MM отслеживает, какие клетки принадлежат каким людям и условиям, так что обнаруженные изменения в экспрессии генов с большей вероятностью отражают подлинную биологию, а не артефакты отбора или пакетные эффекты. В то же время его экономные вычисления делают возможным анализ сотен тысяч клеток на обычных компьютерах, что открывает дорогу к более масштабным исследованиям тонких сигналов заболеваний, различий по полу и редких клеточных состояний. Поскольку подход универсален и доступен в R и Python, его можно расширять на новые технологии, такие как пространственное картирование генов и многослойные молекулярные измерения, помогая исследователям превращать огромные наборы клеточных данных в надёжные клинически значимые выводы.
Цитирование: Xu, C., Pouyabahar, D., Voisin, V. et al. FLASH-MM: fast and scalable single-cell differential expression analysis using linear mixed-effects models. Nat Commun 17, 2384 (2026). https://doi.org/10.1038/s41467-026-69063-2
Ключевые слова: секвенирование РНК одиночных клеток, дифференциальная экспрессия, линейные модели со смешанными эффектами, статистическая геномика, вычислительная биология