Clear Sky Science · ru
Tenascin C+ миофибробласты усугубляют неоинтимальную гиперплазию сосудов посредством распространения взаимодействий нервов и макрофагов у мышей
Когда сосуды заживают неверно
Процедуры, восстанавливающие проходимость закупоренных артерий, такие как ангиопластика и шунтирование, спасают множество жизней. Тем не менее у них часто остаётся скрытая проблема: со временем обработанный сосуд может рубцеваться внутрь, снова сужаясь и возвращая пациента в зону риска. Это исследование на мышах выявляет неожиданное трёхстороннее общение между клетками-опорниками, нервами и иммунными клетками в стенке сосуда, которое приводит к этому вредному «переоздоровлению», и указывает на молекулу tenascin C как перспективную мишень для разрыва этого порочного круга.
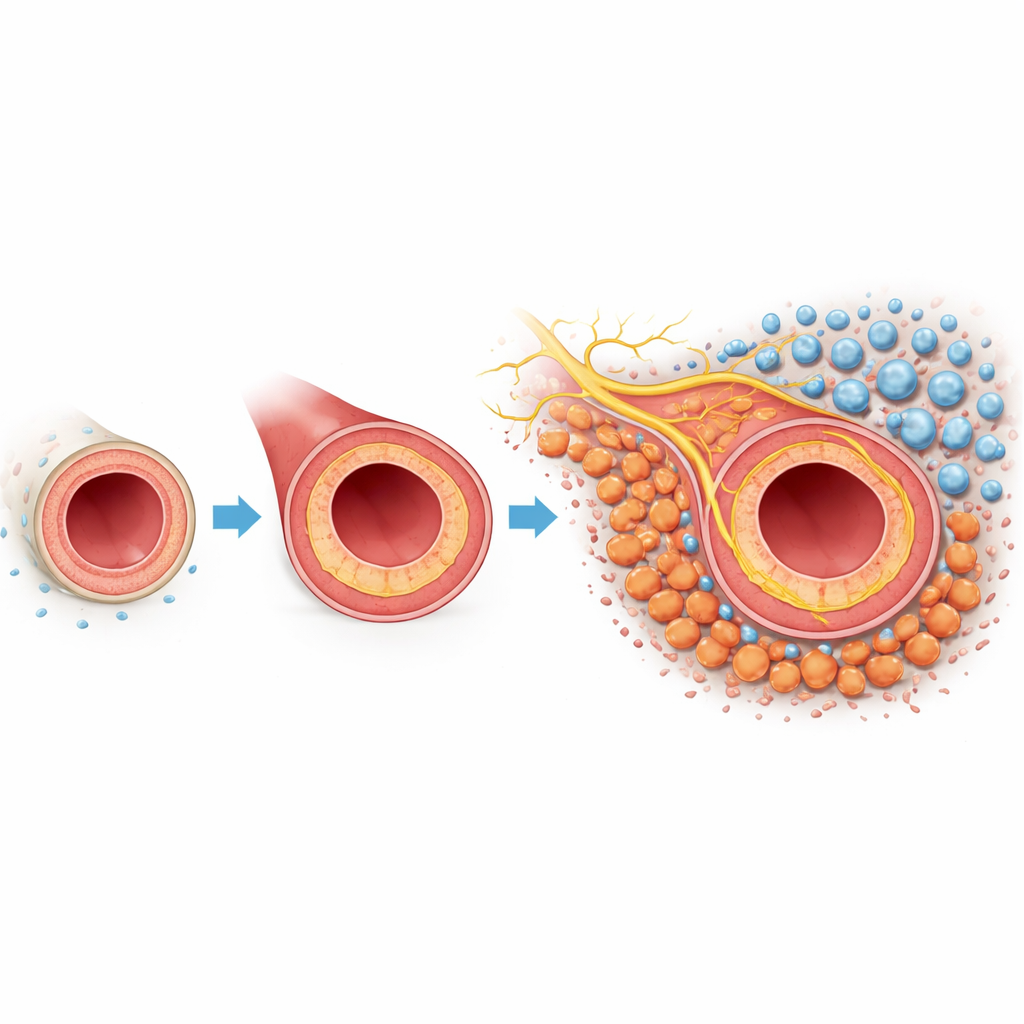
Взгляд поближе на проблемное образование рубца в артериях
Когда артерия повреждается или подвергается манипуляции во время операции, внутренний слой может регенерировать слишком агрессивно. Этот внутренний рост, называемый неоинтимальной гиперплазией, утолщает стенку сосуда и сужает просвет, по которому течёт кровь. Внешний слой сосуда, адвентиция, содержит фибробласты — клетки поддержки, которые обычно поддерживают структуру сосуда. В этой модели у мышей, где общую сонную артерию частично пережимали, имитируя повреждение, исследователи использовали одноклеточное генетическое профилирование и пространственное картирование, чтобы каталогизировать все основные типы клеток, вовлечённые в процесс. Они обнаружили, что фибробласты особенно многочисленны и значительно меняют своё поведение после повреждения, что указывает на то, что эти клетки могут играть центральную роль в ответе на образование рубца.
Появление клеток, формирующих рубец с tenascin C
Углубляясь в популяцию фибробластов, команда обнаружила отдельный подтип, который появлялся только после повреждения. Эти клетки несли признаки миофибробластов — высокий уровень контрактильного белка α-гладкомышечного актина и ещё один маркер, называемый периостином — что свидетельствует о переключении их в режим образования рубца. Существенно, этот подтип также продуцировал большие количества tenascin C, матриксного белка, обычно редкого в здоровых взрослых тканях, но обильного при заболеваниях и при репарации тканей. Лабораторные эксперименты показали, что экспозиция нормальных адвентициальных фибробластов к трансформирующему фактору роста бета или к дополнительному tenascin C подталкивала их к превращению в эти tenascin C–позитивные миофибробласты. Клетки затем секретировали ещё больше tenascin C, создавая самоподдерживающуюся петлю через специфическую пару поверхностных рецепторов, интегрин αvβ1, что постепенно расширяло популяцию формирующих рубец клеток.
Нервы и иммунные клетки заселяют окрестности
История не закончилась на образовании рубца. С помощью 3D‑склейки целых образцов и пространственной транскриптомики исследователи наблюдали, что миофибробласты, богатые tenascin C, образовывали кластеры вблизи прорастающих нервных волокон и иммунных клеток — макрофагов — во внешней стенке сосуда. Повреждённые артерии демонстрировали плотные, запутанные сенсорные нервы и больше синапсоподобных структур, чем в норме, как у мышей, так и в образцах человеческих артерий с неоинтимальной гиперплазией. Макрофаги в этих районах имели воспалительный профиль, производя молекулы, такие как IL‑1β и TGF‑β1, которые могут дополнительно подпитывать рубцевание. В целом данные нарисовали картину реорганизованного микроокружения, в котором клетки, формирующие рубец, нервы и макрофаги физически переплетаются и влияют друг на друга.
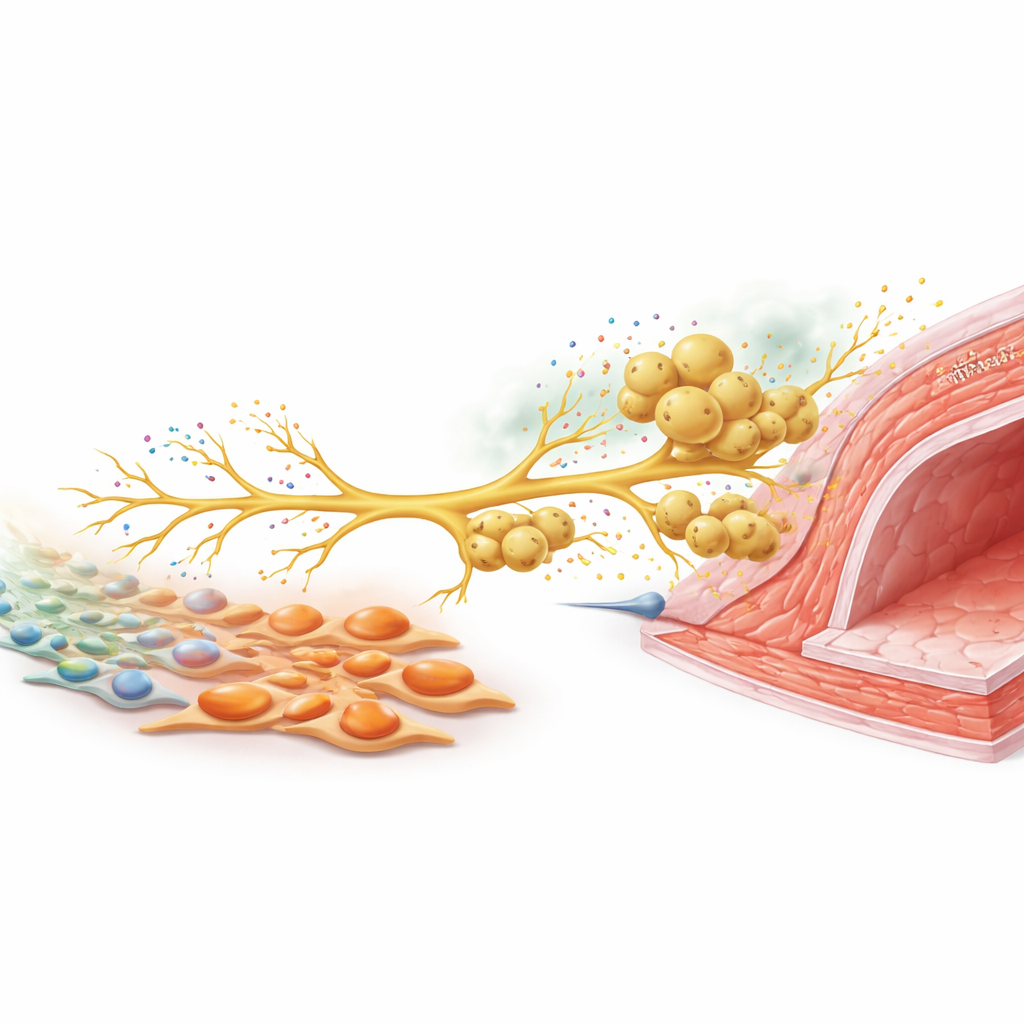
Нервный сигнал, зовущий дополнительных защитников
Чтобы понять, как эти типы клеток общаются, команда сосредоточилась на сенсорных нервах, воспринимающих повреждающие стимулы. В культуре миофибробласты, богатые tenascin C, стимулировали рост нервных волокон из нейронов дорсальных корешковых ганглиев. У повреждённых мышей эти сенсорные нейроны усиливали продукцию CCL2 — химического сигнала, хорошо известного своей способностью привлекать макрофаги. Когда нейроны и макрофаги выращивали вместе, макрофаги мигрировали вдоль растущих нервных волокон, подобно тому, как они располагались вокруг артерий in vivo. Подавление CCL2 в нейронах резко уменьшало привлечение макрофагов. У животных снижение активности сенсорных нервов с помощью токсина или селективное удаление tenascin C только в фибробластах оба приводили к снижению плотности нервов, уровней CCL2, накопления макрофагов и, в конечном счёте, утолщения стенки сосуда. Комбинирование обоих вмешательств не давало дополнительной пользы, что указывает на их действие в рамках одного пути.
Почему этот новый путь важен
В совокупности результаты раскрывают порочный круг: повреждение побуждает фибробласты превращаться в tenascin C–производящие миофибробласты; эти клетки меняют матрикс и стимулируют сенсорные нервы; активированные нервы выделяют CCL2, который привлекает макрофагов; а макрофаги секретируют воспалительные и фибротические факторы, усугубляющие рубцевание и сужение артерии. Выявив tenascin C и его нисходящую ось нерв–макрофаг как ключевые драйверы этого цикла, работа предполагает, что терапевтическое вмешательство, нацеленное на эту молекулу или её сигнальные партнёры, может помочь дольше сохранять проходимость реконструированных артерий, обеспечивая пациентам более устойчивую защиту после сердечно‑сосудистых процедур.
Цитирование: Tong, X., Shi, G., Fang, Z. et al. Tenascin C+ myofibroblasts exacerbate vascular neointimal hyperplasia by propagation of nerve-macrophage interactions in mice. Nat Commun 17, 2199 (2026). https://doi.org/10.1038/s41467-026-69062-3
Ключевые слова: неоинтимальная гиперплазия, tenascin C, ремоделирование сосудов, сенсорные нервы, воспаление макрофагов