Clear Sky Science · ru
Паклитаксел стимулирует расширение популяции макрофагов TREM2+, что объясняет его худшую терапевтическую эффективность по сравнению с наб‑паклитакселом
Почему это исследование важно
Многие женщины с раком молочной железы получают химиотерапию препаратами из группы таксанов, чаще всего паклитакселом или его новой версией, связанной с наночастицами альбумина — так называемым наб‑паклитакселом. Врачи давно подозревали, что новый препарат часто действует лучше, но причины этого были неясны. В этом исследовании на данных пациентов и на экспериментах на животных показано, что стандартный паклитаксел может непреднамеренно способствовать распространению рака в лёгкие, перестраивая иммунные клетки организма, и указаны пути блокирования этого вредного побочного эффекта.
Два похожих препарата — два разных результата
Авторы сначала сравнили реальную эффективность паклитаксела и наб‑паклитаксела у тысяч женщин с раком молочной железы. Объединив результаты 17 клинических исследований с участием 6486 пациентов, они обнаружили, что наб‑паклитаксел обеспечивает более высокие показатели сокращения опухоли и чаще приводит к полной регрессии рака в груди и прилежащих лимфатических узлах до операции. Это преимущество было особенно выражено у пациенток, получавших лечение после неудачи предыдущих терапий. При этом оба препарата применялись в сопоставимых дозах и направлены на делящиеся раковые клетки сходными механизмами, что говорит о том, что различие скорее связано не с прямым уничтожением опухоли, а с чем‑то другим.
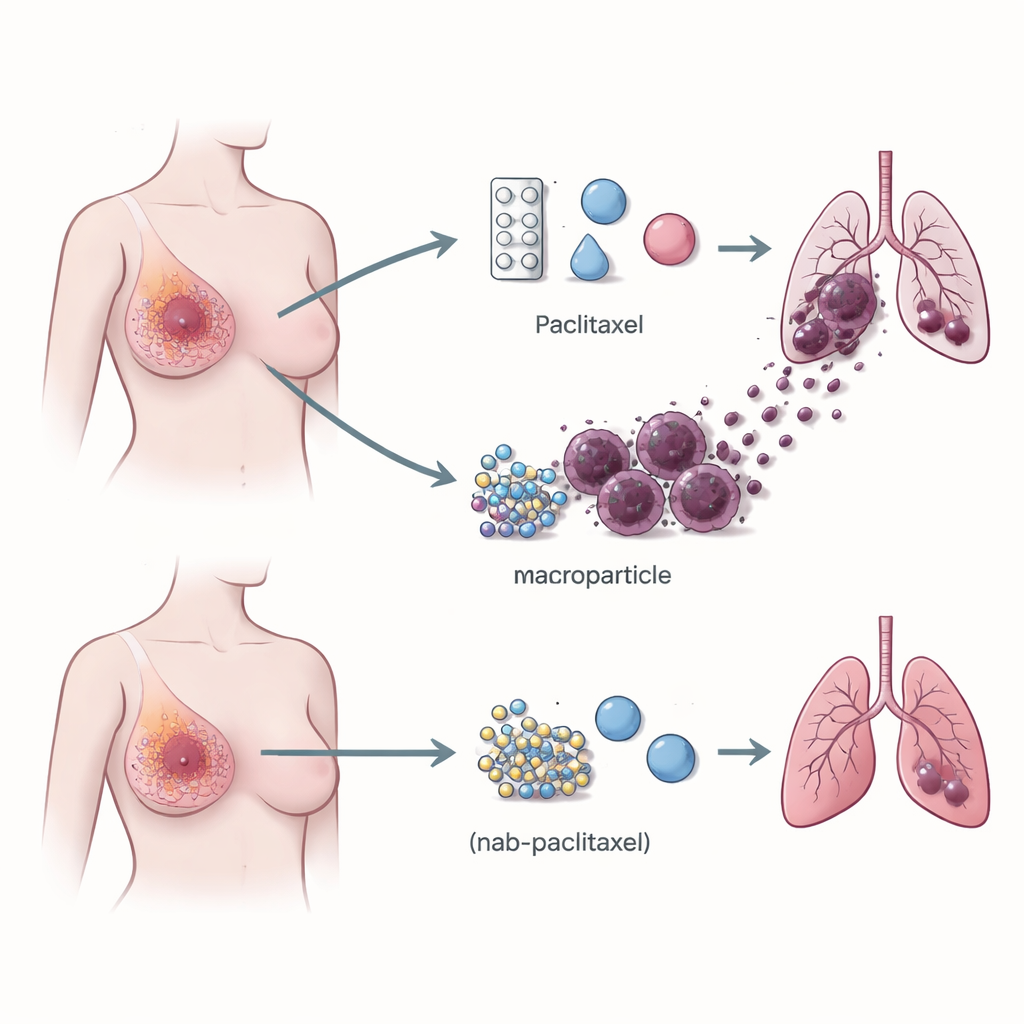
Иммунные клетки, которые помогают раку распространяться
Внимание переключилось на иммунную среду опухоли — набор лейкоцитов, которые могут либо бороться с раком, либо, как это часто бывает, способствовать его росту. С помощью одноклеточного РНК‑секвенирования, которое считывает активность генов в тысячах отдельных клеток, команда сравнила опухоли пациентов, лечившихся паклитакселом и наб‑паклитакселом. Они обнаружили, что в опухолях, обработанных паклитакселом, значительно больше макрофагов, несущих на поверхности рецептор TREM2. Эти TREM2‑позитивные макрофаги были сосредоточены на краях опухоли и встречались намного чаще у пациентов, у которых впоследствии развились метастазы в лёгких, чем у тех, чья болезнь оставалась локализованной. Шаблон подтвердился в больших когортах пациентов и на моделях мышей, что установило прочную связь между этим типом макрофагов и риском метастазирования.
Когда лечение уменьшает опухоль, но стимулирует распространение
У мышей с опухолями молочной железы паклитаксел выполнял свою задачу: он замедлял рост или сокращал первичные опухоли. Но одновременно он увеличивал количество опухолевых очагов в лёгких и повышал число TREM2‑позитивных макрофагов в опухолях и в крови. Наб‑паклитаксел, напротив, уменьшал размер опухоли, не провоцируя метастазирование в лёгкие и не расширяя популяцию этих макрофагов, хотя был столь же эффективен в сокращении основного очага. При удалении гена TREM2 у мышей или при снижении его экспрессии с помощью антисэнсовых олигонуклеотидов (коротких фрагментов ДНК, подавляющих конкретные гены) паклитаксел по‑прежнему уменьшал первичные опухоли, но в значительной степени терял способность стимулировать распространение в лёгкие. Это показывает, что макрофаги, несущие TREM2, — не просто наблюдатели, а необходимые участники метастазирования, запускаемого паклитакселом.
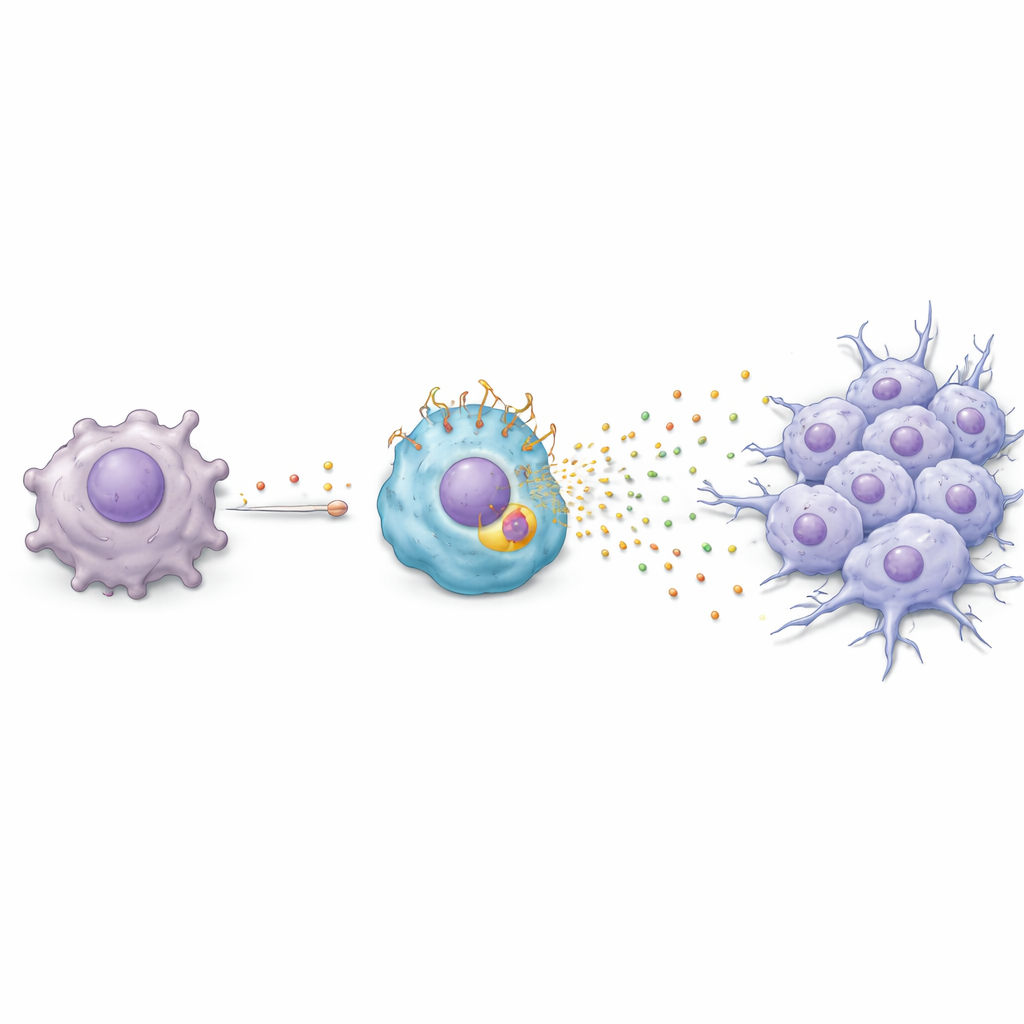
Химическая цепная реакция от опухоли к иммунной клетке
Далее исследователи выясняли, как паклитаксел переводит макрофаги в этот вредоносный TREM2‑обогащённый состояние. Они обнаружили цепочку событий: паклитаксел заставляет раковые клетки активировать ген ответа на стресс ATF3, что в свою очередь повышает продукцию фактора роста FGF2. Раковые клетки выделяют FGF2 в микроокружение, где он действует на соседние макрофаги. В этих макрофагах FGF2 активирует другой регулятор, EGR1, который повышает уровень TREM2. Как только TREM2 повышен, макрофаги начинают выделять набор белков — включая Serpin E1, HGF, CCL3 и CXCL2 — которые переводят раковые клетки в более подвижную, инвазивную форму, известную как эпителиально‑мезенхимальный переход. В лабораторных условиях и на моделях мышей эта химическая «переписка» делала клетки опухоли более склонными к миграции и инвазии — ключевым шагам на пути к метастазированию.
Как превратить меч с двусторонним лезвием в более безопасный инструмент
Из непрофессиональной перспективы ключевая мысль такова: паклитаксел может действовать как меч с двусторонним лезвием — он атакует опухоли, но одновременно инструктирует определённые иммунные клетки помогать раку уходить в отдалённые органы. Наб‑паклитаксел, по-видимому, избегает запуска этого конкретного иммунного сбоя. Обнадеживающая новость в том, что блокирование TREM2 или отдельных звеньев сигнального пути FGF2–EGR1–TREM2 позволяет в животных моделях разделить противоопухолевые эффекты паклитаксела и его способность способствовать метастазам. Если подобные стратегии окажутся безопасными и эффективными у людей, врачи смогут продолжать использовать знакомый и широко доступный химиопрепарат, одновременно снижая его склонность способствовать распространению рака, что приведёт к лучшим долгосрочным результатам для пациентов.
Цитирование: Xing, Y., Zhong, R., Li, Q. et al. Paclitaxel drives TREM2+ macrophage expansion underlying its inferior therapeutic efficacy compared to Nab-paclitaxel. Nat Commun 17, 2272 (2026). https://doi.org/10.1038/s41467-026-69060-5
Ключевые слова: рак молочной железы, паклитаксел, микроокружение опухоли, макрофаги, метастазирование