Clear Sky Science · ru
Надёжное перепрофилирование антительного интеркома внутри клетки
Превращение антител в крошечные инструменты внутри наших клеток
Антитела известны как точные «орудия» в кровотоке, нацеливающиеся на вирусы и другие угрозы. Но основная активность при многих заболеваниях, включая болезнь Альцгеймера, Паркинсона и некоторые виды рака, происходит внутри клеток, куда обычные антитела редко попадают или работают эффективно. В этом исследовании показано, как системно перестраивать существующие антитела в небольшие «интрабоди», которые надёжно функционируют внутри живых человеческих клеток, открывая путь к новым диагностическим средствам, инструментам для исследований и, возможно, будущим терапиям, действующим непосредственно в очагах болезненных процессов.
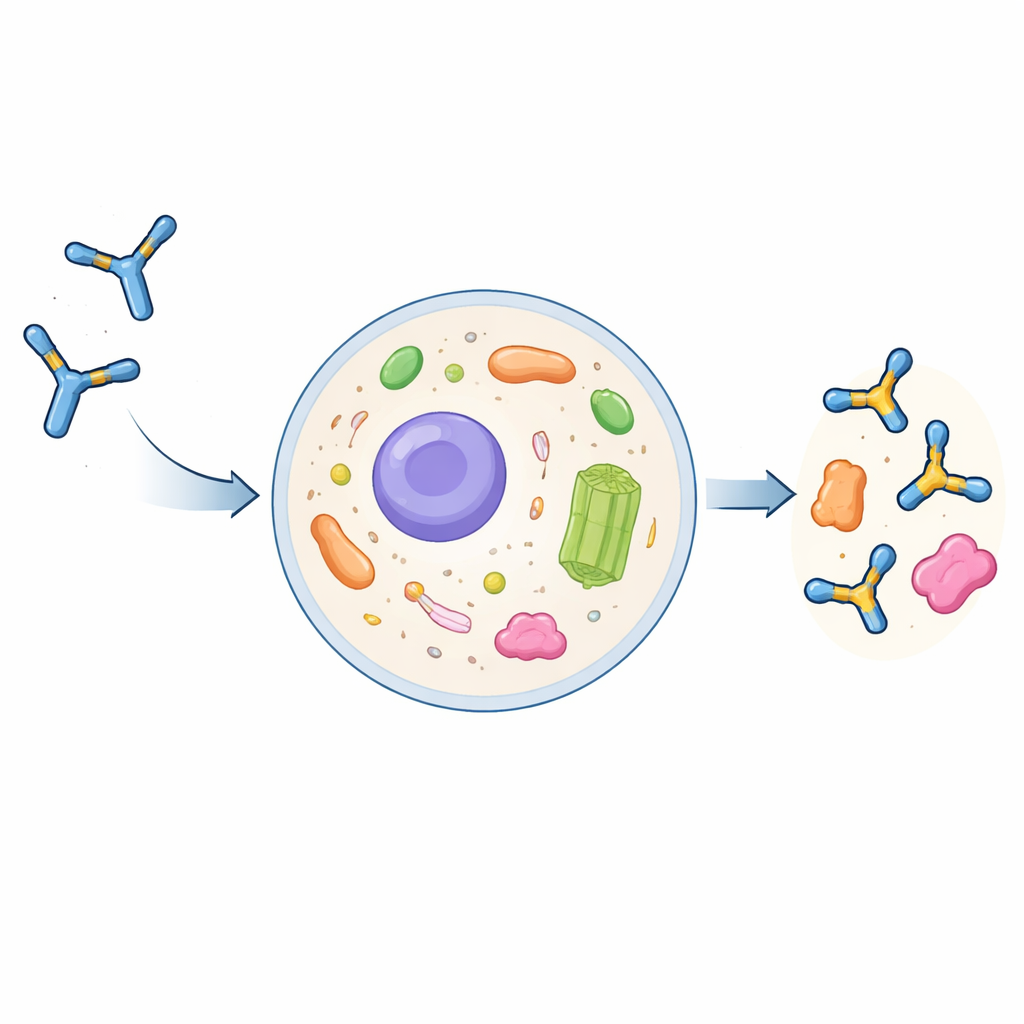
Почему обычные антитела плохо работают внутри клетки
Полноразмерные антитела — крупные Y‑образные белки, эволюционировавшие для работы вне клетки. Они собираются и химически модифицируются в секреторном пути клетки и затем попадают в кровь. Если клетки повторно захватывают антитела, те обычно попадают в компартменты для деградации, а не в жидкую внутреннюю среду клетки — цитоплазму. Учёные могут укоротить антитела до их ключевых распознающих частей, называемых одноцепочечными вариабельными фрагментами (scFv), и экспрессировать их как интрабоди внутри клеток. Однако такие интрабоди часто слипаютcя, становятся нерастворимыми и теряют способность связывать свои мишени. До сих пор не существовало общего и надёжного рецепта превращения обычного антитела в хорошо ведущее себя интрабоди.
Поиск правил дизайна для растворимых интрабоди
Исследователи начали с измерения того, насколько 45 различных интрабоди оставались растворимыми при производстве в человеческих клетках. Они систематически сравнили множество свойств белка — таких как общая гидрофобность, предсказанное качество структуры и свойства петель связывания — чтобы понять, какие из них лучше всего объясняют, остаётся ли интрабоди растворимым. Выделился один простой фактор: общий электрический заряд при близком к физиологическому pH. Интрабоди с сильно отрицательным суммарным зарядом значительно чаще оставались растворимыми, тогда как нейтральные или положительно заряженные варианты склонялись к агрегации. Другие сложные предикторы, включая показатели уверенности структур от AlphaFold, не коррелировали с растворимостью. Это позволило команде построить практичную модель на основе заряда, которая может оценивать, какая доля интрабоди будет находиться в растворимой фракции клеточного экстракта.
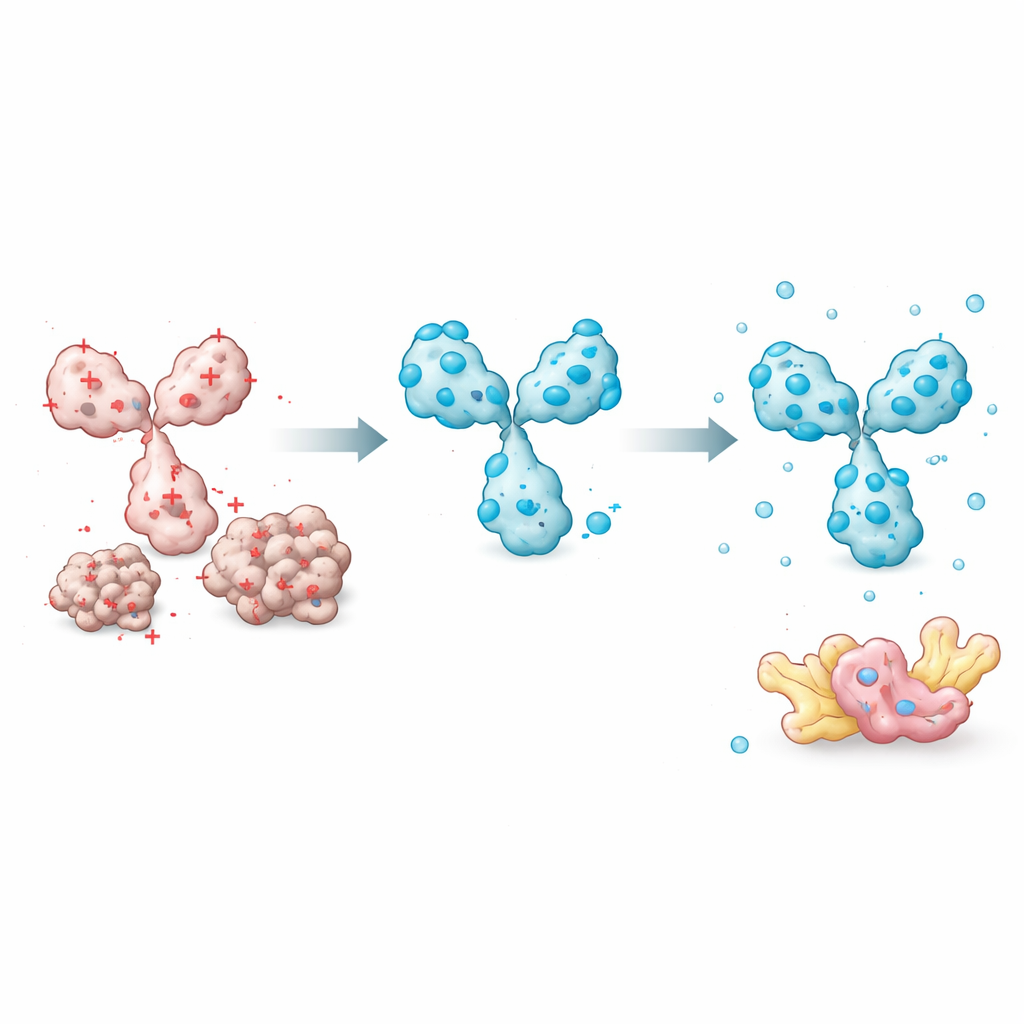
Перепроектирование линкеров и доменов для лучшего поведения
Вооружившись этим пониманием, команда сосредоточилась на характеристиках, которые можно легко изменять, не нарушая распознавания мишени интрабоди. Ключевой элемент — короткий пептидный «линкер», соединяющий два вариабельных домена. Большинство существующих конструкций используют нейтральные линкеры, не меняющие заряд. Подставляя на эти позиции аминокислоты с отрицательным зарядом, исследователи смогли понизить общий заряд интрабоди, резко улучшив растворимость при сохранении связывающей способности. Они также обнаружили, что порядок вариабельных доменов (какой домен — тяжёлый или лёгкий — идёт первым) и определённые позиции в каркасе вне петель связывания влияют на то, как белок сворачивается и остаётся растворимым. Выбор порядка доменов, который защищает более хрупкие участки, и введение тщательно подобранных мутаций с обменом зарядов дополнительно улучшали характеристики.
Использование искусственного интеллекта для масштабного создания интрабоди
Чтобы уйти от по одной проб и ошибок, авторы объединили простые правила по заряду с продвинутым ПО для проектирования белков на основе глубокого обучения. Начиная с известных остовов антител, они использовали «обратное свёртывание» (inverse folding), чтобы предложить новые последовательности, которые сохранят нужную форму, но приобретут поверхностные свойства — прежде всего схемы зарядов — благоприятствующие стабильности и растворимости. Изменения в ключевых петлях связывания ограничивали, чтобы сохранить распознавание, позволяя алгоритму перестраивать окружающие поверхности. Тесты показали, что многие из этих AI‑наведённых интрабоди были не только высоко растворимыми, но и более термостабильными, чем варианты, разработанные вручную, при этом сохраняя способность связывать белки, важные для заболеваний, такие как неправильно свернувшийся SOD1, p53, α‑синеклеин и другие белки, связанные с нейродегенерацией.
Создание библиотеки клеточных ловушек для белков
Применив эти правила и инструменты в большом масштабе, команда вычислительно переформатировала 672 антитела в интрабоди, которые, по предсказанию, будут хорошо работать внутри клеток. Эти спроектированные молекулы охватывают более 60 различных внутриклеточных мишеней, включая белки, вовлечённые в болезни Альцгеймера, Паркинсона и Хантингтона, а также факторы, связанные с раком, и посттрансляционные модификации, такие как фосфорилирование и ацетилирование. В экспериментах выбранные интрабоди успешно извлекали специфические формы белков, связанные с болезнью, например мутантный SOD1 или определённые конформации α‑синеклеина, игнорируя нормальные версии. Все последовательности опубликованы открыто, и авторы предоставляют веб‑инструмент, который позволяет другим оценивать растворимость интрабоди по последовательности с использованием той же модели на основе заряда.
Что это значит для будущих лекарств и исследований
Практически это исследование превращает огромную существующую коллекцию антител — многие из которых уже изучались в клинике — в набор инструментов, который можно надёжно адаптировать для использования внутри клеток. Следуя простому набору правил дизайна, исследователи теперь могут создавать интрабоди, которые, вероятно, будут работать с первой попытки, экономя время и средства. Для непрофессионала ключевая мысль такова: учёные нашли простой способ «перепрограммировать» наши лучшие белковые детекторы так, чтобы они функционировали в густой внутренней среде живых клеток, где начинаются многие болезни. Это может ускорить разработку новых методов отслеживания, изучения и в конечном счёте лечения состояний, вызванных неправильно свернувшимися или нарушенно работающими белками.
Цитирование: O’Shea, C.M., Shahzad, R., Aghasoleimani, K. et al. Reliable repurposing of the antibody interactome inside the cell. Nat Commun 17, 2222 (2026). https://doi.org/10.1038/s41467-026-69057-0
Ключевые слова: интрабоди, инжиниринг антител, растворимость белков, нейродегенеративные заболевания, искусственный интеллект в биологии