Clear Sky Science · ru
Регулирование межфазной воды для переноса кислорода на бензильные C(sp3)–H связи через Ni-активированную вольфрам–кислородную ковалентность
Превращение воды и масла в полезные химикаты
Химики давно ищут более чистые способы превращения простых нефтяных молекул в более ценные компоненты для пластмасс, лекарств и повседневных продуктов. В этом исследовании показано, как тщательная «настройка» тонкого слоя воды, соприкасающегося с электродом, позволяет обычной воде снабжать кислородом инертные углеводородные молекулы, сокращая при этом отходы и энергозатраты.
Почему кислород из воды важен
Многие промышленные химические вещества получают путем присоединения кислорода к углеводородам — молекулам, состоящим в основном из углерода и водорода. Сегодня это часто требует сильных окислителей и высоких температур, что потребляет много энергии и приводит к выбросам, ускоряющим изменение климата. Вода — дешёвый, безопасный и доступный источник кислорода, но заставить её напрямую отдать кислород прочным связям углерод–водород обычно можно только при очень высоких напряжениях. При таких жестких условиях большая часть электричества тратится на расщепление воды с образованием кислорода, а не на получение полезных продуктов.
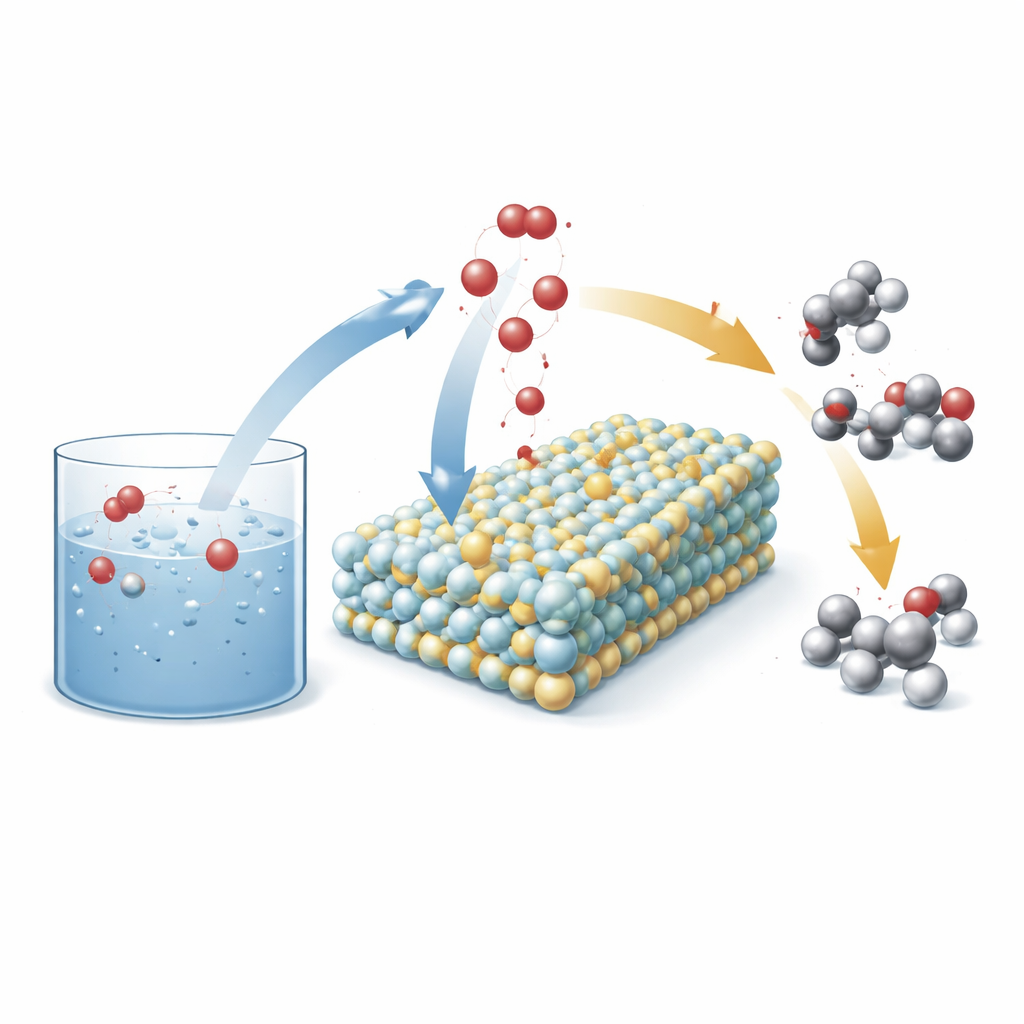
Умный электрод, который перестраивает воду
Исследователи разработали новый тип анода (положительного электрода в электрохимической ячейке), построенного из крошечных частиц карбида вольфрама, которые в процессе работы преобразуются в аморфный вольфрамо–кислородный материал. В эту матрицу вкрапляют отдельные атомы никеля. В реакционных условиях кислород из воды мигрирует в твердое тело, превращая его в поверхность вольфрамового оксида, активированную никелем, с множеством открытых реакционноспособных участков. Эта перестроенная поверхность затем служит платформой, где вода и молекулы углеводородов встречаются и обмениваются кислородом в контролируемом режиме, предпочитая ценные продукты, такие как спирты и кетоны, а не перенасыщенные кислоты и другие побочные продукты.
Ослабление водной «клетки» у поверхности
Ключевое открытие состоит в том, что атомы никеля тонко нарушают способ упаковывания молекул воды у электрода. Как правило, вода на заряженной поверхности образует плотную сеть водородных связей, подобную тугой сетке, которая замедляет движение. Компьютерные моделирования и чувствительные инфракрасные измерения показывают, что в районах, легированных никелем, эта сеть становится более рыхлой, с меньшим числом водородных связей и большим количеством «свободных» молекул воды. Это открывает каналы, через которые вода легче диффундирует к реакционноспособным вольфрамо–кислородным участкам. В результате фрагменты, несущие кислород из воды, достигают поверхности быстрее и чаще, питая реакцию вместо того, чтобы улетучиваться в виде кислорода газа.
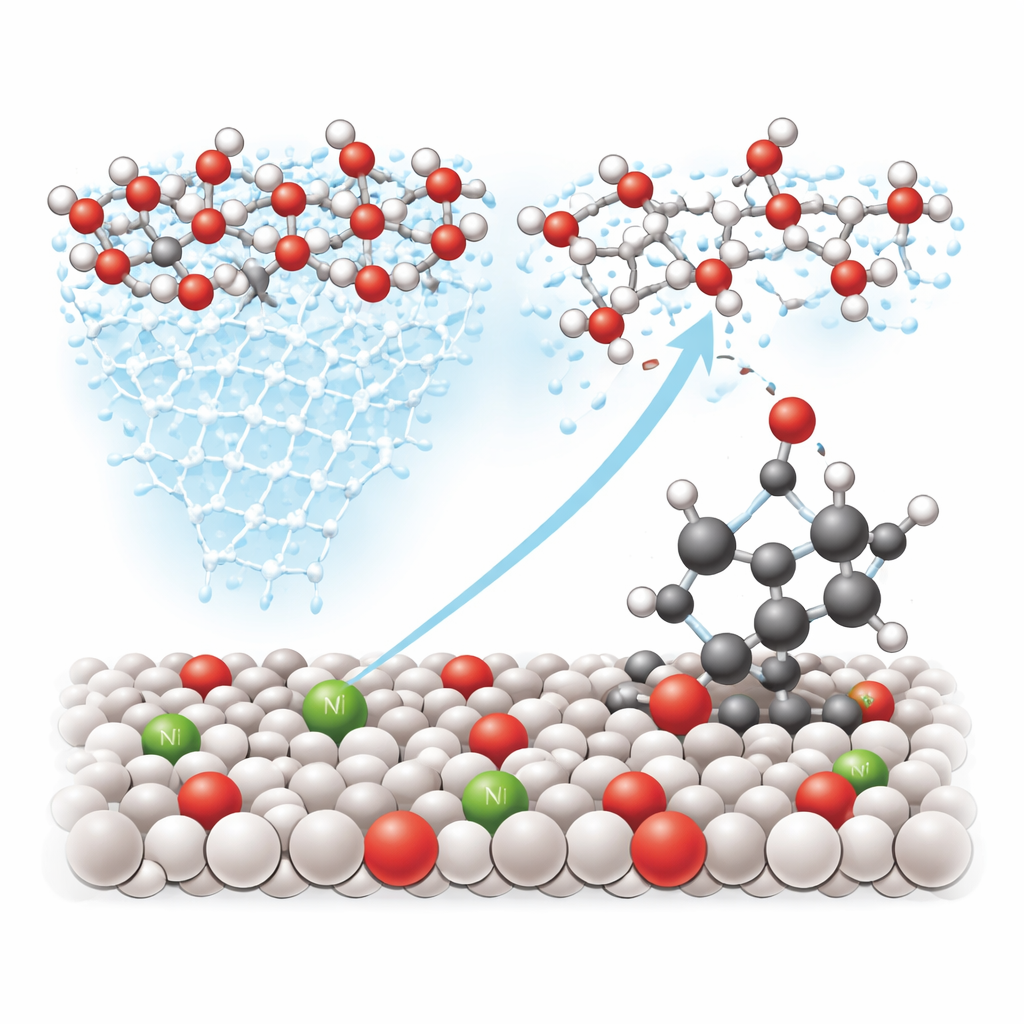
Направление кислорода к нужным связям
Помимо улучшения «трафика» у поверхности, никель также настраивает электронную структуру соседних атомов вольфрама, делая отдельные участки особенно способными захватывать и активировать воду. Эксперименты с изотопами — специальными версиями кислорода и водорода, которые можно отслеживать — показывают, что активный кислород происходит из недавно расщеплённой воды, а не из объёма самого оксида. Спектроскопические «моментальные снимки» фиксируют короткоживущий мостик между вольфрамом, кислородом и бензильным углеродом в молекулах вроде этилбензола. Теоретические расчеты подтверждают, что на никелем модифицированной поверхности атаку кислородного атома по этому углеродно–водородному участку легче осуществить, чем пойти по обычному пути расщепления воды с образованием кислорода, эффективно направляя реакцию к полезным окисленным продуктам.
Эффективно, селективно и надёжно
В испытаниях никел-активированный электрод превращает ряд бензильных связей углерод–водород в спирты и кетоны с фардадическими эффективностями — доля электрического заряда, идущая на желаемую химию — обычно выше 50%, достигая более 56% в оптимизированных случаях. Система работает в течение многих циклов без потери активности, при этом сохраняя свою никель–вольфрамовую структуру. Поскольку в качестве единственного источника кислорода используется вода и не требуются дополнительные химические окислители, она предлагает конкурентную энергетическую эффективность и более низкие материальные затраты по сравнению с другими передовыми методами. Хотя текущая область применения сосредоточена на бензильных участках, лежащий в основе принцип — использование атомарных добавок для перестройки межфазной воды и перенаправления путей реакции — указывает на более широкий набор инструментов для более экологичного, электроэнергетического окисления иначе инертных C–H связей.
Что это значит для более чистой химии
Эта работа показывает, что небольшие изменения на атомарном уровне могут иметь непропорционально большие эффекты на поведение воды у электрода и на то, куда в итоге попадает её кислород. Используя атомы никеля как для ослабления структуры межфазной воды, так и для тонкой настройки реакционных участков, авторы превращают воду в эффективного донора кислорода для трудноактивируемых углеводородных связей, одновременно подавляя нежелательное образование газообразного кислорода. В долгосрочной перспективе стратегии наподобие этой могут помочь переработать окислительную химию в промышленности, сделав её более энергоэффективной и климатически безопасной за счёт использования электричества и воды вместо жестких окислителей и реагентов, полученных из ископаемого топлива.
Цитирование: Leng, BL., Lin, X., Dong, HY. et al. Regulating interfacial water for oxygen transfer to benzylic C(sp3)–H bonds via Ni-activated tungsten-oxygen covalency. Nat Commun 17, 2355 (2026). https://doi.org/10.1038/s41467-026-69054-3
Ключевые слова: электрокатализ, окисление воды, активация бензильных C–H связей, вольфрамовый оксид, легированный никелем, зеленая химия