Clear Sky Science · ru
Двойной RNA‑Seq in vivo выявляет ключевые эффекторные молекулы, разрушающие эпителиальный барьер внеклеточным патогеном
Как некоторые микробы проскальзывают мимо наших клеточных заборов
Органы выстланы плотно сомкнутыми клетками, которые действуют как стены, удерживая кровь, микробы и токсины на своих местах. Тем не менее некоторые возбудители всё же проникают между этими клетками и распространяются по организму. В этом исследовании подробно показано, как бактерия, вызывающая лептоспироз — серьёзное заболевание с мировой распространённостью — тихо добирается до печени и почек, а затем с помощью хитрого приёма, связанного с кальцием внутри наших клеток, раздвигает эти защитные барьеры.
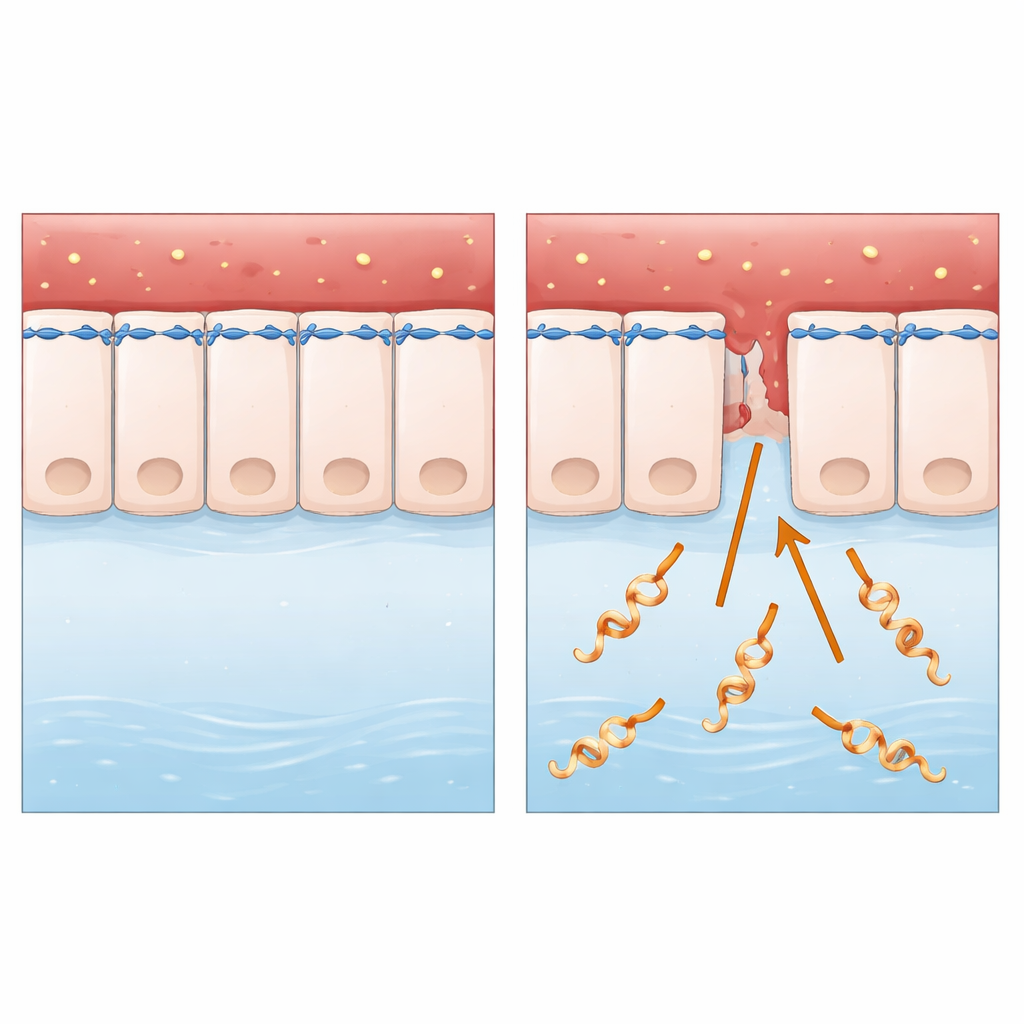
Скрытный захватчик тканей животных и человека
Исследование сосредоточено на Leptospira interrogans, спиральной бактерии, передающейся в основном от животных к человеку через загрязнённую воду или почву. Попав через мелкие повреждения кожи или слизистые оболочки, она распространяется по крови и может вызывать тяжёлые заболевания, включая отказ печени и почек и внутренние кровотечения. В отличие от многих хорошо изученных микроорганизмов, Leptospira ведёт вне‑клеточный образ жизни и лишена некоторых классических «молекулярных орудий», на которые учёные обычно ориентируются. Это сделало её идеальной моделью для простого, но важного вопроса: как казалось бы простая внеклеточная бактерия так эффективно пересекает неповреждённые слои клеток?
Наблюдая, как одновременно говорят гены хозяина и возбудителя
Чтобы запечатлеть процесс инфекции в живом животном, команда использовала двойной секвенирование РНК в хомяках — модели острого лептоспироза. Этот метод одновременно показывает, какие гены включаются или выключаются у хозяина и у патогена. Учёные инфицировали хомяков и собирали ткани печени и почек через один и три дня. На ранней стадии, несмотря на большое число бактерий, активность генов клеток животных почти не менялась, что говорит о том, что Leptospira сначала ускользает от внимания иммунной системы. Однако к третьему дню в обоих органах развилась выраженная реакция, особенно в печени: резко изменились гены, связанные с воспалением, клеточными контактами и внутриклеточным скелетом, указывая на активную перестройку тканевых барьеров.
Разрывая клеточную молнию изнутри наружу
Слои клеток герметизируются плотными и адгезионными соединениями, которые связывают соседние клетки и закрепляют их за кольцо актин‑миозин — ту же пару белков, что участвует в сокращении мышц. Микроскопия человеческих эпителиальных клеток, инфицированных Leptospira, показала изменение формы клеток, появление щелей между ними и ослабление или смещение ключевых белков контактов. Важно, что клетки не умирали, то есть барьер не разрушался насильственно, а демонтировался. Исследователи также заметили признаки стресса в фабриках сворачивания белка клетки, но блокирование этого стресса не восстановило соединения, что указывало на другого виновника.
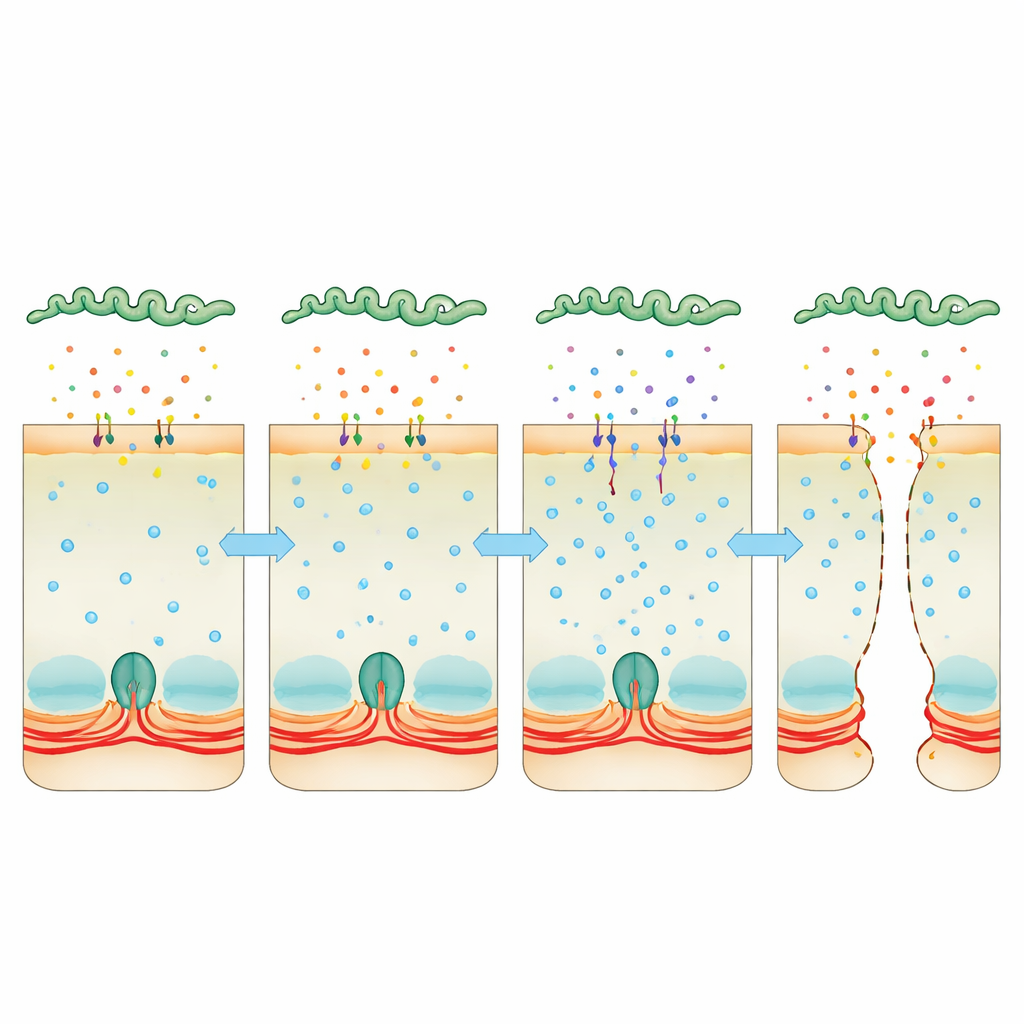
Присвоение кальция как скрытой монтировки
Внимание переключилось на кальций — универсальный внутриклеточный сигнал, который может затягивать или ослаблять актин‑миозиновое кольцо. В инфицированных клетках накопление кальция увеличилось, и это было связано с повышенной активностью киназы лёгкой цепи миозина, фермента, заставляющего сократительное кольцо натягивать контакты. Когда команда использовала соединение, связывающее кальций, или препараты, ингибирующие кальмодулин или эту киназу, слои клеток оставались более целыми и бактериям было сложнее просачиваться. Одновременно глубокое секвенирование бактериальной РНК показало, что внутри хозяина Leptospira резко усиливает производство двух «модифицирующих вирулентность» белков, напоминающих токсины. Эти белки секретируются в окружение, прикрепляются к клеткам хозяина и обнаруживаются внутри них. Когда бактерии лишались одного или обоих этих белков, они значительно теряли способность пересекать клеточные слои и вызывать летальный исход, а их секретируемая среда больше не повышала уровни кальция и не разрушала контакты так эффективно.
Что это значит для болезни и будущих защитных мер
В совокупности результаты вырисовывают ясную картину. Просочившись в тело почти незаметно, Leptospira начинает выделять белки, похожие на токсины, — модификаторы вирулентности. Эти белки связываются с эпителиальными клетками и нарушают внутриклеточный баланс кальция, что, в свою очередь, запускает сократительный путь, разрывающий «молнию» клеточных контактов, удерживающих соседние клетки вместе. По мере ослабления плотных и адгезионных соединений появляются микроскопические щели, позволяющие бактериям проходить между клетками, колонизировать органы и вызывать тяжёлое заболевание. Выявив этот зависимый от кальция механизм и бактериальные белки, которые за ним стоят, исследование прокладывает путь к новым стратегиям — например к блокированию этих белков или их сигнального пути — чтобы укрепить наши клеточные барьеры и ограничить распространение лептоспироза и, возможно, других инфекций, использующих схожие приёмы.
Цитирование: Giraud-Gatineau, A., Haustant, G., Monot, M. et al. In vivo dual RNA-Seq uncovers key effectors of epithelial barrier disruption by an extracellular pathogen. Nat Commun 17, 2274 (2026). https://doi.org/10.1038/s41467-026-69033-8
Ключевые слова: лептоспироз, эпителиальный барьер, кальциевые сигналы, бактериальные токсины, взаимодействия хозяин–патоген