Clear Sky Science · ru
Усиленный суперзаряжением nDIA‑MS позволяет глобально профилировать лекарственно-индуцированные сдвиги в растворимости протеома
Почему поведение белков важно не только с точки зрения их количества
Лекарства могут менять не только то, сколько белка синтезирует клетка, но и куда этот белок перемещается, а также находится ли он в свободном состоянии или ассоциирован с клеточными структурами. Эти сдвиги в «месте» и «форме» существования белков внутри клетки тесно связаны с такими заболеваниями, как рак и нейродегенерация, но их трудно измерить в масштабе. В этом исследовании предложен быстрый и мощный метод, позволяющий одновременно просканировать тысячи человеческих белков и оценить, как меняется их растворимость — то есть находятся ли они в свободном или в более зафиксированном состоянии — при обработке клеток двумя широко используемыми экспериментальными препаратами.
Более быстрый и точный способ изучать белки
Авторы основываются на ключевой технологии современной биологии: масс‑спектрометрии — методе, который взвешивает и считает фрагменты белков. Стандартные подходы уже прекрасно показывают, сколько каждого белка присутствует, но им сложнее выявлять изменения в состоянии белка, например переход на ДНК или в плотные сборки. В работе исследователи улучшают вариант масс‑спектрометрии, называемый узкооконной data‑independent acquisition (nDIA‑MS). Добавляя в жидкость, которая переносит пептиды через прибор, небольшие химические вспомогательные вещества — так называемые суперзаряжающие реагенты — они повышают электрические заряды этих фрагментов и значительно усиливают сигнал.
После тестирования двух распространённых суперзаряжающих добавок — диметилсульфоксида (DMSO) и m‑нитробензилового спирта (mNBA) — они обнаруживают, что 3% DMSO даёт наибольшее общее усиление сигнала и наибольшее число обнаруживаемых белков, тогда как mNBA лучше повышает количество и заряд отдельных пептидных фрагментов. С оптимизированной настройкой команда может идентифицировать около 9600 человеческих белков всего из одного микрограмма стандартного клеточного дигеста за 15‑минутный прогон — впечатляющее сочетание скорости и глубины для рутинных экспериментов. Эта производительность открывает возможность использовать nDIA‑MS не только для подсчёта белков, но и для изучения того, как их физическое состояние реагирует на стресс.
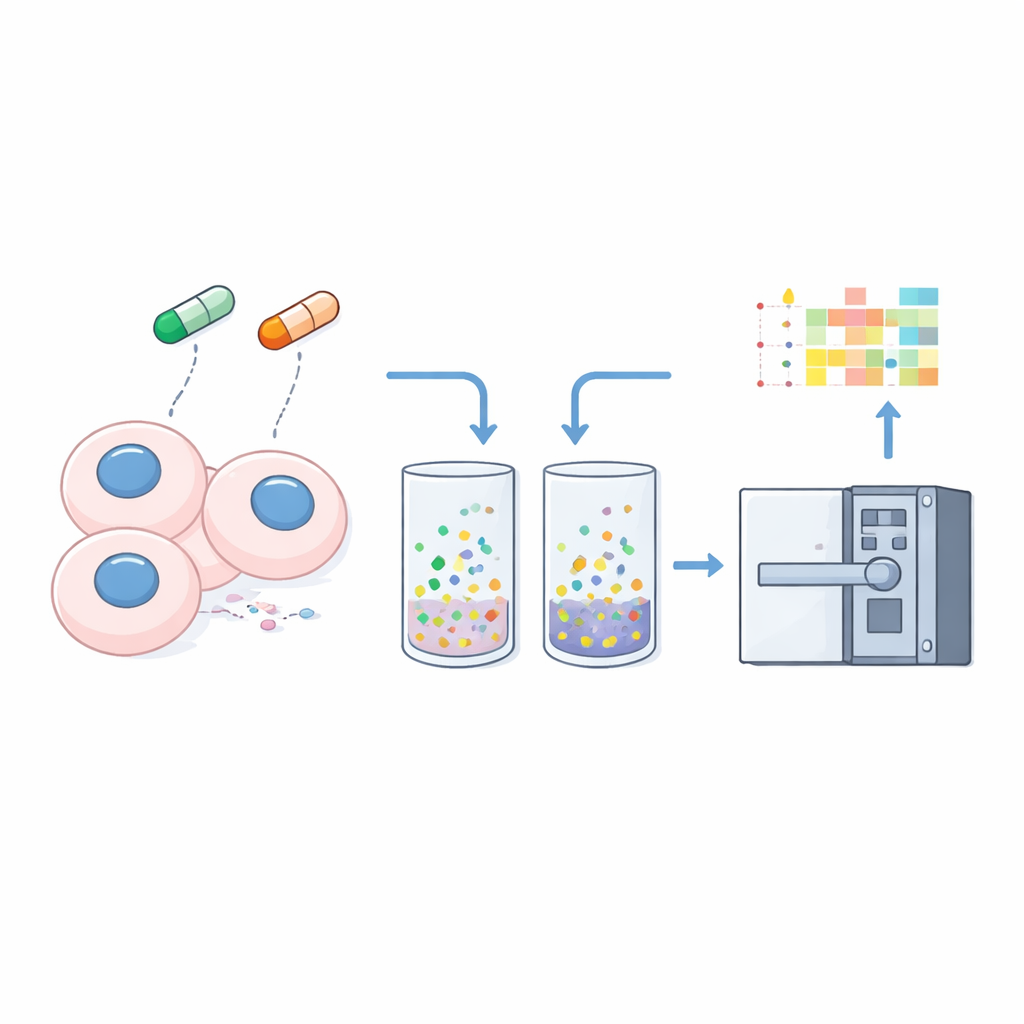
Преобразование растворимости в показатель клеточных изменений
Чтобы превратить растворимость в измеримый сигнал, исследователи мягко предварительно обрабатывают клетки щадящим детергентом, который извлекает свободно растворимые белки, оставляя материал, прочно связанный с ДНК, мембранами или другими структурами. Они анализируют и цельный клеточный лизат, и этот «нерастворимый» осадок из трёх раковых клеточных линий, используя оптимизированный метод nDIA‑MS. Сравнивая содержание каждого белка в осадке относительно цельного образца, они вычисляют простой «коэффициент нерастворимости» — более высокие значения указывают на более сильную ассоциацию с клеточными структурами, более низкие — на более растворимое, свободное состояние.
Команда затем подвергает клетки всего лишь одному часу воздействия двух препаратов: MG132, блокатора протеасомы, который предотвращает деградацию нежелательных белков, и ML‑792, ингибитора активации SUMO, вмешивающегося в ключевую систему белкового мечение. Это краткое воздействие преднамеренно: оно направлено на фиксацию быстрых, ранних сдвигов в поведении белков до того, как изменения экспрессии генов полностью развернутся. Даже за это короткое время они могут количественно оценить изменения растворимости и содержания для 8 694 белков и подтвердить, что их фракционирование чётко разделяет классические растворимые белки, такие как тубулин, и белки, связанные с хроматином, такие как гистоны.
Препараты, перестраивающие белковый ландшафт клетки
MG132 и ML‑792 вызывают широкое, но различное перестроение растворимости белков. MG132 делает более тысячи белков менее растворимыми и более шестьсот — более растворимыми в трёх клеточных линиях. Многие затронутые белки находятся на перекрёстке контроля качества белков, ответа на повреждение ДНК, регуляции генов и аутофагии — системы самочистки клетки. Например, компоненты комплекса активации протеасомы и адаптеры, помогающие маркировать дефектные белки, становятся менее растворимыми, что намекает на то, что при блокировании деградации ключевые факторы контроля качества сами оказываются захваченными на структурах, таких как хроматин или клеточные мембраны. Белки аутофагии и участники ответа на повреждение, включая регулятор стресса HSF1, также смещаются в сторону более нерастворимых, конденсатоподобных состояний, что согласуется с формированием ядерных стрессовых тел.
ML‑792, напротив, целенаправленно влияет на белки, участвующие в транскрипции и в самой системе SUMO. Сотни белков становятся либо более нерастворимыми, либо более растворимыми при блокировании активации SUMO, а основные SUMO‑белки перемещаются в растворимую фракцию, как и ожидалось. В исследовании выделяются примечательные поведения: субъединицы РНК‑полимеразы III становятся более нерастворимыми, что указывает на изменённый ядерный импорт или связывание с хроматином; ключевые репрессоры, связанные с ядерными телами, такие как SP100 и DAXX, становятся более растворимыми, что свидетельствует о том, что пометки SUMO помогают удерживать их в этих компартментах. При применении обоих препаратов по отдельности или последовательно некоторые белки, включая NAB2, SMAD2 и RB1, демонстрируют согласованные или даже противоположные сдвиги растворимости, раскрывая тонкое взаимодействие между системами убиквитин‑ и SUMO‑мечение в контроле локализации белков.
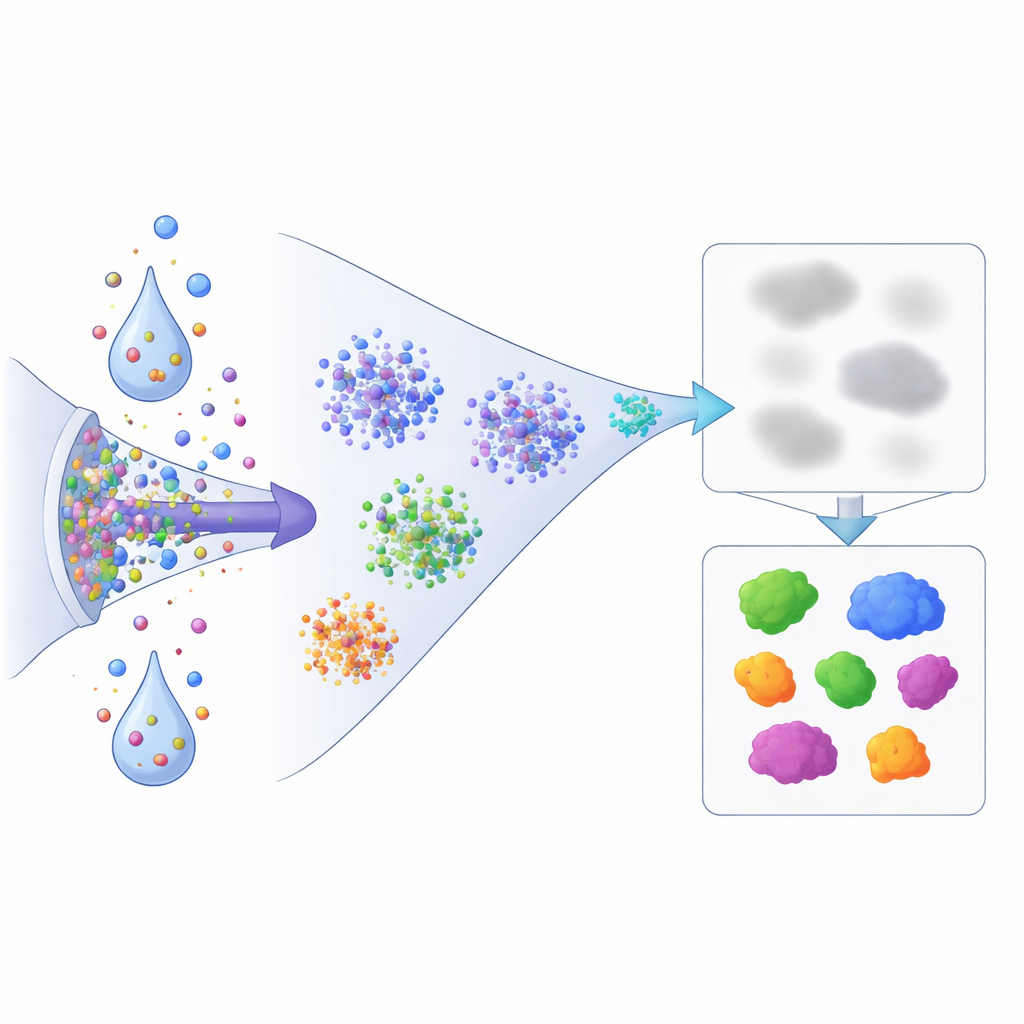
Что это означает для будущих разработок лекарств
Для неспециалистов главный вывод в том, что белки меняют не только свою количественную представленность при стрессе или воздействии препаратов; они также перемещаются, конденсируются и изменяют степень своей связи с клеточными структурами. Эта работа предоставляет быстрый, протеомный способ наблюдать за этими сдвигами. Сочетая отлаженный рабочий процесс масс‑спектрометрии с простым сравнением растворимое‑против‑нерастворимого, авторы показывают, что распространённые экспериментальные препараты быстро реорганизуют внутренний белковый ландшафт клетки так, как бы это осталось незамеченным при стандартных измерениях количества. Подход открывает путь к картированию того, как кандидат‑лекарства перестраивают состояния белков по всей клетке, помогая исследователям выявлять неожиданные мишени, стрессовые пути и точки отказа, которые могут быть критичны для понимания как терапевтического действия, так и побочных эффектов.
Цитирование: Xiong, Y., Zhang, H., Tan, L. et al. Supercharging-enhanced nDIA-MS enables global profiling of drug-induced proteome solubility shifts. Nat Commun 17, 2350 (2026). https://doi.org/10.1038/s41467-026-69025-8
Ключевые слова: растворимость протеома, масс-спектрометрия, ингибитор протеасомы MG132, ингибитор сумоилирования ML-792, переходы состояний белков