Clear Sky Science · ru
Инженерная внутренняя архитектура коро́бочно-оболочечных липидных наночастиц способствует эффективному эндосомальному высвобождению мРНК
Почему этот новый трюк доставки важен
Многие из самых перспективных новых лекарств, от вакцин против COVID-19 до экспериментальных противораковых препаратов, созданы на основе матричной РНК, или мРНК. Но существует давняя проблема: как только эти хрупкие молекулы попадают в клетки, большая их часть застревает и разрушается в небольших внутренних мешочках, называемых эндосомами. В этом исследовании предложена продуманная переделка крошечных жировых пузырьков — липидных наночастиц, которые переносят мРНК. Переорганизовав их внутреннюю структуру вокруг твёрдого золотого ядра, исследователи значительно повысили долю мРНК, которая уходит в рабочее пространство клетки, где она может синтезировать полезные белки.
Новый план строения для крошечных курьеров
Современные мРНК-вакцины и терапии в основном используют мягкие, аморфные частицы из смеси липидов, окружающие мРНК. В теории специальные «ионизируемые» липиды в этих частицах должны принимать положительный заряд в кислой среде эндосомы и разрушать её мембрану, освобождая мРНК. На практике отрицательный заряд мРНК частично нейтрализует этот эффект, поэтому лишь около 2% доставленной мРНК достигают белкового аппарата клетки. Авторы задали простой, но мощный вопрос: вместо того чтобы менять только химию липидов, что если переинженерить внутреннюю архитектуру частицы, чтобы контролировать, где мРНК и липиды располагаются относительно друг друга?
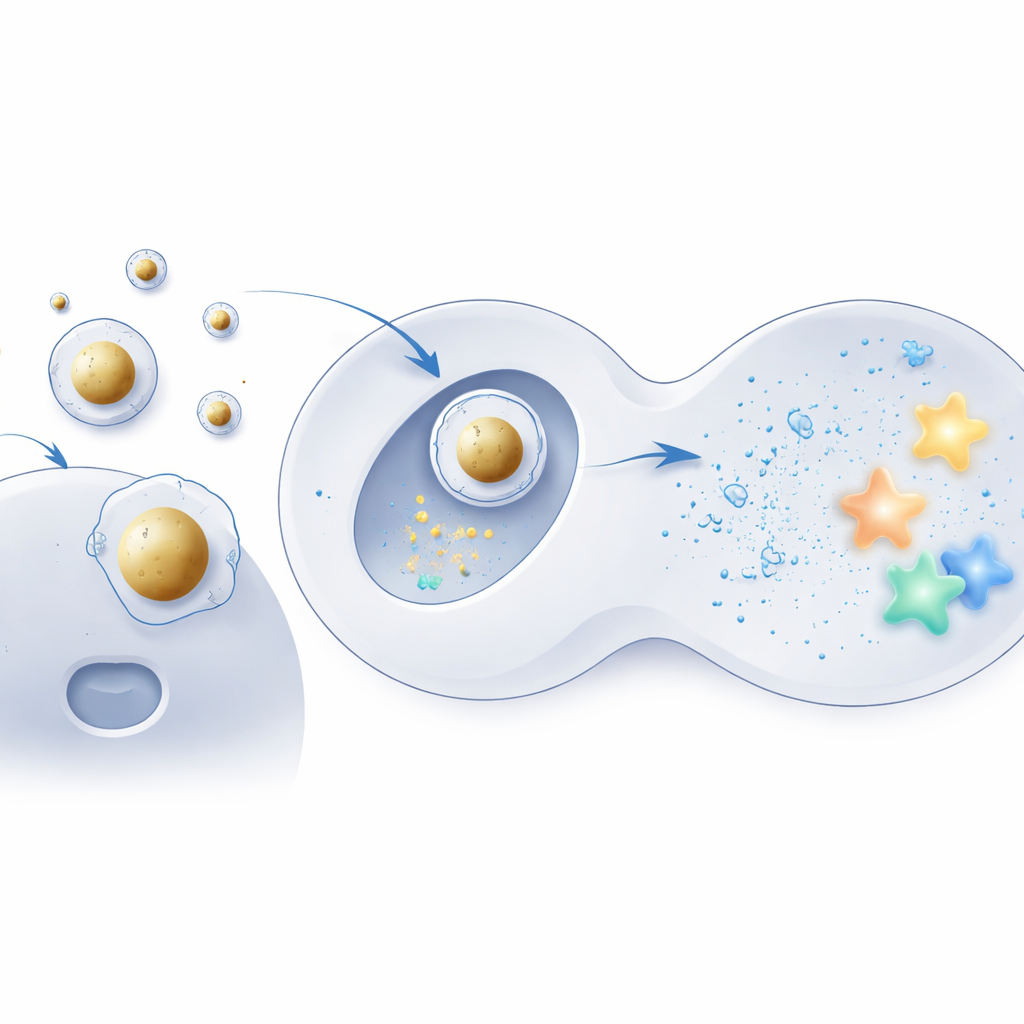
Создание оболочки доставки с золотым центром
Чтобы проверить эту идею, команда использовала крошечные золотые сферы как жёсткие ядра и покрыла их теми же ионизируемыми липидами, что применяются в обычных составах. Отрицательно заряженную мРНК сначала конденсировали на этих ядрах, и лишь затем сборку обёртывали знакомой смесью вспомогательных липидов и стабилизирующих молекул, создавая упорядоченную коро́бочно-оболочечную структуру. Электронная микроскопия и компьютерное моделирование показали, что эти «Au‑LNP» были высокооднородными, термодинамически стабильными и сохраняли форму в водных, приближенных к биологическим, условиях. Важно, что общий липидный состав оставался тем же, что и у стандартных частиц, выделяя внутреннюю структуру — а не ингредиенты — как ключевое изменение.
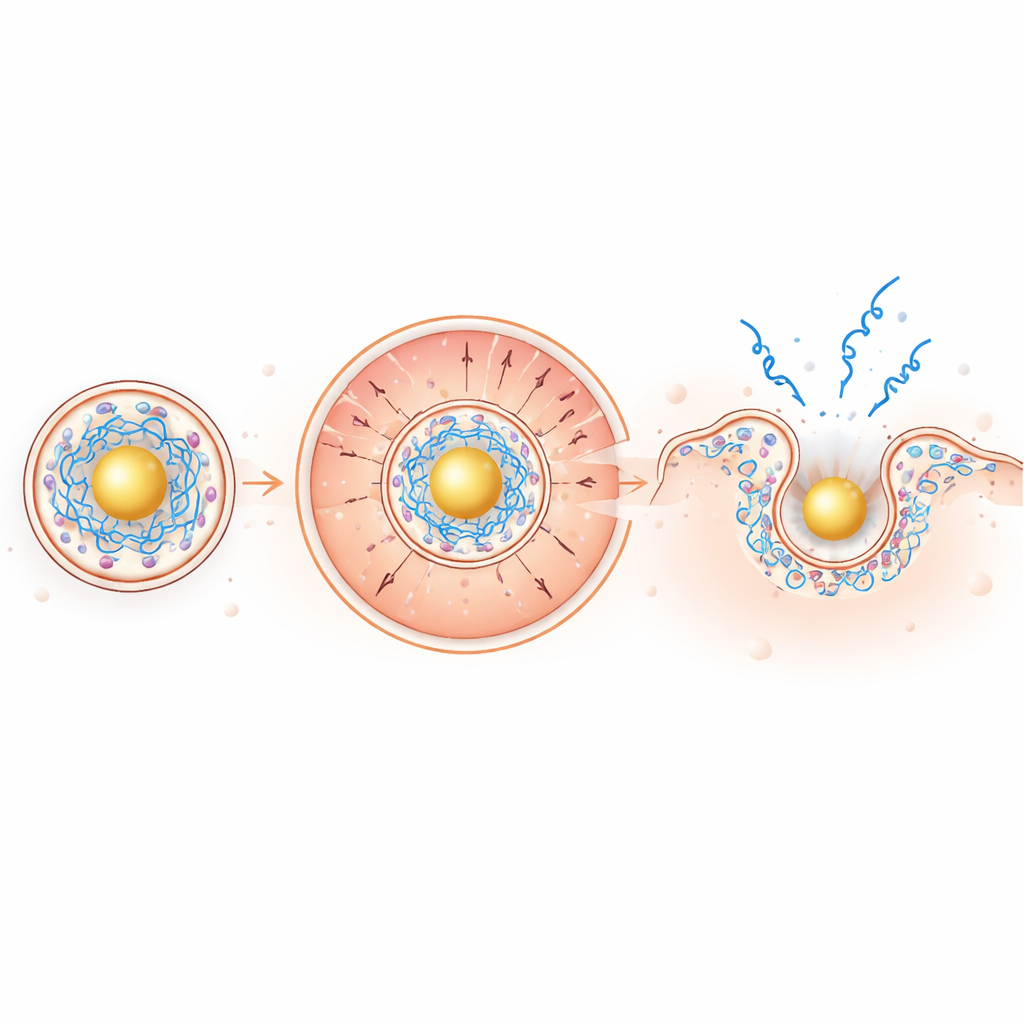
Как перестроенный интерьер усиливает побег
В слабо кислотной среде эндосомы золотообразное ядро становится сильно положительным, притягивая к себе отрицательно заряженную мРНК и выталкивая положительно заряженные ионизируемые липиды наружу, к окружающей мембране. Такое распределение зарядов концентрирует липиды, разрывающие мембраны, именно там, где они нужны. В тестах на модельных мембранах и в эритроцитах новые частицы эффективнее прокалывали мембраны при низком pH, оставаясь при этом инертными при нейтральном pH — желательное свойство с точки зрения безопасности. В живых клетках визуализация флуоресцентной мРНК показала приблизительно двукратное увеличение выхода из эндосом и поразительное примерно 100-кратное увеличение площади распространения мРНК по цитоплазме по сравнению со стандартными частицами.
От чашек Петри до мышей: более сильные сигналы и лучшая защита
Эти физические преимущества перешли в реальные биологические выигрыши. В разных типах клеток частицы с золотым ядром стимулировали значительно более высокий синтез репортёрных белков по сравнению со стандартными составами, особенно при низких дозах. У мышей они увеличивали продукцию белка, направляемого мРНК, в 5–7 раз после инъекций в мышцу или в вену, не изменяя при этом профиль распределения частиц по органам. При доставке мРНК-вакцины против S-пика SARS‑CoV‑2 переработанные частицы примерно удваивали уровень антител после первой инъекции и ещё увеличивали их после бустера, одновременно вызывая более мощные вирус-нейтрализующие антитела. В сложной модели тройного-негативного рака молочной железы мРНК-вакцины на новых частицах более эффективно уменьшали опухоли, снижали сигналы активности опухоли и заметно продлевали выживаемость.
Безопасность и путь к будущим препаратам
Несмотря на использование золота в ядре, частицы оказались хорошо переносимы у мышей. Масса тела, маркеры воспаления и гистологические исследования не выявили выраженной токсичности, а уровни золота в органах вернулись близко к исходному уровню в течение двух дней. Авторы подчёркивают, что золото служит главным образом демонстрационным каркасом: тот же принцип внутренней организации можно реализовать с использованием других безопасных или биоразлагаемых материалов. Главная мысль для неспециалистов — то, как мы упаковываем мРНК внутри её крошечного носителя, может быть столь же важным, как и то, с чем мы её упаковываем. Придавая липидным наночастицам более упорядоченную внутреннюю структуру, эта работа предлагает новый способ преодолеть давнюю узкую точку в доставке мРНК — открывая путь к более эффективным вакцинам и терапиям при инфекционных заболеваниях, раке и не только.
Цитирование: Li, T., Zhang, J., Guo, J. et al. Engineered internal architecture of core-shell lipid nanoparticles promotes efficient mRNA endosomal release. Nat Commun 17, 2187 (2026). https://doi.org/10.1038/s41467-026-69017-8
Ключевые слова: доставка мРНК, липидные наночастицы, побег из эндосомы, наномедицина, РНК-вакцины