Clear Sky Science · ru
FGF13 функционирует как регулятор оси ERK/аэробный гликолиз в воспалительном состоянии при септическом повреждении легких
Почему это исследование важно для пациентов с тяжелыми инфекциями
Сепсис — это опасное для жизни осложнение инфекции, которое может привести к отказу легких в течение нескольких часов, вынуждая пациентов зависеть от аппарата ИВЛ и повышая риск смерти. В этом исследовании изучается малоизвестный внутриклеточный белок FGF13 и раскрывается, как он способствует неконтролируемому воспалению и чрезмерному расходу энергии, сильно повреждающим легкие при сепсисе. Проследив эту скрытую контрольную схему, работа указывает на новые лекарственные мишени, которые могли бы усмирить «бурю» в легких, не подавляя полностью иммунную систему организма.
Скрытый участник повреждения легких при сепсисе
Исследователи начали с сопоставления тканей легких у септических мышей и пациентов и тканей у неконтролируемых (не септических) образцов. Они изучали семейство молекул, известных как фибробластные факторы роста, которые поддерживают здоровье легких. Среди них особенно выделялся FGF13: его уровни были значительно ниже в легких септических пациентов и животных. При картировании локализации FGF13 выяснилось, что он преимущественно находится внутри двух ключевых типов клеток: эндотелиальных клеток, образующих внутренний слой кровеносных сосудов, и макрофагов — иммунных клеток, реагирующих и усиливающих воспаление. В септических легких количество FGF13-позитивных эндотелиальных клеток и макрофагов было сильно уменьшено, что указывает на связь изменений этого молекулы с тяжелым повреждением легких.
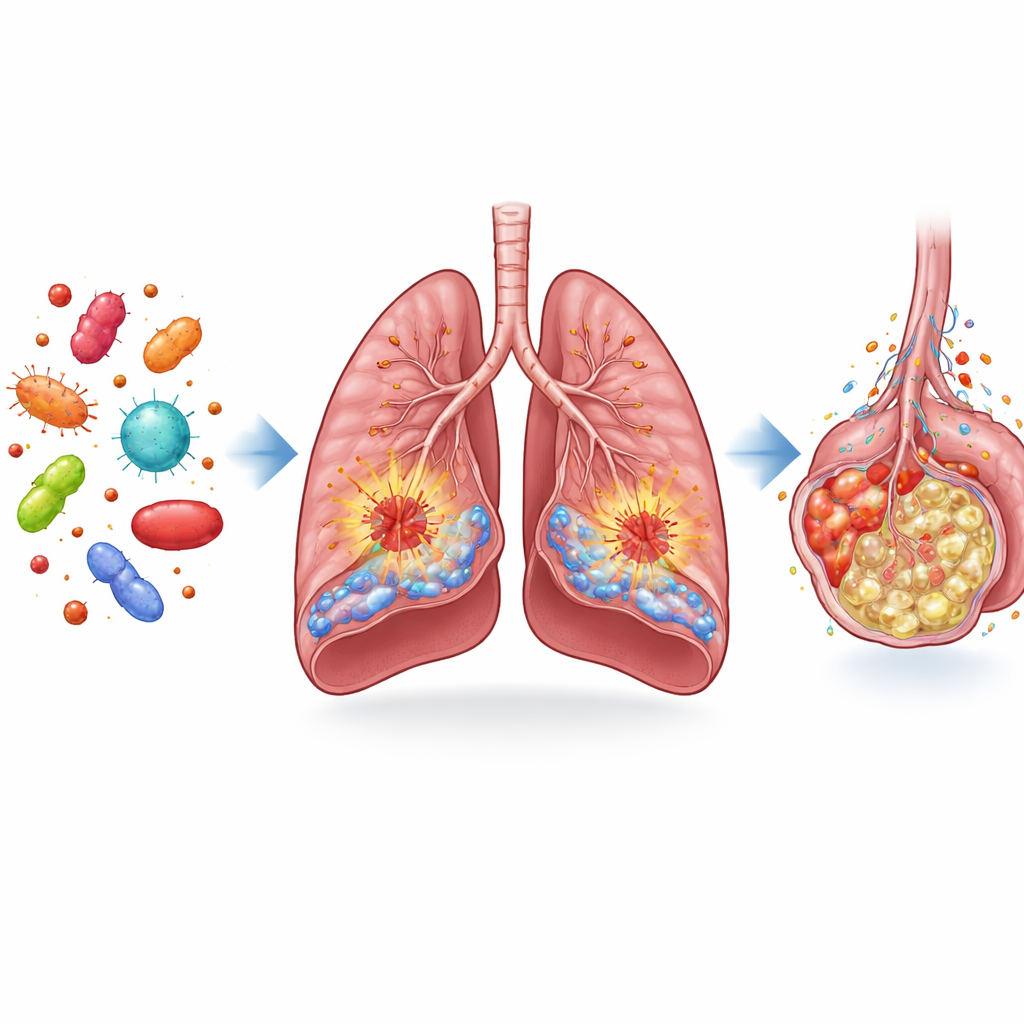
Как FGF13 превращает защитников легких в катализаторов повреждений
Чтобы проверить, что именно делает FGF13, команда использовала генетические инструменты у мышей, либо удаляя его в отдельных клетках, либо заставляя эти клетки синтезировать его в избытке. Когда FGF13 был удалён только в эндотелиальных клетках, у септических мышей отмечалось меньшее пропитывание и отек легких, меньшее вторжение иммунных клеток и лучшая выживаемость. Противоположный эффект наблюдался при усиленной продукции FGF13 в эндотелии: отёк легких, кровотечение и накопление воспалительных клеток усугублялись. Подобная картина прослеживалась и в макрофагах. Мыши с дефицитом FGF13 в этих иммунных клетках демонстрировали ослабленные воспалительные ответы и меньшее повреждение легких, тогда как макрофаги с принудительной сверхэкспрессией FGF13 выделяли больше провоспалительных молекул и усиливали повреждение. В культурах клеток снижение FGF13 делало клетки сосудистой стенки и макрофаги менее «прилипающими», менее воспалёнными и менее токсичными для соседей.
Воспалённые клетки переключаются на «сахарный» режим
Воспалённые клетки, как и раковые, часто меняют стратегию энергетического обмена: вместо медленного окислительного сжигания топлива они быстро расщепляют сахар в процессе, называемом аэробным гликолизом, с образованием молочной кислоты. Авторы показали, что FGF13 сильно способствует этому переключению. У септических мышей с дефицитом FGF13 в эндотелиальных клетках или макрофагах уровень лактата в крови был ниже. В культурах клетки с пониженным FGF13 поглощали меньше глюкозы и производили меньше лактата после воспалительной стимуляции, в то время как клетки с избыточным FGF13 демонстрировали усиленный гликолиз. Блокирование гликолиза препаратами значительно ослабляло провоспалительный эффект избытка FGF13, напрямую связывая вредоносную роль молекулы с этой программой «сжигания сахара».
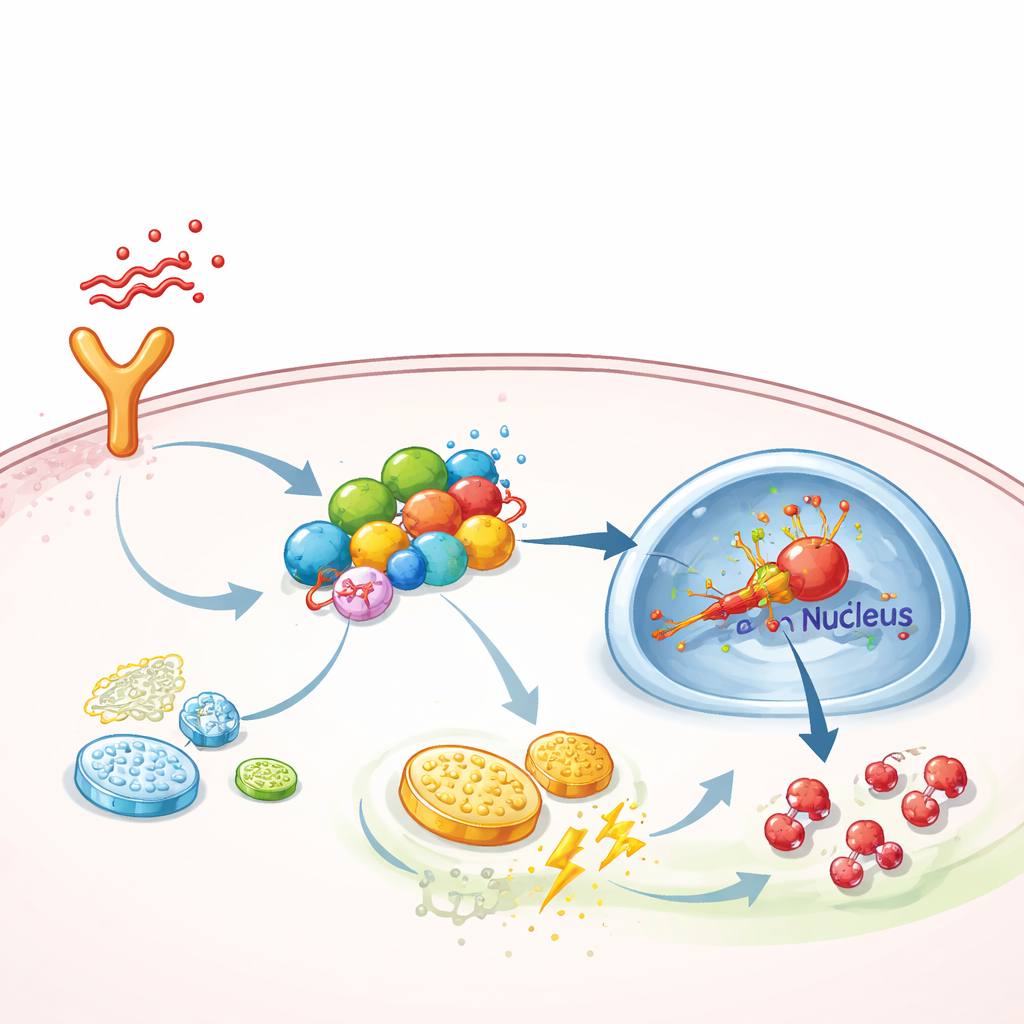
Молекулярный «каркас», усиливающий воспалительный сигнал
Углубляясь, команда выяснила, как FGF13 толкает клетки в этот высокоэнергетический режим. Они обнаружили, что FGF13 физически связывается с несколькими сигнальными белками, формирующими цепочку от рецепторов на поверхности до ядра клетки — в частности с каскадом TAK1–MEK–ERK, известным активацией главного регулятора реакции на гипоксию HIF-1α. FGF13 действует как каркас, удерживающий эти компоненты вместе и делая передачу сигналов более эффективной. При снижении FGF13 активация ERK и HIF-1α уменьшалась, и гликолиз ослабевал; при увеличении FGF13 путь становился гиперактивным. Сверхэкспрессия HIF-1α у мышей устраняла защитный эффект удаления FGF13, тогда как селективный ингибитор ERK, SCH772984, нейтрализовал вред от сверхпродукции FGF13 и улучшал состояние легких у септических животных.
Что это значит для будущих терапий при сепсисе
Для неспециалиста ключевое сообщение таково: септическое повреждение легких — это не просто случайное разрушение тканей; оно подпитывается конкретной молекулярной схемой внутри эндотелиальных клеток и макрофагов. FGF13 находится в центре этой схемы, помогая собрать сигнальный узел, который принуждает клетки перейти в «сахаролюбивое», высоковоспалительное состояние. Хотя уровни FGF13 падают при сепсисе — вероятно, как часть более широкого стрессового ответа — это исследование показывает, что оставшийся белок остаётся мощным источником вреда. Блокируя либо партнеров по сигналингу FGF13, либо вызываемое им гликолитическое переключение, возможно уменьшить отёк, проницаемость и воспаление легких, не парализуя способности организма бороться с инфекцией. Эта работа выделяет FGF13 и ось ERK–HIF‑1α–гликолиз как перспективные направления для разработки более точных и безопасных методов лечения при септической недостаточности легких.
Цитирование: Zhu, J., Wang, J., Jiang, C. et al. FGF 13 functions as a regulator of the ERK/aerobic glycolysis axis in the inflammatory state during septic lung injury. Nat Commun 17, 2383 (2026). https://doi.org/10.1038/s41467-026-69014-x
Ключевые слова: септическое повреждение легких, FGF13, эндотелиальное воспаление, аэробный гликолиз, ERK-сигналинг