Clear Sky Science · ru
Комбинированная таргетная и эпигенетическая терапия усиливает антиопухолевый иммунитет, стабилизируя GATA6-зависимое экспрессирование MHCI при аденокарциноме панкреатического протока
Почему это исследование важно для панкреатического рака
Аденокарцинома панкреатического протока — один из самых смертоносных видов рака, во многом потому что опухоль ускользает от иммунной системы и устойчиво сопротивляется большинству лекарств. В этом исследовании выявлено особое состояние опухолевых клеток, управляемое геном GATA6, которое делает клетки панкреатического рака более заметными для иммунной атаки. Авторы также показывают, как сочетание двух типов препаратов может сохранять это уязвимое состояние и усиливать способность цитотоксических Т-клеток атаковать опухоли в экспериментальных моделях.
Состояние опухолевой клетки, которое привлекает иммунную систему
Не все клетки панкреатического рака ведут себя одинаково. Часть сохраняет более упорядоченную, эпителиальную идентичность, тогда как другие переходят к более подвижному, агрессивному мезенхимоподобному состоянию. Транскрипционный фактор GATA6 помогает поддерживать эпителиальную идентичность и связан с лучшими исходами у пациентов. В больших когортах пациентов опухоли с высоким уровнем GATA6 содержали больше иммунных клеток, включая CD8 «киллерные» Т-клетки, чем опухоли с низким или отсутствующим GATA6. С помощью передовой пространственной визуализации образцов человеческих опухолей исследователи обнаружили, что GATA6-положительные раковые клетки чаще располагались рядом с CD8 Т-клетками и проявляли более высокий уровень молекулы MHCI, которая действует как флаг, показывающий Т-клеткам, что находится внутри клетки. Эти наблюдения указывали на то, что GATA6 маркирует популяцию опухолевых клеток, которая естественным образом более заметна для иммунной системы. 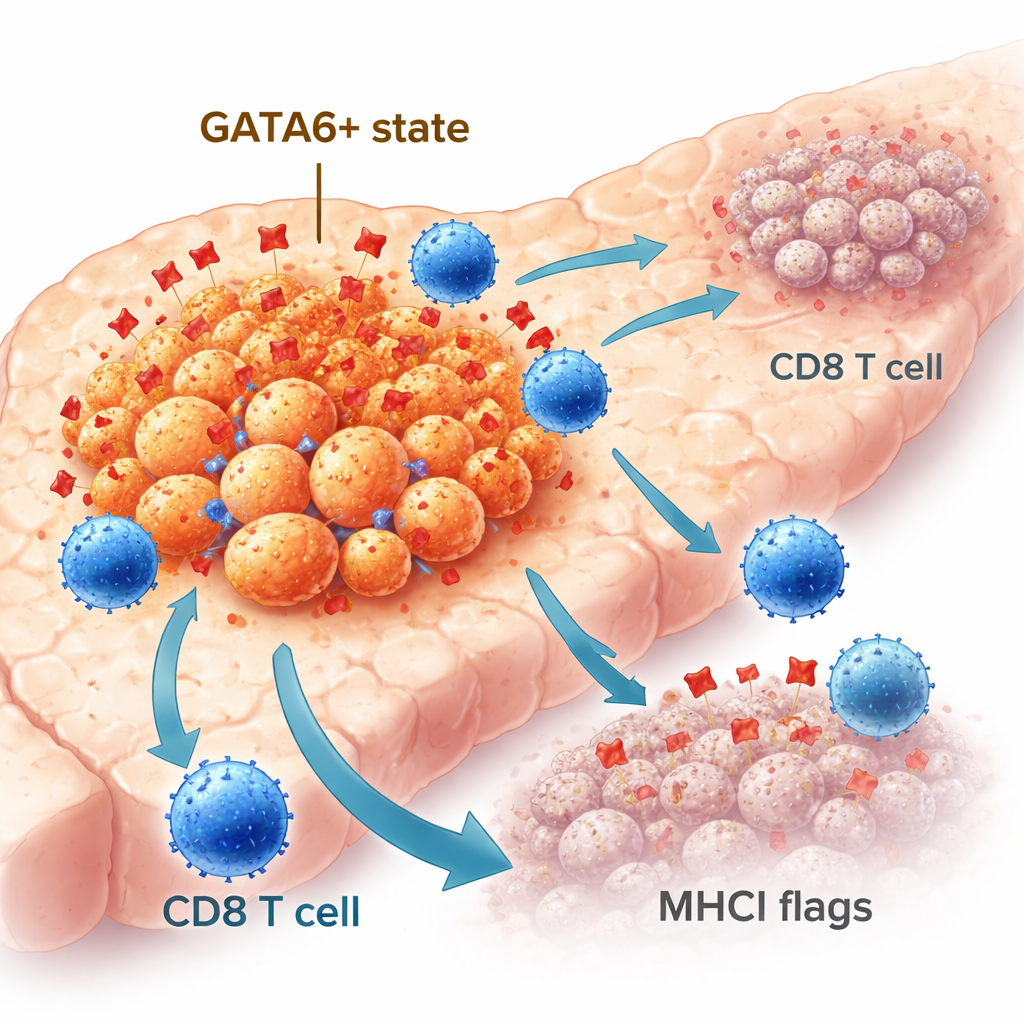
Таргетная терапия, повышающая видимость опухоли — но с ценой
Далее команда задала вопрос, могут ли таргетные препараты ещё больше повысить эту заметность. Они сосредоточились на ингибиторах MEK — классе препаратов, блокирующих сигнальный путь роста, часто активный при панкреатическом раке. В клеточных линиях рака поджелудочной железы мышей и в опухолях, выращенных у мышей и в ксенотрансплантатах, полученных от пациентов, ингибирование MEK увеличивало экспрессию MHCI на поверхности GATA6-высоких опухолевых клеток, делая их потенциально лучшими мишенями для Т-клеток. При лечении мышей с опухолями, богатыми GATA6, ингибиторами MEK рост опухолей замедлялся, уровень MHCI повышался, и в опухоли проникало больше CD8 Т-клеток, несущих цитотоксические молекулы. Прямое подавление GATA6 — либо удалением гена, либо быстрым деградированием белка — устраняло повышение MHCI и контроль опухоли, индуцированные ингибитором MEK, что демонстрирует, что GATA6 необходим для этого благоприятного эффекта.
Как опухоли приспосабливаются: переход в более трудноубиваемое состояние
Однако история имела поворот. Длительное лечение ингибиторами MEK приводило многие опухолевые клетки к переходу из GATA6-положительного эпителиального состояния в более мезенхимальное состояние с низким уровнем GATA6, ассоциированное с резистентностью к лечению. В моделях на мышах и в ксенотрансплантатах, обработанных ингибиторами MEK, со временем наблюдали меньше GATA6-положительных клеток, больше маркеров эпителиально-мезенхимального перехода и в целом менее устойчивый эффект. Хотя отдельные GATA6-положительные клетки по-прежнему повышали MHCI в ответ на препарат, сокращение этой популяции ограничивало общее улучшение презентации опухолевых антигенов, что помогало объяснить, почему ингибиторы MEK поодиночке разочаровали в клинических испытаниях при панкреатическом раке.
Эпигенетические препараты, удерживающие опухоли в уязвимом состоянии
Чтобы противодействовать этой адаптивной эскейп-стратегии, исследователи обратились к ингибиторам гистондеацетилаз (HDAC) — классу эпигенетических препаратов, известных влиянием на клеточную идентичность и иммунную заметность. В культурах клеток и моделях на мышах сочетание ингибиторов MEK с ингибиторами HDAC класса I, такими как доматинастат, восстанавливало экспрессию GATA6, подавленную ингибированием MEK, устраняло признаки эпителиально-мезенхимального перехода и дополнительно повышало уровень MHCI на опухолевых клетках. Важно, что эта комбинированная терапия приводила к более выраженной инфильтрации и активации CD8 Т-клеток и к большему уровню гибели опухолевых клеток в ортотопических опухолях мышей и в генетически модифицированной мышиной модели, близкой к человеческому панкреатическому раку. Истощение CD8 Т-клеток устраняло большую часть пользы, подтверждая, что комбинация действует главным образом за счет усиления эффективности киллерных Т-клеток.
К более продуманным комбинированным терапиям против сложного рака
Собрав эти данные вместе, исследование предлагает стратегию, при которой таргетное ингибирование MEK и эпигенетическое ингибирование HDAC используются совместно для стабилизации GATA6-управляемого состояния опухолевых клеток, богатого MHCI и потому легко узнаваемого иммунной системой. Путем как увеличения числа GATA6-положительных клеток, так и усиления их «флагов» MHCI это сочетание способствует более глубокой инфильтрации CD8 Т-клеток, усилению цитотоксической активности и продлению выживаемости в агрессивных мышиных моделях панкреатического рака. Хотя ингибиторы HDAC могут иметь значимые побочные эффекты и работа пока доклиническая, это исследование указывает на возможные будущие подходы к лечению, которые могли бы сочетать препараты, нацеленные на сигнальные пути, с тщательно подобранными эпигенетическими модуляторами, чтобы сделать панкреатические опухоли более уязвимыми для собственных иммунных защит организма. 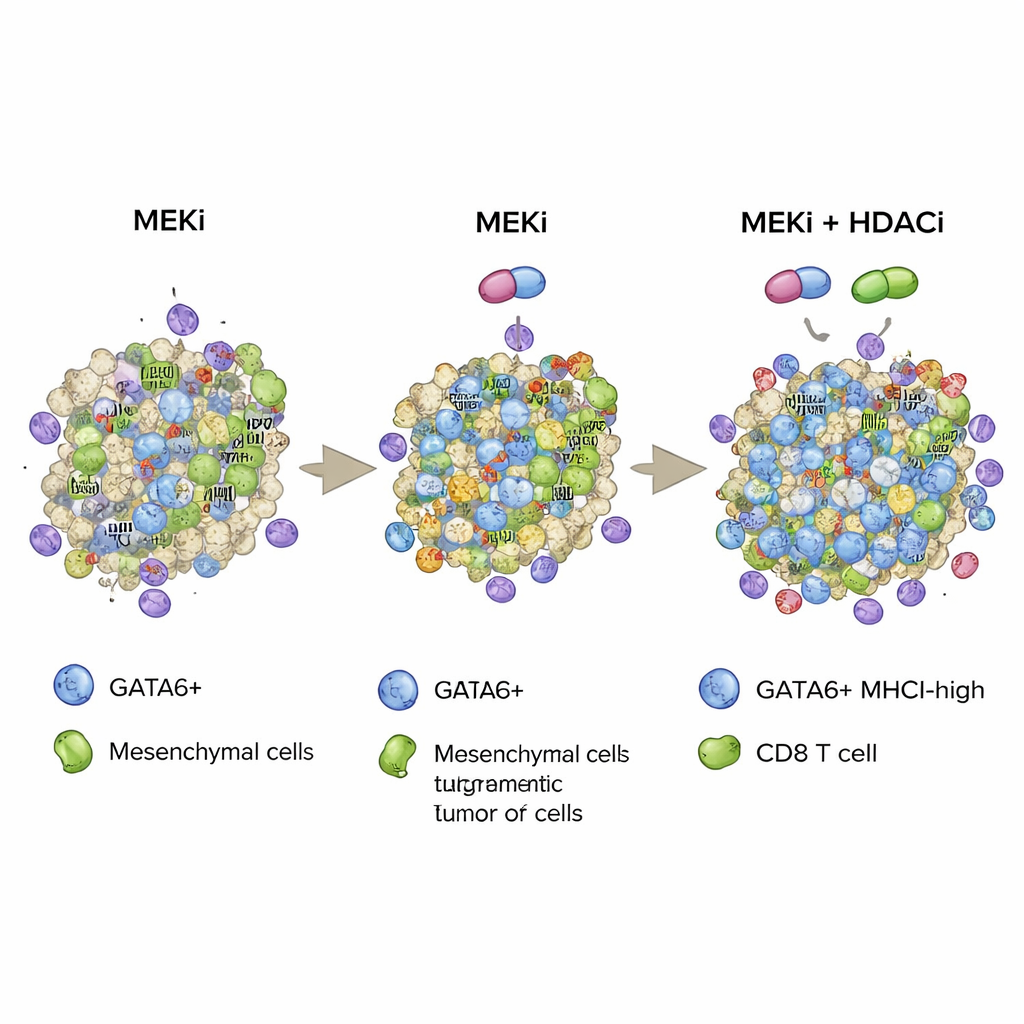
Цитирование: Peng, J., Yang, J., Antonopoulou, G. et al. Combined targeted and epigenetic-based therapy enhances antitumor immunity by stabilizing GATA6-dependent MHCI expression in pancreatic ductal adenocarcinoma. Nat Commun 17, 1476 (2026). https://doi.org/10.1038/s41467-026-69013-y
Ключевые слова: панкреатический рак, опухолевый иммунитет, GATA6, ингибитор MEK, ингибитор HDAC