Clear Sky Science · ru
AACRNL эволюционировал из фактора вирулентности в эпигенетического паразита, приводящего к расширению генома у свободноживущих эукариот
Когда старые токсины осваивают новые трюки
Наши геномы — это не тихие инструкции. Это переполненные арены, где гены, вирусы и мобильная ДНК постоянно соперничают за место и контроль. В этом исследовании обнаружен неожиданный участник этой борьбы: белок, который зародился как токсин, применяемый микробами для атаки хозяев, но затем был перепрофилирован внутри свободноживущих животных в нечто вроде «эпигенетического паразита», помогающего самому себе расширять присутствие в геноме.
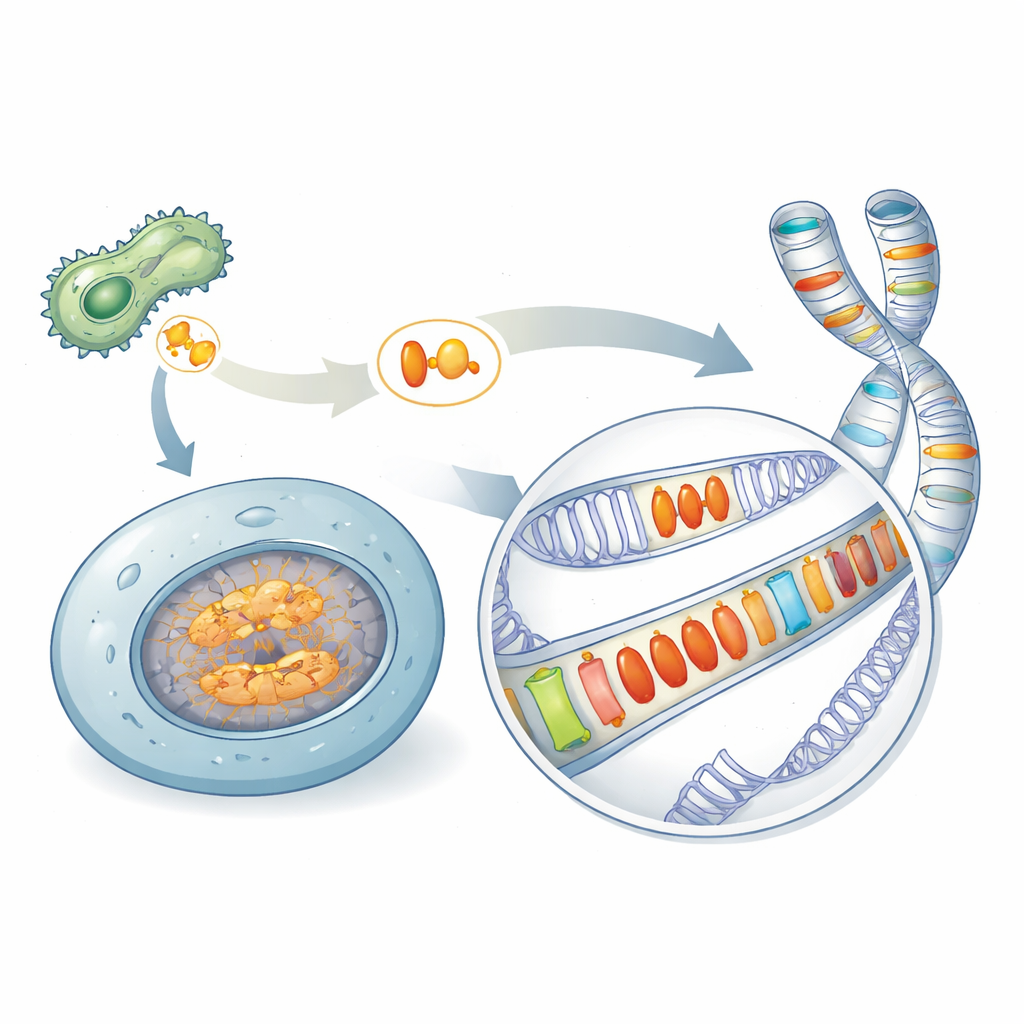
Скрытое наследие микробных оружий
Многие патогенные микроорганизмы полагаются на специальные белки, называемые эффекторами, чтобы саботировать защиту инфицируемых организмов. Одна известная семья, называемая Crinklers, считалась присущей только патогенам. Просканировав широкий набор видов, авторы обнаружили родственные белки — здесь объединённые под именем AACRNL — в неожиданных местах, включая губок, кораллы, морских ежей и костистых рыб, которые не являются классическими патогенами. Эти белки AACRNL сохраняют токсиноподобное ядро, способное химически модифицировать другие белки, но их передняя «транспортная» часть, которой патогены пользуются для проникновения в клетки хозяина, в основном разрушена. Такая структурная перестройка указывает на переход от атаки других организмов к действию внутри собственных клеток хозяина.
Эгоистичное переключение в геноме
У костистых рыб гены AACRNL встречаются в нескольких копиях, разбросанных по разным хромосомам. Сравнивая соседние участки ДНК, исследователи показали, что некоторые линии AACRNL перестали копироваться, тогда как другие умножились с помощью рядом расположенных движущихся сегментов ДНК, называемых транспозонами. Эти транспозоны действуют как геномные шаттлы: при перемещении или дупликации они могут утащить за собой AACRNL. В результате получается мозаика повторяющихся копий AACRNL, встроенных среди последовательностей транспозонов — характерный признак гена, распространяющегося ради собственной выгоды, а не ради пользы хозяина.
Снятие «тишины» генома
Обычно клетки держат такую мобильную ДНК в строжайшем контроле. Одной из ключевых защит является химическая метка на белках упаковки ДНК, известная как H3K27me3, которая помогает удерживать опасные или шумные регионы в выключенном состоянии. Авторы обнаружили, что активная версия AACRNL у рыб, названная AACRNLβ, может химически модифицировать EZH2 — фермент, налагающий эту репрессивную метку. Когда AACRNLβ изменяет EZH2, уровень H3K27me3 на собственном генетическом участке и на соседних транспозонах снижается, локальная ДНК становится более доступной, и как AACRNLβ, так и его транспозонные соседи начинают выражаться сильнее. По сути, белок нажимает собственную кнопку «включено» и ослабляет тормоза у тех самых мобильных элементов, которые могут переносить его в новые участки генома.
Уклонение от иммунных сторожей
Освобождение транспозонов и аномальной генетической активности рискует привлечь внимание иммунной системы. Исследование демонстрирует, что AACRNLβ решает эту проблему тоже. Он присоединяет небольшую химическую метку к TRAF6 — центральному белку‑хабу, который помогает запускать противовирусные и воспалительные сигналы. Отмеченный таким образом TRAF6 становится менее стабильным и всё чаще помечается для утилизации клеточными механизмами ограничения. Ослабив этот сигнальный узел, ключевые защиты активируются слабее, создавая более терпимую среду, в которой AACRNLβ и связанные с ним транспозоны могут сохраняться и копироваться с меньшими рисками быть замеченными.
Хрупкая гонка вооружений внутри клетки
История не заканчивается на том, что AACRNLβ действует без ограничений. Тот же белок TRAF6, на который нацеливается AACRNLβ, в свою очередь может прикреплять свои метки к самому AACRNLβ, помечая паразитоподобный белок для разрушения. Это взаимное противодействие похоже на молекулярную гонку вооружений: AACRNLβ использует химию, унаследованную от токсина, чтобы изгибать хроматин и иммунитет в свою пользу, в то время как белки хозяина отвечают деградацией и делают его активность спорадичной и рискованной. Авторы утверждают, что это перетягивание каната позволило бывшему микробному оружию выжить как эгоистичному жителю свободноживущих геномов, увеличивая содержимое ДНК и меняя правила генетического конфликта изнутри.
Почему это важно для нашего представления о геномах
Для неспециалиста главный вывод таков: геномы — это не только чертежи, оптимизированные для выживания хозяина. В них также селятся оппортунисты. Эта работа показывает, что даже классические токсины могут быть усыновлены в такие элементы, используя свою исходную деструктивную химию, чтобы пройти через эпигенетические замки и иммунные сигналы и распространяться по геному в ходе эволюции. Понимание этого скрытого конфликта помогает объяснить, почему геномы такие большие, сложные и динамичные, и указывает на то, что другие «отставные» токсины могут тихо переписывать ДНК во многих видах, возможно, и в нашем собственном.
Цитирование: Xu, T., Geng, S., Lv, X. et al. AACRNL evolved from virulence factor to epigenetic parasite driving genome expansion in free-living eukaryotes. Nat Commun 17, 2130 (2026). https://doi.org/10.1038/s41467-026-69012-z
Ключевые слова: эгоистичные генетические элементы, эволюция генома, эпигенетическая регуляция, транспозоны, врожденный иммунитет