Clear Sky Science · ru
Многокомпонентная синергетическая иммобилизация с помощью in-situ и динамических обменных стратегий для создания иерархических биофармацевтических препаратов
Почему важно создавать более умные лекарства
Многие из самых мощных современных лекарств — это крупные, хрупкие биомолекулы, такие как белки и ферменты. Они могут бороться с раком, уничтожать вредные бактерии и ускорять заживление, но легко повреждаются и их трудно доставить в нужное место организма. В этой работе описан новый способ «упаковать» несколько таких чувствительных компонентов вместе внутри защитного губчатого материала, чтобы они могли работать последовательно с большей эффективностью и меньшими побочными эффектами.
Превращение кристалла в молекулярный жилой дом
Исследователи начинают со специального пористого материала, собранного из ионов металлов и небольших органических строительных блоков. Он ведёт себя как крошечный гибкий жилой дом с комнатами и коридорами. Они показывают, что этот каркас, называемый цеолитоподобным пиримидиновым каркасом, можно вырастить вокруг белков так, что белки оказываются защищёнными внутри кристалла. Такое «in-situ» захватывание не разрушает и не дезактивирует белки, а детальная визуализация подтверждает их равномерное распределение по всему объёму, словно жильцы, заселившие все этажи дома.
Хозяин, меняющий форму, для украшения поверхности
У того же материала есть ещё один неожиданный приём: он может обратимо изменять свою внутреннюю структуру при контакте с определёнными растворителями или водой. В ходе этого щадящего изменения некоторые химические связи в каркасе ослабляются, а затем вновь формируются. Команда обнаружила, что определённые химические группы на поверхности белков — например, встречающиеся в некоторых аминокислотах — могут воспользоваться этим моментом ослабления. Они временно конкурируют с исходными строительными блоками каркаса и проникают в вновь образующиеся «дефекты» на поверхности. В результате формируется слой белков, прикреплённых преимущественно снаружи кристалла, тогда как внутренние белки остаются на своих местах. Этот процесс динамического обмена позволяет учёным контролировать, какие компоненты размещаются глубоко внутри, а какие украшают внешнюю оболочку.
Проектирование ферментных конвейеров
Имея под контролем как внутренние, так и наружные пространства, авторы создают крошечные ферментные «сборочные линии». В одном примере фермент, превращающий сахар в агрессивный побочный продукт, запирается внутри каркаса, в то время как второй фермент, безопасно разрушающий этот побочный продукт, фиксируется ближе к поверхности. Такое внутренне‑внешнее расположение ускоряет и делает реакцию более эффективной по сравнению с традиционными конструкциями «ядро–оболочка» или случайными смесями ферментов. Поскольку наружные ферменты легче доступны для молекул, а вредный промежуточный продукт быстро удаляется, система остаётся активной в течение многих циклов и лучше выдерживает тепло, жёсткие условия и многократное использование.
Умные противораковые и антибактериальные упаковки
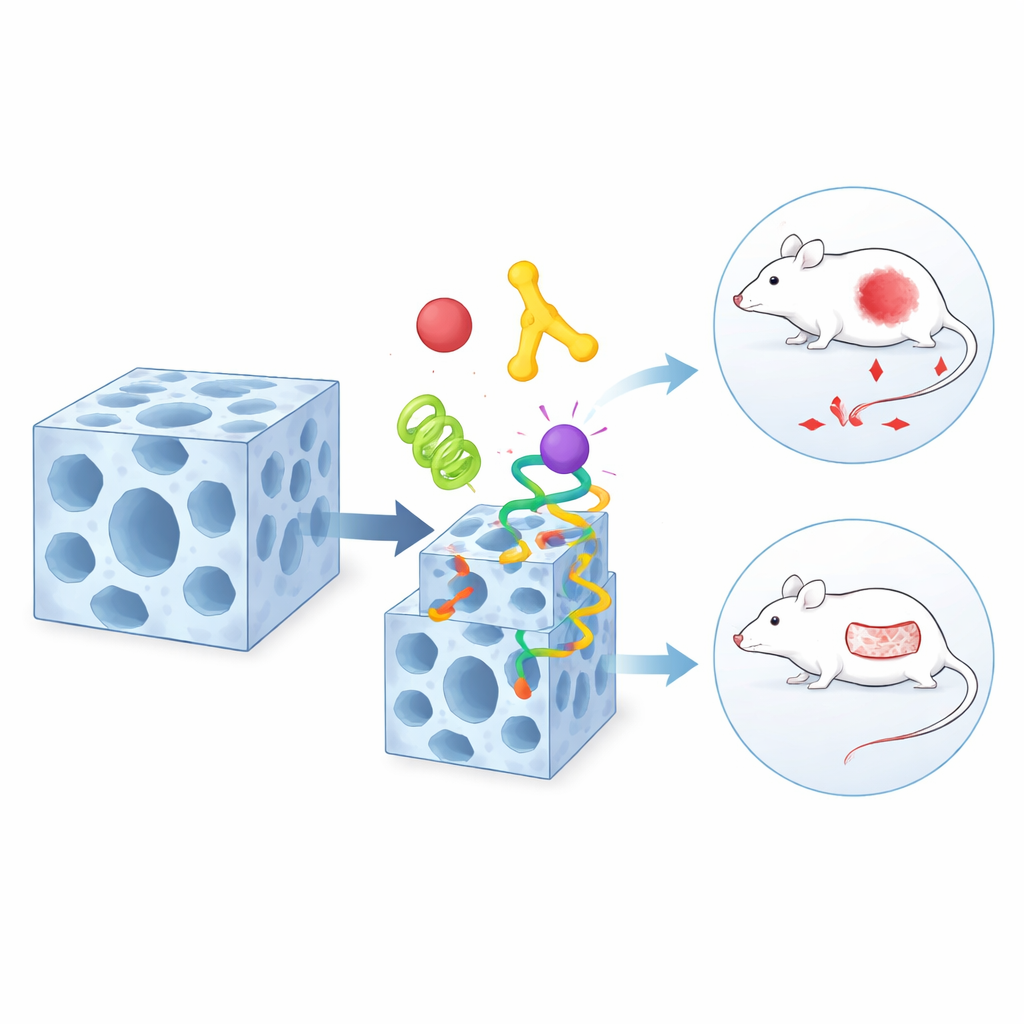
Истинная сила этого подхода проявляется при применении в медицине. Команда сочетает белок, нацеливающийся на опухоль, фермент, «поедающий» глюкозу, и стандартный химиотерапевтический препарат в одной слоистой частице. Поверхностный таргетный компонент направляет частицу к раковым клеткам, фермент исчерпывает их энергоресурсы, потребляя местный сахар, а маломолекулярный препарат наносит дополнительный смертельный удар. У мышей с имплантированными человеческими опухолями этот трёхкомпонентный пакет сокращает опухоли значительно эффективнее, чем любой из компонентов по‑отдельности или более простые комбинации. В другом варианте авторы адаптируют каркас для инфицированных кожных ран, размещая антибактериальный пептид и энзим, восстанавливающий ткань, в разных областях одного носителя. В модельных экспериментах на крысах такие частицы резко снижают инфекцию и ускоряют закрытие трудно заживающих ран по сравнению с обычными методами лечения.

Как эта работа продвигает медицину вперёд
Для неспециалиста ключевая мысль заключается в том, что это исследование превращает один пористый кристалл в программируемый дом для множества терапевтических молекул. Определяя, кто живёт внутри, кто располагается на поверхности и в каком соотношении, исследователи могут оркестрировать поэтапные лечения — сначала нацеливание, затем атака, затем восстановление — внутри одного крошечного объекта. Эта стратегия не только защищает хрупкие биологические препараты, но и позволяет им взаимно усиливать действие, приводя к более мощным и точным противораковым и антибактериальным терапиям. Те же принципы дизайна могут быть адаптированы для многих будущих «умных лекарств», которым нужно согласованное действие нескольких компонентов в нужном месте и в нужное время.
Цитирование: Yang, M., Meng, X., Shi, R. et al. Multicomponent synergistic immobilization via in-situ and dynamic exchange strategies for constructing hierarchical biopharmaceuticals. Nat Commun 17, 2208 (2026). https://doi.org/10.1038/s41467-026-69009-8
Ключевые слова: металлоорганические каркасы, иммобилизация ферментов, наномедицина против рака, заживление ран, доставка биофармацевтических средств