Clear Sky Science · ru
Внеклеточный матрикс обеспечивает кластеризацию циркулирующих опухолевых клеток при метастазировании тройного-негативного рака молочной железы
Как «отступившие» раковые клетки молочной железы объединяются в кровотоке
Когда рак молочной железы распространяется, это часто происходит потому, что отдельные раковые клетки попадают в кровоток и дают начало опухолям в отдалённых органах. В этом исследовании рассматривается на первый взгляд простой, но очень важный вопрос: как самые агрессивные раковые клетки, потерявшие свои привычные «липучки» для сцепления, всё же умудряются путешествовать плотными кластерами — и почему это делает их особенно опасными?
Липкий сахарный «плащ», заменяющий классический клеточный клей
Авторы сосредоточились на тройном-негативном раке молочной железы (TNBC) — особенно агрессивной форме, которая часто даёт циркулирующие опухолевые клетки (CTC) в кровь. В многих опухолях кластеры CTC гораздо вероятнее приводят к метастазам, чем одиночные клетки. Обычно такие кластеры удерживаются эпителиальными адгезивными контактами — специальными белковыми комплексами, которые действуют как молекулярные заклёпки между соседними клетками. Но клетки TNBC часто теряют эти белки сцепления, что создаёт парадокс: без привычного клея что удерживает их кластеры? Анализ больших баз данных генов рака показал, что в опухолях TNBC повышена экспрессия генов, связанных с внеклеточным матриксом — внешним каркасом клетки. Один из выделяющихся генов, HAS2, кодирует фермент, синтезирующий гиалуронан (HA) — длинный сахарный полимер, покрывающий поверхность клеток. Высокие уровни HAS2 и HA были тесно связаны с агрессивными, метастатическими свойствами опухолей.
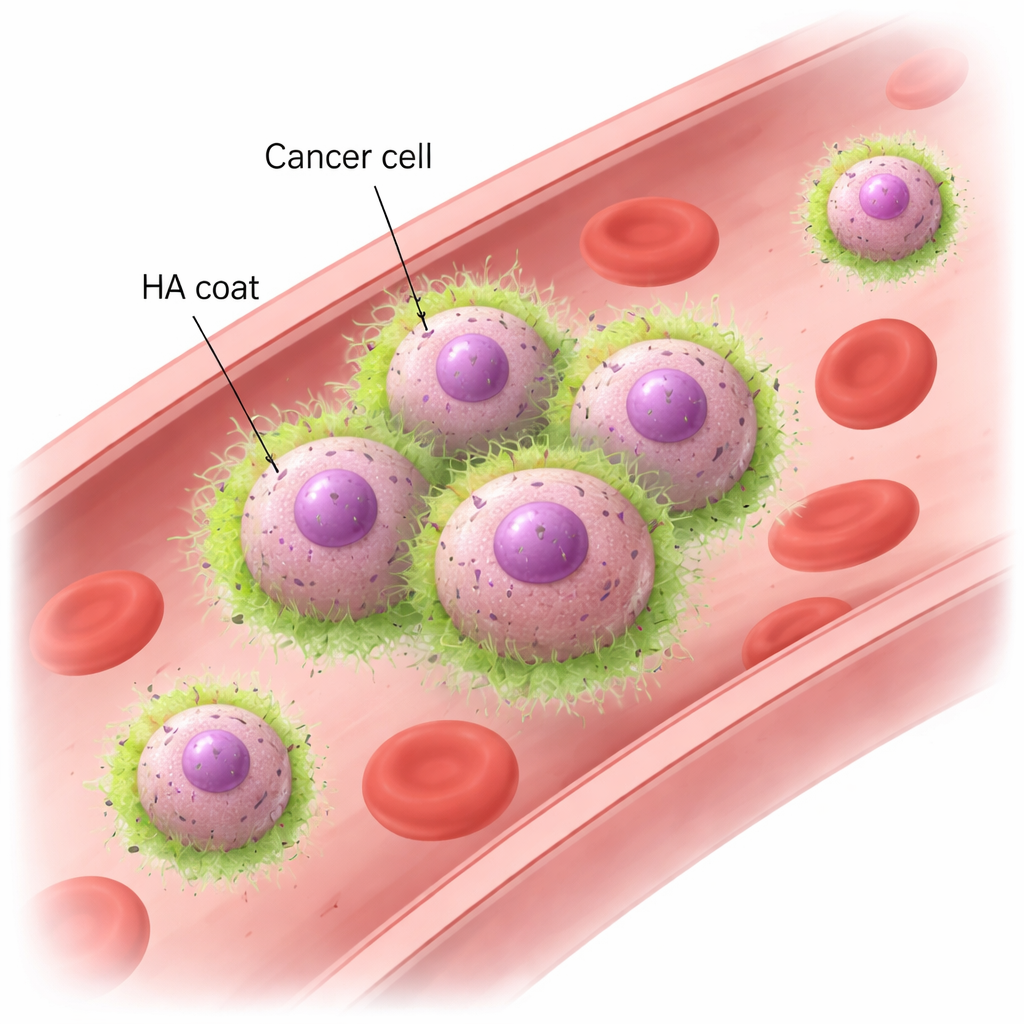
Гиалуронан и CD44: новый способ «держаться за руки»
С помощью моделей на мышах и линий человеческих раковых клеток молочной железы команда показала, что метастатические клетки TNBC быстро образуют кластеры при воздействии вихревого потока, имитирующего кровоток. Эти кластеры остаются целыми даже под воздействием сил, сопоставимых с реальными кровеносными сосудами, тогда как менее агрессивные клетки распадаются и дрейфуют поодиночке. Микроскопия показала, что метастатические клетки покрыты «плащом» из HA, который концентрируется именно в местах контакта между клетками. Удаление HA ферментами или подавление HAS2 лишало клетки способности образовывать кластеры в потоке, хотя при отсутствии потока такие клетки могли оседать вместе. Ключевой партнёр на поверхности клетки — CD44, общий рецептор, связывающий HA. Клетки без CD44 не могли удерживать HA на поверхности и теряли способность к кластеризации. Наоборот, нечёткие клетки, генетически модифицированные для продукции HAS2 и CD44, приобрели устойчивую способность к образованию кластеров. Эти эксперименты показали, что взаимодействие HA с CD44 одновременно необходимо и достаточно для того, чтобы раковые клетки удерживались вместе в быстром кровотоке.
Мелкие выступы и механические «замки» создают прочные кластеры
Высокорасрешающая визуализация раскрыла физическую хореографию образования кластеров. Одиночные клетки TNBC выпускают многочисленные тонкие, актин-зависимые мембранные выступы — своего рода «щупальца» — усеянные CD44 и увенчанные HA. Когда две клетки сближаются, эти щупальца сначала встречаются и образуют начальные мостики HA–CD44. Со временем выступы скользят друг рядом с другом, притягивая тела клеток ближе, пока огромные участки мембран не окажутся почти бок о бок. Этот процесс напоминает формирование адгезивных контактов в нормальных эпителиальных клетках, но здесь он опирается на гибкий сахарный слой, а не на жёсткие белковые цепи. По мере созревания зоны контакта включается ещё один набор структур: десмосомы — прочные соединения, связывающие мембраны клеток с их внутренним каркасом. Белки десмосом накапливаются только после установления HA-опосредованного контакта и действуют как механические «замки», помогающие кластерам противостоять разрывным силам потока. При снижении компонентов десмосом кластеры формировались, но распадались при более высоком сдвиговом напряжении.
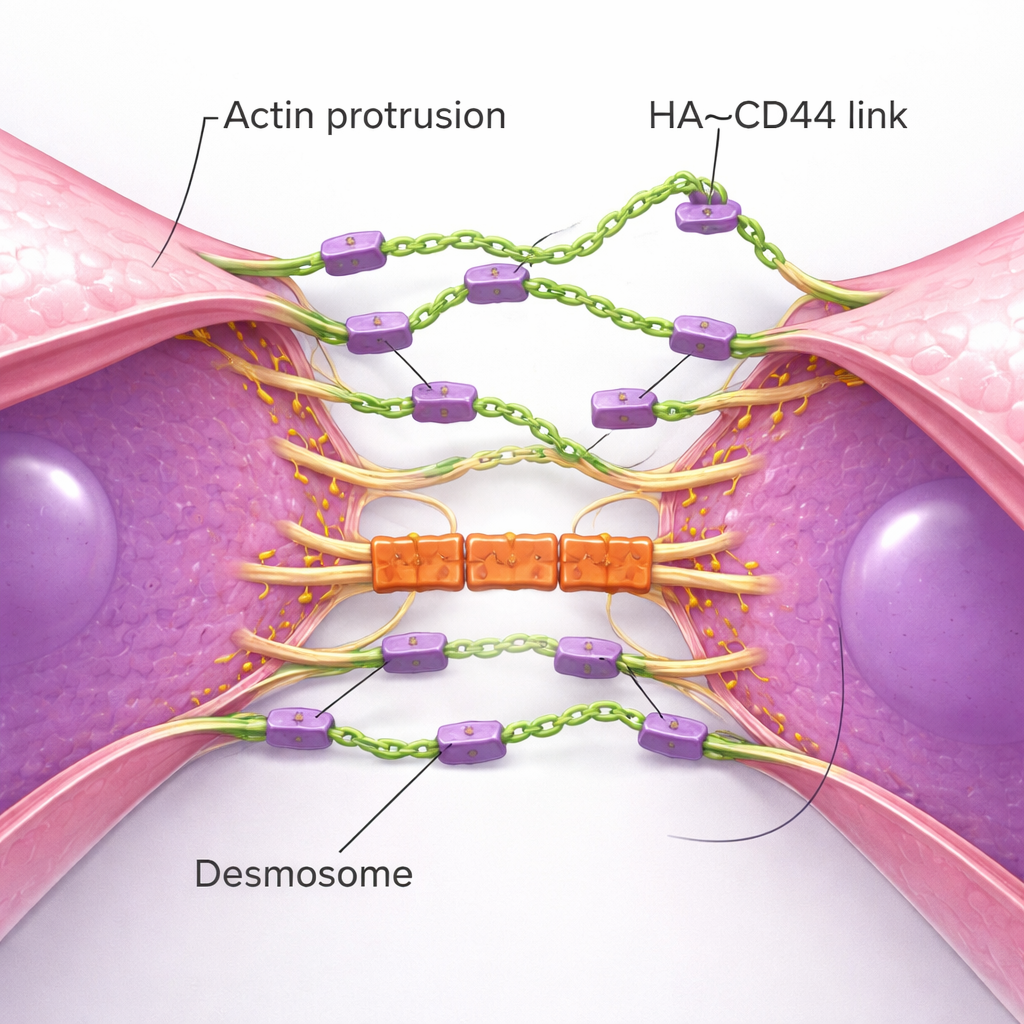
Почему кластеризация важна для выживания и метастазирования
Система кластеризации на основе HA оказалась не просто способом оставаться вместе — она прямо повышала выживаемость. При длительном моделировании кровотока HA-богатые кластеры демонстрировали значительно более низкие уровни повреждающих реактивных форм кислорода и намного меньше гибели клеток по сравнению с очищенными от HA одиночными клетками. В моделях на мышах клетки TNBC без HAS2 давали гораздо меньше CTC, образовывали только крошечные кластеры и вызывали значительно меньше метастазов в лёгких — хотя их первичные опухоли росли не хуже. Когда вливали заранее сформированные кластеры контрольных и лишённых HAS2 клеток, HA-бедные клетки гораздо реже успешно колонизировали лёгкие. Кроме того, HA-покрытые CTC могли «набирать» другие клетки — как раковые клетки без HA, так и нормальные иммунные клетки, например нейтрофилы — в смешанные кластеры при условии, что у этих партнёров был CD44. Анализ крови пациенток с метастатическим TNBC показал ту же картину: CTC часто были покрыты HA, причём HA концентрировался в местах контакта между опухолевыми клетками и между опухолевыми и не-опухолевыми клетками.
Что это значит для пациентов и будущих терапий
Для неспециалиста главный вывод таков: некоторые из наиболее смертоносных клеток рака молочной железы путешествуют не в одиночку, а в виде маленьких кооперативных групп, удерживаемых наружным сахарным «плащом» и его рецептором, а не классическими «заклёпками» между клетками, характерными для нормальных тканей. Этот механизм на основе HA–CD44 помогает опухолевым клеткам выживать в жёстком кровотоке, объединяться друг с другом и с поддерживающими клетками крови и эффективнее посылать метастазы в отдалённые органы. В теории, подавление синтеза HA (например, ингибирование HAS2) или блокирование взаимодействия HA с CD44 могло бы ослабить эти кластеры и затруднить метастазирование TNBC, что открывает новое направление для разработки противометастатических терапий.
Цитирование: Bobkov, G.O., Patel, K.J., Lege, B.M. et al. Extracellular matrix mediates circulating tumor cell clustering in triple-negative breast cancer metastasis. Nat Commun 17, 1352 (2026). https://doi.org/10.1038/s41467-026-69007-w
Ключевые слова: тройной-негативный рак молочной железы, циркулирующие опухолевые клетки, гиалуронан, CD44, метастазирование