Clear Sky Science · ru
Escherichia coli способствует метастазированию колоректального рака, поддерживая петли «энхансер–промотор» через высвобождение внеклеточных ловушек нейтрофилов
Кишечные микробы и скрытая магистраль рака
Колоректальный рак часто убивает не из‑за первичной опухоли в кишечнике, а потому что раковые клетки мигрируют в печень и там оседают. В этом исследовании выявлен неожиданный соучастник этого пути: обычная кишечная бактерия Escherichia coli. Отслеживая цепочку событий от бактерий в кишечнике до агрессивных опухолей в печени, авторы показывают, как микроорганизмы, иммунные клетки и архитектура ДНК внутри раковых клеток могут действовать сообща, подпитывая метастазирование — и предлагают новые подходы, чтобы разорвать эту цепочку.
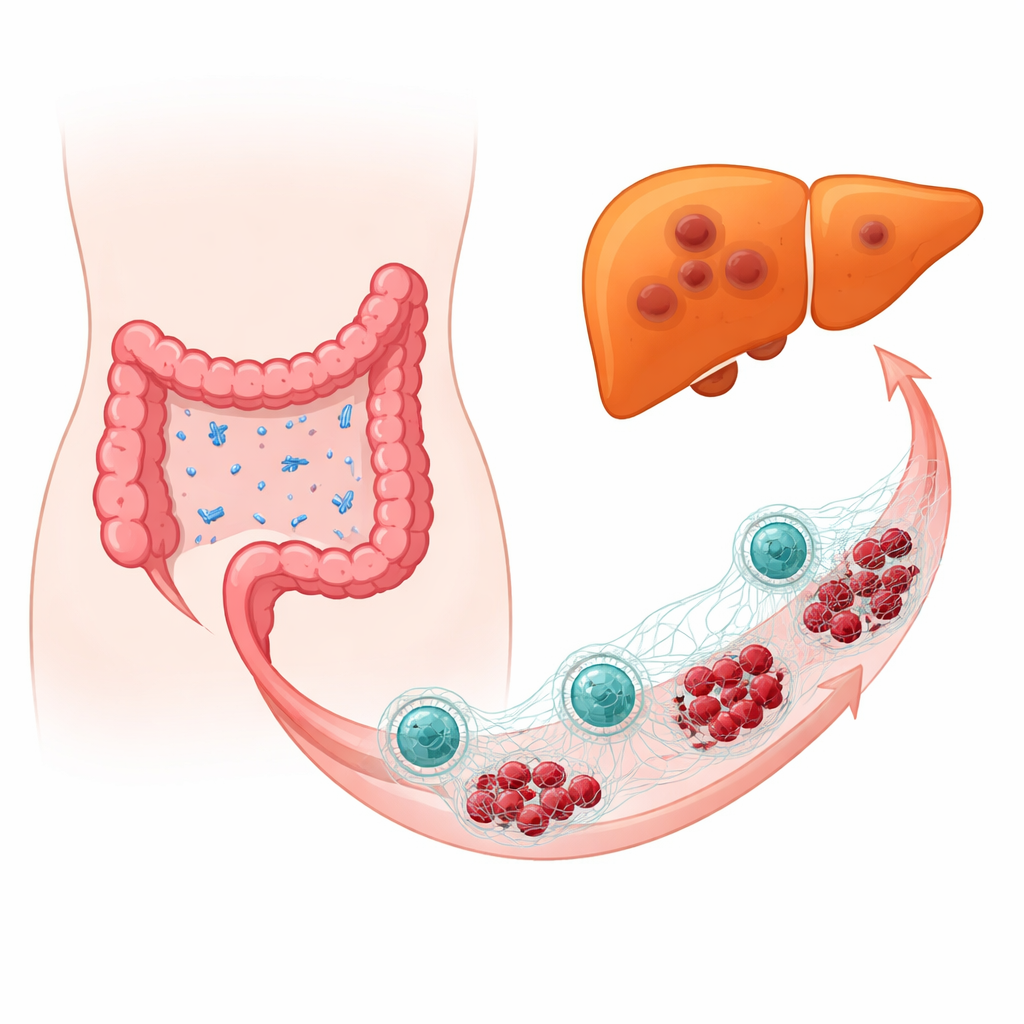
Когда «дружественные» бактерии становятся враждебными
Команда изучила образцы опухолей у пациентов с колоректальным раком, сравнив те случаи, при которых рак уже метастазировал в печень, с теми, где этого не произошло. С помощью высокоточной ДНК‑типизации микробиоты они обнаружили, что E. coli встречалась в значительно больших количествах в опухолях, уже давших отсевы в печень. В модельных экспериментах на мышах и на мышах с «очеловеченной» иммунной системой целенаправленное добавление E. coli рядом с колоректальными опухолями делало метастазы в печени крупнее и более частыми и переводило опухолевые клетки в более подвижное, инвазивное состояние. Даже когда большую часть нормальной флоры убирали антибиотиками и заново вводили только E. coli, бактерия по‑прежнему усиливала рост и распространение опухоли, что указывает на роль именно E. coli, а не на общее нарушение микробиоты.
Иммунные сети, помогающие раку сбежать
Нейтрофилы — первичные клетки иммунной защиты, которые обычно ловят и уничтожают микробы — оказались ключевыми посредниками. В ответ на E. coli нейтрофилы выпускали сетевидные структуры, называемые внеклеточными ловушками, состоящие из ДНК и токсичных белков. Эти сети предназначены для захвата бактерий, но в описанном контексте они непреднамеренно защищали и усиливали раковые клетки. Когда исследователи разрушали сети ферментами или блокировали важные ферменты, необходимые для их формирования, печеночные метастазы уменьшались, а опухоли становились менее агрессивными. Истощение нейтрофилов давало схожий защитный эффект, указывая на парадокс: иммунный ответ, направленный на борьбу с инфекцией, был захвачен в помощь распространению рака.
От электрических сигналов к генным переключателям
Как липкие ДНК‑сети вне клетки могут изменить процессы глубоко внутри её ядра? Ответ оказался в кальции — простом ионе, выполняющем функцию электрического сигнала в клетках. В исследовании показано, что нейтрофильные сети повышали уровень канального белка TRPC1 на колоректальных раковых клетках. TRPC1 позволял дополнительному кальцию вливаться в клетку, что активировало кальций‑чувствительный регулятор NFATC3 и создавало самоусиливающийся цикл, поддерживавший высокий уровень TRPC1. Этот всплеск кальция способствовал тому, что две мелкие белковые молекулы, S100A8 и S100A9, сцеплялись между собой и затем связывались с важным регулятором роста STAT3. Тройка перемещалась в ядро, где совершала особенно заметное действие: помогала изгибать и формировать петли ДНК, так что отдалённые регуляторные участки и места начала транскрипции оказывались в физическом контакте, стабилизируя «энхансер–промоторные петли», усиливающие экспрессию определённых генов.
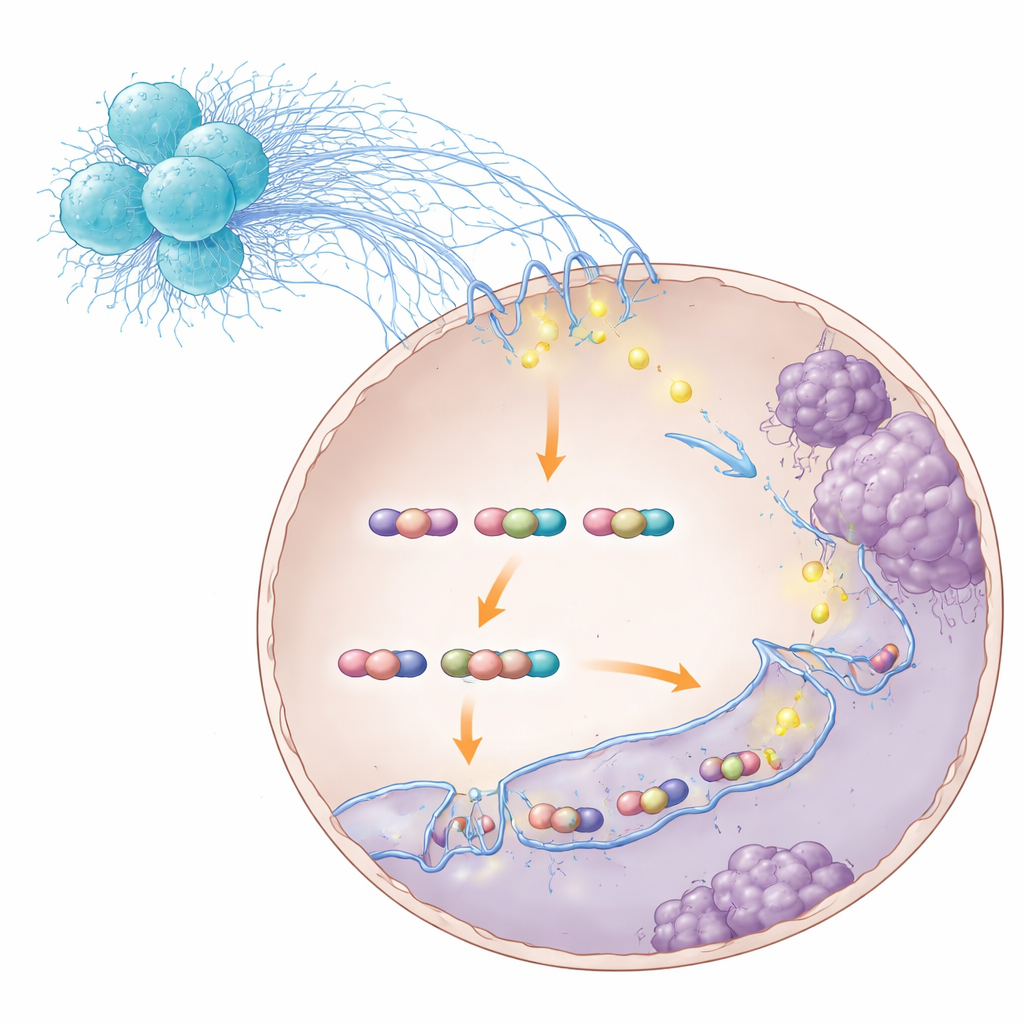
Перепрограммирование раковых клеток для метастазирования
Картируя трёхмерные контакты вдоль генома, исследователи обнаружили, что комплекс STAT3–S100A8/9 способствовал формированию петель, благоприятствовавших генам, вовлечённым в подвижность и инвазию клеток. Одним из ключевых генов оказался TNS1, который побуждает клетки ослаблять прикрепления и легче мигрировать. При разрушении комплекса STAT3–S100A8/9 многие такие петли ослабевали или исчезали, уровень TNS1 падал, и клетки теряли часть способности к инвазии и посеву в печени. Важно, что это вмешательство не прекращало вообще взаимодействие STAT3 с ДНК — оно специфически дестабилизировало петлевую архитектуру, которая гипервключала программы метастазирования. В модельных экспериментах блокирование разных звеньев этой цепочки — от бактериального сенсора RIPK2 в нейтрофилах до S100A8/9 и самого STAT3 — снижало печёночные метастазы и улучшало выживаемость.
Разрывая цепочку между микробами и опухолями
Для неспециалистов ключевая мысль такова: обычная кишечная бактерия может помогать колоректальному раку распространяться, сначала вызывая у иммунных клеток выброс ДНК‑сетей, а затем используя эти сети для запуска кальциево‑зависимой цепочки, которая перепрограммирует включение онкогенных генов. Вместо широкого применения антибиотиков, что может повредить полезную микрофлору и ослабить противораковую иммунотерапию, работа указывает на более точные лекарственные цели: бактериальные сенсоры вроде RIPK2, каскад TRPC1–кальций–S100A8/9 и STAT3‑опосредованные петли ДНК, которые фиксируют гены, связанные с метастазированием, в состоянии повышенной активности. Прерывание этой цепочки на одном или нескольких уровнях может предоставить новую стратегию, чтобы не дать колоректальному раку превратиться из локальной проблемы в кишечнике в смертельное заболевание печени.
Цитирование: Pan, B., Yao, Y., Zhang, Z. et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nat Commun 17, 2290 (2026). https://doi.org/10.1038/s41467-026-69005-y
Ключевые слова: метастазирование колоректального рака, микробиота кишечника, внеклеточные ловушки нейтрофилов, сигнальный путь STAT3, эпигенетическая регуляция генов