Clear Sky Science · ru
Дизайн ковалентных ингибиторов обеспечивает активность против форм KRAS G12C, связанных как с GDP, так и с GTP
Почему это важно для будущих методов лечения рака
Раковые заболевания, вызванные мутациями в гене KRAS, долгое время считались одними из самых трудных для лечения. В последнее время новые препараты, блокирующие одну распространённую мутантную форму — KRAS G12C, — дошли до пациентов и начали менять эту картину. В этой работе исследуется более амбициозная идея: можно ли сконструировать лекарства, которые блокируют KRAS G12C в двух основных рабочих режимах внутри клетки, и будет ли это делать лечение рака более быстрым, эффективным или долговременным?
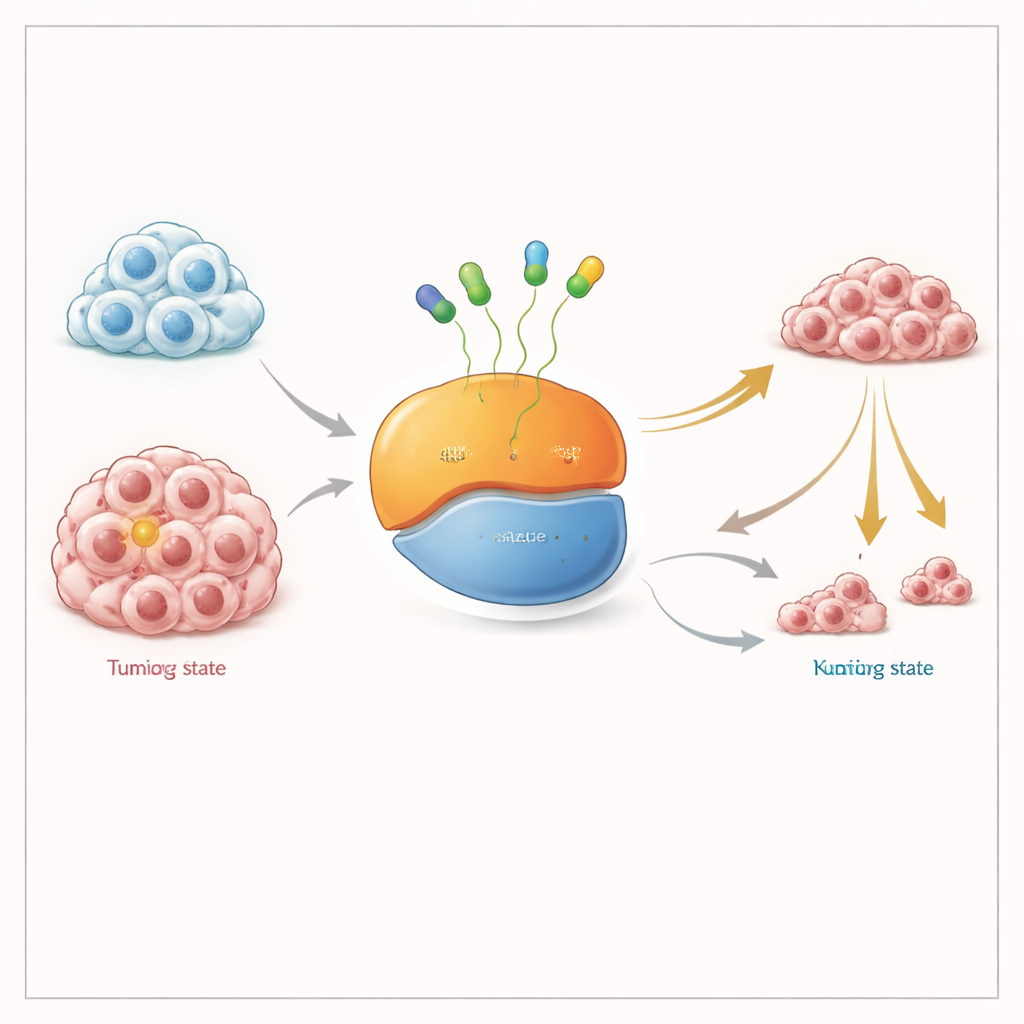
Выключение молекулярного переключателя в двух положениях
KRAS действует как крошечный выключатель сигналов роста клетки. Он переливается между «выключенным» состоянием, в котором связан с одной энергетической молекулой (GDP), и «включённым» состоянием, когда он связан с другой (GTP). Мутация KRAS G12C держит этот переключатель частично включённым и подпитывает рост опухоли. Существующие препараты, одобренные FDA, цепляются за «выключенную» форму и закрепляют её; со временем, по мере того как большее число молекул KRAS проходит через это состояние, общий пул мутантного белка становится неактивным. Многие учёные полагают, что препарат, способный захватывать KRAS в обеих формах — включённой и выключенной, — должен работать лучше, особенно в опухолях, которые адаптируются, удерживая больше KRAS в активном состоянии.
Проектирование нового типа молекулярного крючка
Авторы поставили цель создать такие универсальные препараты. Они сосредоточились на небольшой бороздке рядом с гибкой областью KRAS, называемой Switch II, где уже связываются существующие лекарства. Вместо того чтобы менять силу взаимодействия молекул с этой бороздкой, они переработали «ударную» часть молекулы (warhead), которая образует прочную ковалентную связь с мутантной цистеином в позиции 12. С помощью компьютерного моделирования и синтеза десятков вариантов они обнаружили особую трёхкомпонентную ударную группу, которая подходит к цистеину под немного иным углом. Это тонкое смещение создаёт достаточно места для более громоздкой молекулы GTP, позволяя новым соединениям связываться с KRAS как в форме с GDP, так и с GTP. Биохимические тесты подтвердили, что ведущие соединения могут нарушать взаимодействие KRAS с ключевым сигнальным партнёром RAF в обоих состояниях.
Наблюдение за перестройкой белка
Чтобы понять, почему эти молекулы работают, команда определила кристаллические структуры высокого разрешения комплекса препарата с KRAS. Эти снимки показали, что новая ударная группа реагирует в необычном участке химического скелета, отщепляя атом фтора и образуя ковалентную связь на другом атоме углерода, чем это обычно наблюдается у противораковых препаратов, нацеленных на цистеин. Эта изменённая химия помогает препарату помещаться в карман Switch II даже при наличии GTP. Структуры также показали, что при связывании ингибитор смещает маленькую молекулу воды и тонко перестраивает другую петлю, Switch I, которая обычно контактирует с белками нижестоящей сигнальной цепи. Эта аллостерическая перестройка сближает две аминокислоты, формируя плотный солевой мост, и деформирует поверхность так, что RAF больше не может прикрепляться и передавать сигналы роста.
Быстрое выключение, но без более сильного долгосрочного эффекта
Опиравшись на эти структурные данные, исследователи оптимизировали два ведущих соединения, которые эффективно и селективно цепляются за KRAS G12C, при этом в значительной степени не затрагивая другие белки с цистеинами. В клеточных линиях рака эти ингибиторы двух состояний быстро блокировали ключевой сигнальный каскад, известный как путь MAPK, что наблюдали по исчезновению химической метки на белке ERK и сильному подавлению роста клеток. Они инактивировали KRAS в клетках быстрее, чем эталонный препарат, нацеленный только на неактивное состояние. В моделях опухолей у мышей одно из ведущих соединений показало хорошую пероральную доступность, быстро образовывало ковалентные связи с мишенью и уменьшало опухоли или замедляло их рост. Тем не менее, при сравнении ингибиторов двух состояний и препаратов, нацеленных на неактивное состояние, на более длинных временных интервалах оба класса в конечном итоге достигали схожих уровней блокировки KRAS, ингибирования пути и контроля опухоли.
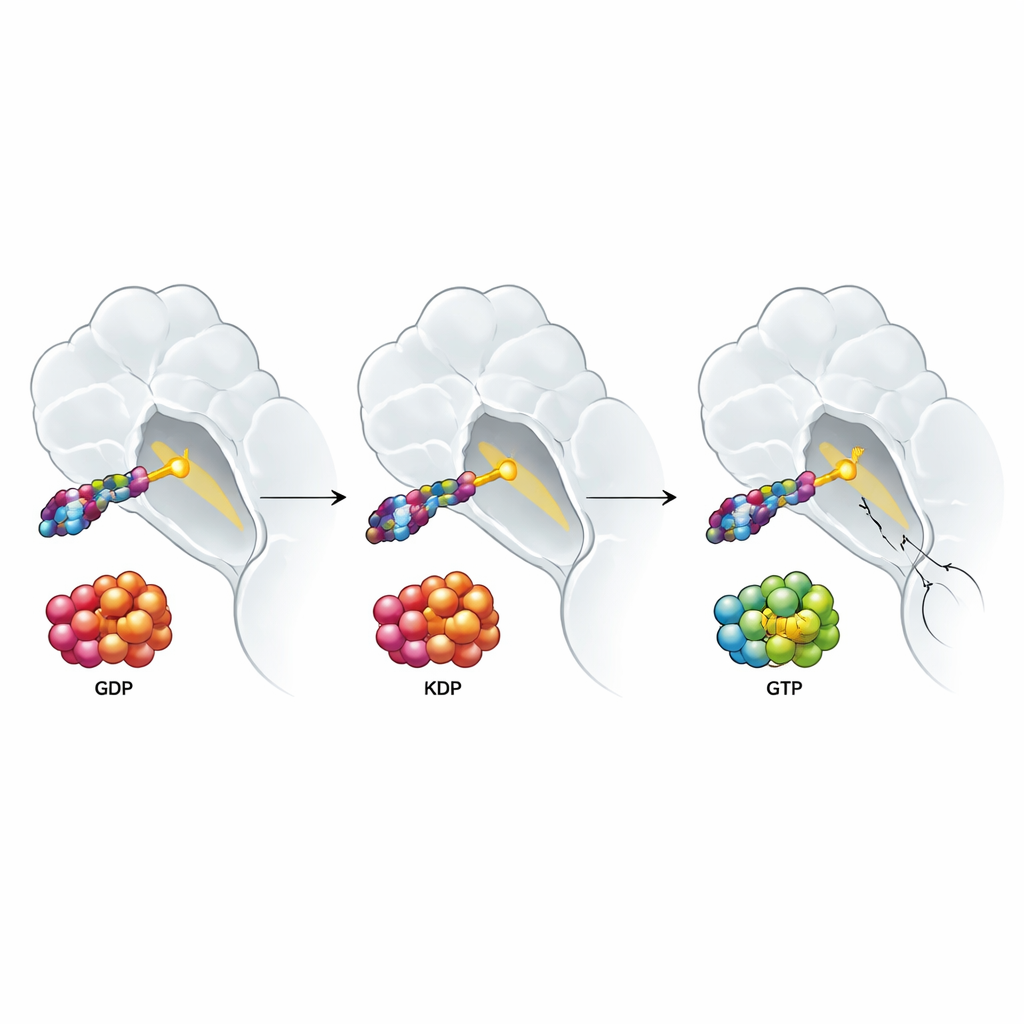
Почему сигналы роста из окружающей опухоль среды всё же побеждают
Исследование также рассмотрело, как сигналы из микроокружения опухоли влияют на эффективность этих препаратов. Факторы роста, такие как EGF и HGF, которые часто присутствуют вокруг многих опухолей, сдвигают белки RAS в активную форму с GTP и известны тем, что уменьшают чувствительность к таргетным терапиям. Можно было бы ожидать, что препарат, связывающий активную форму KRAS G12C, обойдёт эту проблему. Вместо этого авторы обнаружили, что и ингибиторы двух состояний, и препараты, нацеленные на неактивное состояние, теряли силу при наличии таких факторов роста. Подробные эксперименты указали на неожиданный виновник: активация нормальных, немутированных форм RAS (H‑RAS и N‑RAS), которые могут обходить KRAS G12C и поддерживать передачу сигнала роста. Когда исследователи удалили H‑RAS и N‑RAS в клеточной линии рака лёгкого, вызванная факторами роста резистентность в значительной степени исчезла для всех типов препаратов, нацеленных на KRAS G12C, тогда как препарат, блокирующий более нижестоящий шаг пути, изначально был менее подвержен этому эффекту.
Что это значит для пациентов и разработки лекарств
В целом работа демонстрирует, что химически и структурно выполнимо создать ковалентные препараты против KRAS G12C, которые захватывают белок как в активном, так и в неактивном состояниях, и что эти ингибиторы двух состояний способны быстрее выключать сигнализацию по сравнению с существующими средствами. Однако быстрое взаимодействие не привело к явно лучшему контролю опухоли или к решению проблемы резистентности, вызванной факторами роста, в доклинических моделях. Для пациентов это означает, что просто добавление активности против активной формы KRAS может быть недостаточным; могут потребоваться комбинационные стратегии, которые также учитывают другие члены семейства RAS или узлы нижестоящей сигнализации. Тем не менее новая ударная группа и представленная здесь структурная схема расширяют набор инструментов для нацеливания на KRAS и будут информировать будущие поколения прецизионных противораковых терапий.
Цитирование: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
Ключевые слова: KRAS G12C, ковалентный ингибитор, ингибиция двух состояний, MAPK-сигнализация, лекарственная устойчивость