Clear Sky Science · ru
Молекулярно определённая базало‑префронтально‑таламическая цепь регулирует сенсорные и аффективные составляющие боли у самцов мышей
Почему эта мозговая цепь важна для боли
Боль — это не только резкая колкость или тупая ноющая чувствительность; она также несёт эмоциональную нагрузку и способна изменять настроение и поведение на годы. Многие пациенты с хронической болью мало выигрывают от существующих препаратов и часто сталкиваются с серьёзными побочными эффектами. Это исследование на самцах мышей выявляет точно очерченную мозговую цепь, которая позволяет мозгу усиливать или ослаблять боль как по силе восприятия, так и по степени неприятности. Картирование и управление этим путём указывают на новые, более прицельные подходы к облегчению хронической боли без единственной опоры на традиционные анальгетики.
Скрытое шоссе от «мыслительного» мозга к узлу боли
Исследователи сосредоточились на медиальной префронтальной коре — лобной области мозга, участвующей в принятии решений, эмоциях и контроле боли, — и на таламусе, глубоком релейном центре, формирующем интенсивность и неприятность боли. Они обнаружили, что определённая группа клеток в медиальной префронтальной коре, помеченная геном Foxp2, образует крупный выходной путь к таламусу. Эти клетки локализованы преимущественно в самой глубокой корковой слое и посылают длинные волокна в отдельные таламические ядра, при этом в значительной мере игнорируя другие типичные цели префронтальной коры. С помощью методов трассировки и картирования всего мозга команда показала, что нейроны, помеченные Foxp2, тесно связаны с тремя таламическими областями, известными своим влиянием на обработку боли: паратенциальным ядром, медиодорсальным таламусом и вентромедиальным таламусом. 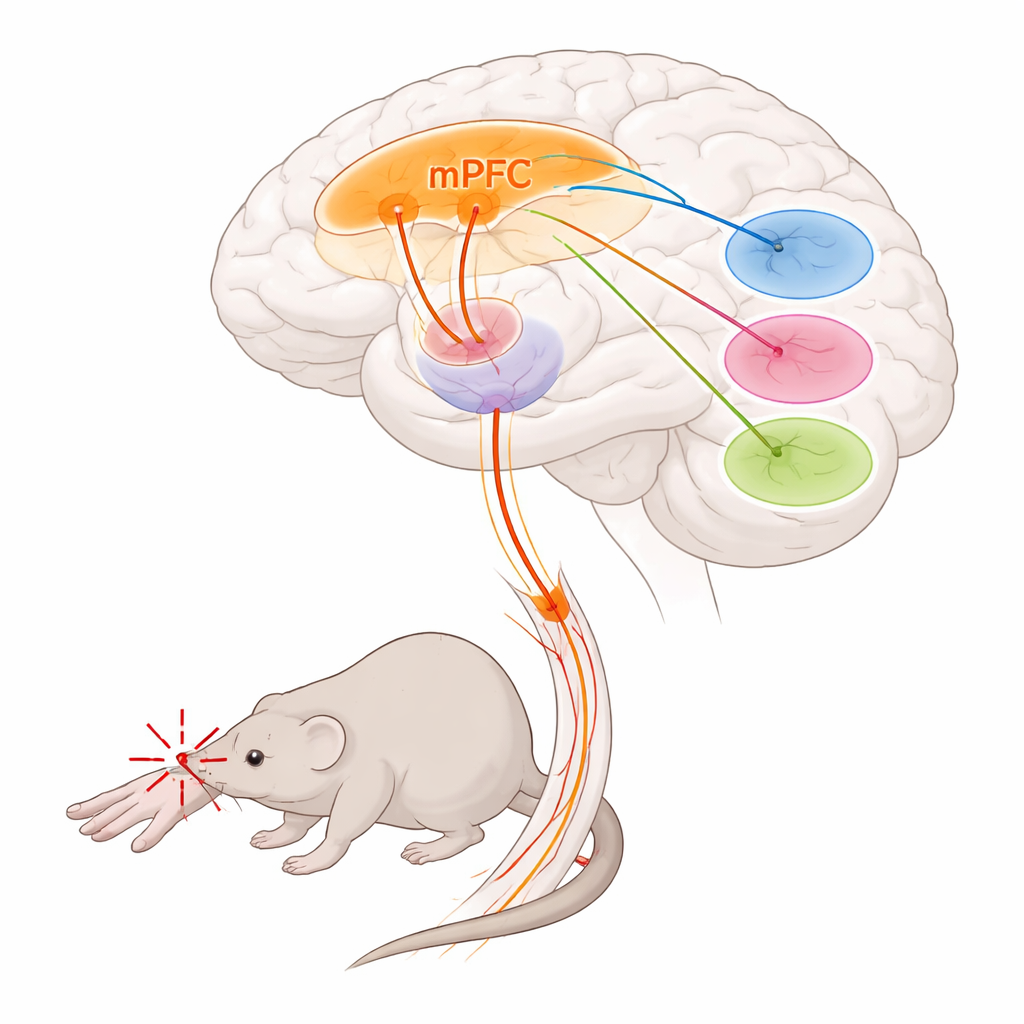
Когда возникает боль, ключевой центр управления «замолкает»
Чтобы узнать, как этот путь ведёт себя во время боли, учёные имплантировали крошечные линзы над медиальной префронтальной корой и регистрировали активность отдельных нейронов, помеченных Foxp2, у бодрствующих мышей. Во время кратковременных механических защипов, химической боли, вызванной формалином, и длительной воспалительной боли эти клетки последовательно снижали активность: большинство демонстрировало меньше всплесков активности во время болевых эпизодов и в последующие дни после воспалительной травмы. Это подавление было выраженным; в некоторых условиях более трети и даже почти половина клеток становились значительно менее активными. Полученные данные указывают на то, что острые и хронические болевые состояния частично могут отражать «выключение» естественной префронтальной тормозящей системы, которая в ином случае помогала бы держать боль под контролем.
Включение и выключение цепи меняет опыт боли
Далее команда спросила, является ли это притихание лишь побочным эффектом боли или её причиной. С помощью генетических инструментов они либо длительно блокировали выход нейронов, помеченных Foxp2, либо кратковременно усиливали их активность. Постоянная инактивация делала мышей более чувствительными к прикосновениям и теплу, что указывает на то, что этот путь обычно сдерживает входящие болевые сигналы. Напротив, кратковременная активация повышала порог болезненных стимулов, уменьшала количество лизаний в поздней фазе теста с формалином (показатель продолжающейся воспалительной боли) и заставляла мышей предпочитать окружения, где цепь была включена, сигнализируя об облегчении эмоционального бремени боли. Подсвечивая конкретные ветви пути, исследователи показали, что проекции к паратенциальному таламусу уменьшают и физическую чувствительность, и реактивные копинговые ответы, тогда как проекции к медиодорсальному и вентромедиальному таламусу в основном настраивают эмоциональные и поведенческие аспекты. В совокупности результаты раскрывают тонко разделённую схему проводки, в которой разные ветви одной и той же префронтальной популяции контролируют различные грани переживания боли.
Химическая настройка: холинергическое усиление ради облегчения боли
Что регулирует эти префронтальные нейроны, приносящие облегчение от боли? Эксперименты по трассировке выявили сильные входы из холинергической области базального мозга, называемой горизонтальной диагональной полосой. Многие клетки, посылающие сигналы из этой области на нейроны, помеченные Foxp2, используют ацетилхолин — нейромедиатор, участвующий во внимании и бодрствовании. Активация этой холинергической проекции снижала механическую чувствительность и копинговые реакции и смягчала воспалительную гиперчувствительность, хотя явно не смещала негативный эмоциональный тон боли. На приёмной стороне нейроны, помеченные Foxp2, оказались обогащены определённым типом рецепторов к ацетилхолину, известным как α4β2-никотиновый рецептор. Прямое введение селективного агониста α4β2 в медиальную префронтальную кору делало мышей менее чувствительными к болезненному теплу и прикосновениям, даже в условиях хронического воспаления, и усиливало активность нейронов, помеченных Foxp2. Блокирование этих нейронов устраняло полезный эффект препарата, показывая, что этот рецептор облегчает боль именно за счёт возбуждения этого типа клеток. 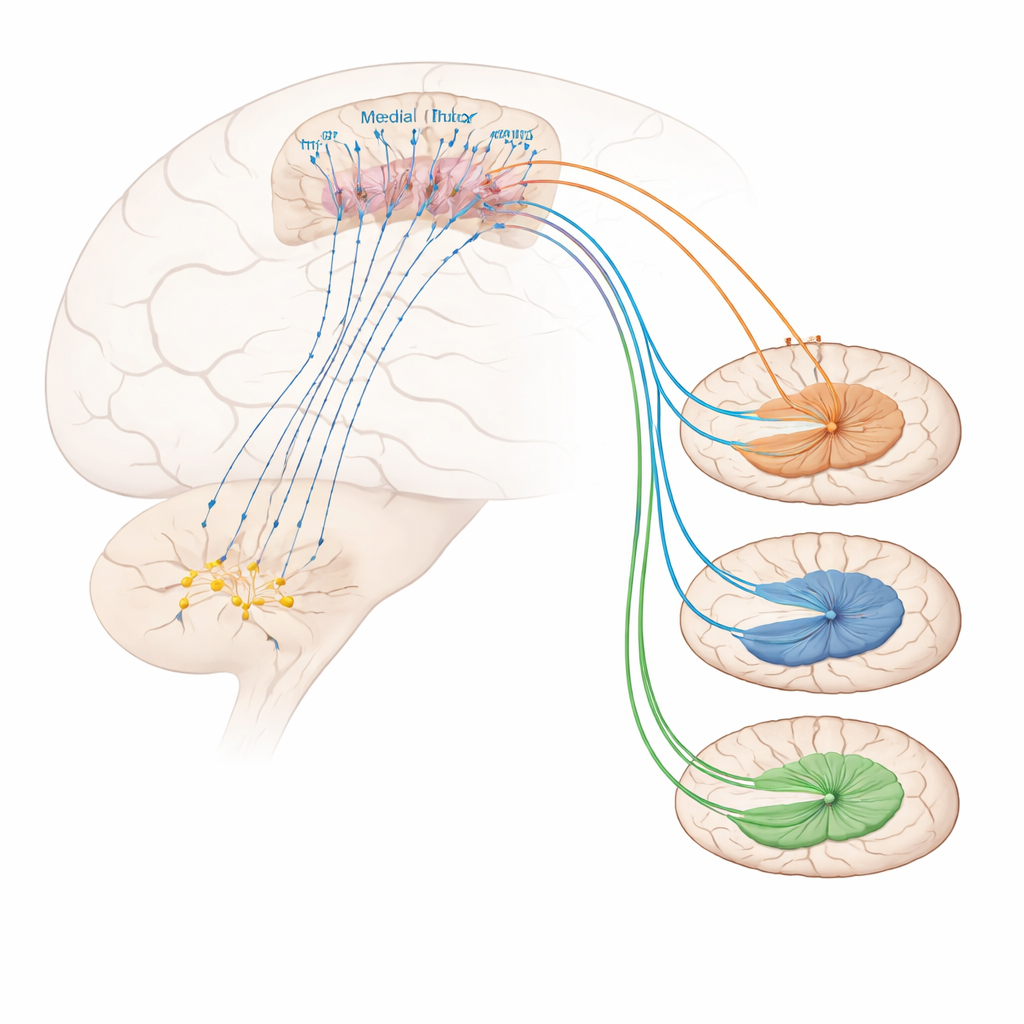
Что это значит для будущего лечения боли
Проще говоря, исследование выделяет точную трёхступенчатую схему: холинергическую «запускающую» область в базальном мозге, специализированный набор контрольных клеток в медиальной префронтальной коре и отдельные релейные узлы в таламусе, которые по‑отдельности управляют тем, насколько сильно болит, насколько это плохо эмоционально и как мы на это реагируем. Похоже, что боль выключает эту цепь; её реактивация, либо прямой стимуляцией, либо воздействием на ацетилхолиновые рецепторы, уменьшает и физическую остроту, и эмоциональное страдание от воспалительной боли у самцов мышей. Хотя многое ещё предстоит сделать, чтобы перенести эти выводы на человека и на другие формы хронической боли, результаты подчёркивают многообещающую стратегию: вместо притупления всех ощущений будущие лечения могут восстанавливать или тонко настраивать собственные антиболевые цепи мозга для более эффективной и, возможно, более безопасной долгосрочной терапии.
Цитирование: Xie, G., Liu, Y., Qi, X. et al. A molecularly defined basalo-prefrontal-thalamic circuit regulates sensory and affective dimensions of pain in male mice. Nat Commun 17, 2134 (2026). https://doi.org/10.1038/s41467-026-69001-2
Ключевые слова: хроническая боль, медиальная префронтальная кора, таламус, холинергическая сигнализация, никотиновые рецепторы