Clear Sky Science · ru
Ковалентная модификация глутаминовой кислоты по мотивам технологии HaloTag
Преобразование «якорей» белков в лекарственные мишени
Многие современные противораковые препараты действуют, прикрепляясь к белкам внутри клеток. Но у некоторых из важнейших белков нет очевидных «ручек», за которые могли бы зацепиться лекарства. В этом исследовании предложен хитрый химический приём, вдохновлённый популярным лабораторным инструментом HaloTag, который позволяет захватить обычно труднодоступное место на белке, контролирующее сигналы, связанные с ростом и раком. Работа может открыть новые пути разработки препаратов, способных более надёжно блокировать опухолевые пути передачи сигналов.
Почему большинство ковалентных лекарств нацелены на одно и то же место
В последние годы так называемые таргетные ковалентные препараты стали захватывающим классом средств. Они содержат умеренно реактивную химическую группу, которая образует прочную связь с конкретной аминокислотой белка, фиксируя лекарство на месте. Практически все такие препараты нацелены на цистеин — относительно редкую, но очень реактивную аминокислоту. Для сравнения, две другие аминокислоты — аспартат и глутамат — гораздо более распространены и часто критичны для формы и функции белка, но их кислотные карбоксилатные группы значительно менее реактивны в водной среде клетки. Это затрудняет их селективную модификацию, и до этой работы существовало лишь несколько удачных примеров ковалентных препаратов, нацеленных на глутамат или аспартат.
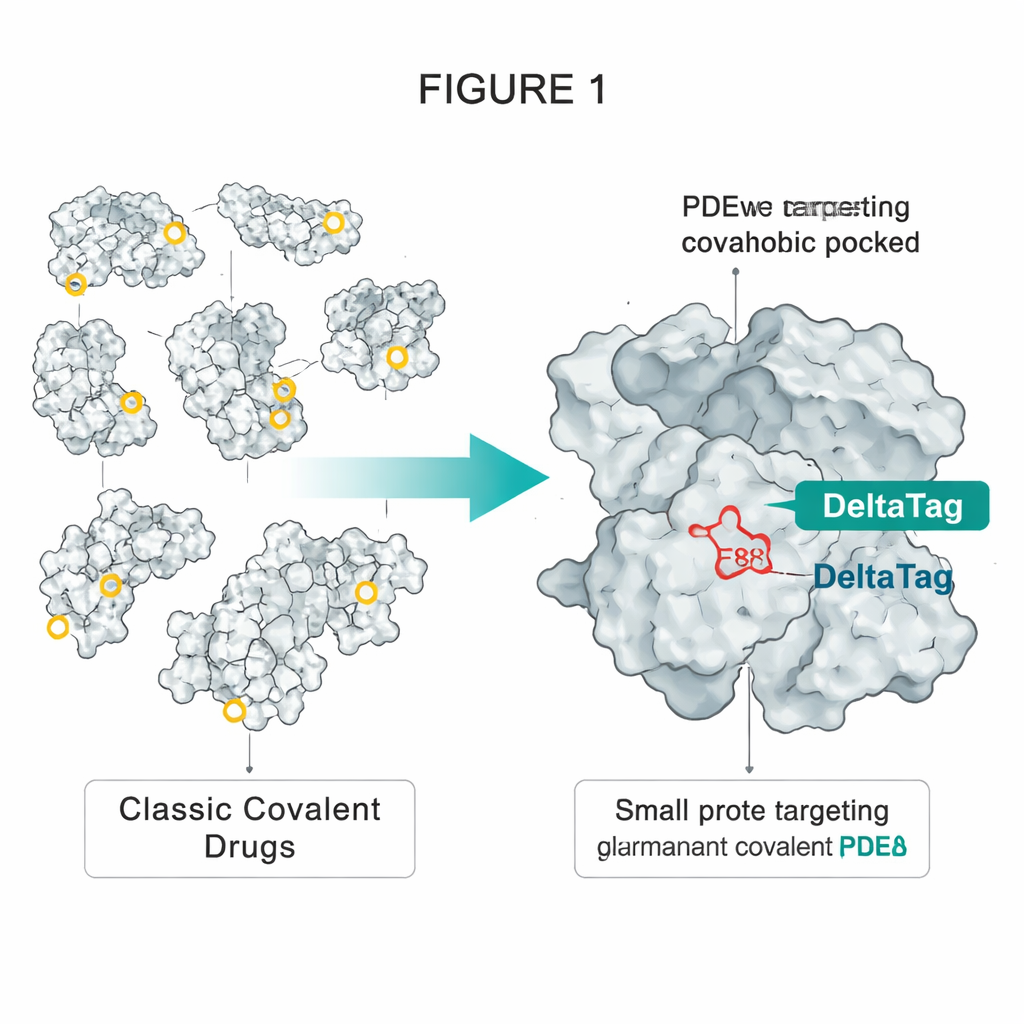
Заимствование приёма у технологии HaloTag
Авторы вдохновились HaloTag — широко используемым инженерным белком, который можно постоянно метить флуоресцентными красителями. В HaloTag специально расположенный аспартат глубоко в гидрофобном кармане реагирует с простым хлоралкановым хвостом красителя, образуя стабильную эфирную связь. Исследователи заметили, что другой белок, PDEδ, имеет сходный гидрофобный карман, содержащий одну доступную глутаминовую кислоту, обозначенную как E88. PDEδ переносит липофильные сигнальные белки, такие как малый GTPase Rheb, по клетке, помогая им достигать мембран, где активируются комплекс mTORC1 и другие ростоподдерживающие комплексы. Ранние нереверсивные ингибиторы PDEδ могли блокировать этот «шаттл», но их эффект был ограничен, потому что другой белок, Arl2, со временем мог вытеснять их из кармана.
Проектирование DeltaTag для связывания с глутаматом
Чтобы преодолеть проблему «выдавливания», исследователи взяли за отправную точку известный блокатор PDEδ с высокой сродственностью и перестроили один из его боковых фрагментов, добавив галоалкановую «боеголовку», похожую на те, что используются в лигандах HaloTag. После нескольких раундов структурной оптимизации, руководимых данными рентгеноструктур белка, они получили соединение под названием DeltaTag. Его ключевая особенность — фенэтилбромидная группа, расположенная так, что когда молекула занимает липидный карман PDEδ, бромид точно выровнен для реакции с E88. Биофизические измерения и данные высокоразрешающей рентгеноструктуры подтвердили, что DeltaTag образует ковалентную эфирную связь специфически с этой глутаминовой кислотой, а другие потенциально более реактивные аминокислоты в PDEδ остаются нетронутыми. Соединение достаточно реактивно, чтобы эффективно метить белок, но достаточно стабильно в воде и в присутствии основного сульфурного антиоксиданта клетки — глутатиона, чтобы избегать широкомасштабного неселективного повреждения.
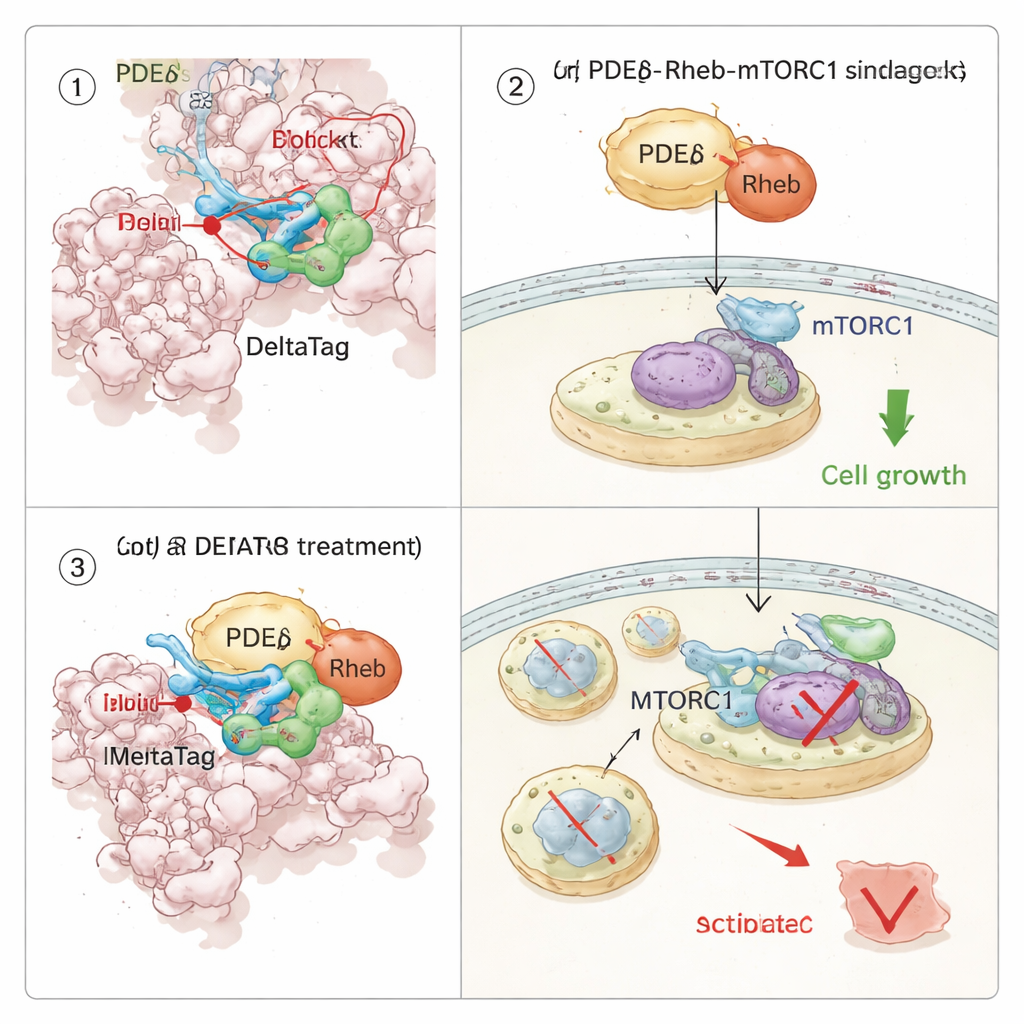
Перепрограммирование пути роста внутри раковых клеток
Поскольку PDEδ штурмует Rheb, а Rheb, в свою очередь, включает сигнальный путь mTORC1, команда изучила, как ковалентная ингибиция PDEδ повлияет на клеточную сигнализацию. С помощью профилирования термостабильности тысяч белков они показали, что DeltaTag селективно связывается с PDEδ в клеточных экстрактах и нарушает белки, связанные с осью Rheb–mTOR. В экспериментах по визуализации живых клеток DeltaTag вызывал перераспределение Rheb от рассеянного локуса в цитоплазме к более кластеризованным внутренним мембранам, что согласуется с нарушением его нормального транспорта. Глобальный фосфопротеомный анализ и целевые Western-блот‑исследования показали, что активность mTORC1, отслеживаемая фосфорилированием рибосомального белка S6, со временем снижалась, в то время как компенсаторные сигналы в родственных путях возрастали. Важно, что в нескольких линиях человеческих раковых клеток, зависимых от мутантного KRAS и сильного сигнала mTOR, DeltaTag замедлял пролиферацию эффективнее, чем близкие по структуре обратимые ингибиторы, и его эффект был слабее в клетках без PDEδ, что поддерживает вывод о его on‑target действии.
Открытие двери для новых типов лекарственных мишеней
Эта работа демонстрирует, что возможно создать малые молекулы, образующие постоянную, высокоспецифичную связь с одной глутаминовой кислотой, спрятанной в гидрофобном кармане белка, используя относительно простую галоалкановую химию, заимствованную у HaloTag. На примере PDEδ такая ковалентная связь даёт более долговременную блокаду релевантного для рака пути роста по сравнению с ранними обратимыми препаратами. В более широком смысле ту же логику дизайна можно применить к другим белкам с гидрофобными полостями, но без привычных «реактивных» аминокислот, при условии наличия стратегически расположенного глутамата или аспартата. При дальнейшем улучшении ковалентные ингибиторы, нацеленные на глутамат, подобные DeltaTag, могут стать полезными инструментами химической биологии и, в конечном счёте, кандидатами для разработки новых терапий против трудно поддающихся лечению белков.
Цитирование: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
Ключевые слова: ковалентные ингибиторы, таргетирование глутамата, PDEδ, сигналинг mTOR, разработка противораковых препаратов