Clear Sky Science · ru
Создание синтетических клеток с внутримембранными доменами, обладающими разными асимметриями билипидного слоя
Почему важны крошечные синтетические пузырьки
Каждая живая клетка окружена мембраной, которая ведёт себя как умная, гибкая «кожа». Эта кожа не однородна: внутренняя и внешняя стороны, а также разные участки по поверхности могут существенно различаться по составу и форме. Эти различия помогают клеткам передавать сигналы, связывать белки и даже делиться. Тем не менее чрезвычайно сложно создать простые управляемые модельные мембраны, которые воспроизводят эту сложность. В этом исследовании предложен практичный способ получения клеткоразмерных «синтетических клеток», чьи мембраны асимметричны по обоим слоям и латерально разбиты на отдельные области — что открывает путь к более реалистичным имитаторам клеток и к изучению того, как узоры на мембране приводят к выбуханию и делению. 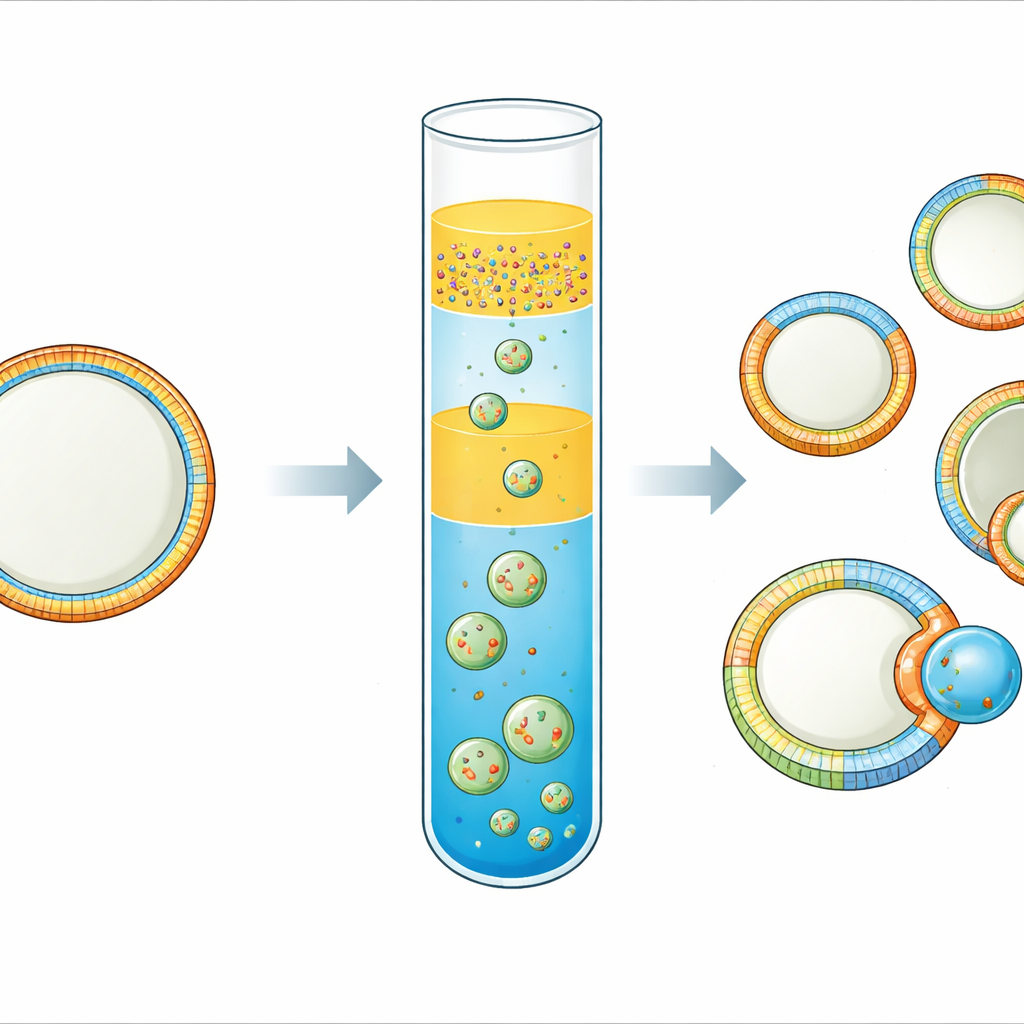
Создание лучших имитаций клетки
Реальные клеточные мембраны асимметричны: внутренняя сторона богата отрицательно заряженными липидами, которые привлекают сигнальные белки, тогда как внешняя сторона несёт другие липиды, обеспечивающие распознавание между клетками. Многие лабораторные методы позволяют получать гигантские везикулы — полые сферы из жироподобных молекул — но их два листка обычно оказываются одинаковыми, а доступ к внутренности затруднён. Другие подходы, создающие асимметрию, часто требуют сложного оборудования, специальных липидов или приводят к тому, что везикулы прочно прилипают к поверхности. Авторы поставили цель создать свободно плавающие, клеткоразмерные везикулы, которые сочетают высокую инкапсуляцию биомолекул с устойчивой, настраиваемой асимметрией, более похожей на живую клетку.
Трёхслойный рецепт для асимметричных мембран
Команда усовершенствовала технику «перевёрнутой эмульсии», при которой маленькие водные капли, покрытые липидами, продавливаются через масляно-водный интерфейс и формируют везикулы. Ключевое новшество — установка с тройным слоем масла. Внизу находится масло, содержащее липиды, предназначенные для внешнего листка мембраны. Над ним размещён тонкий промежуточный слой масла без липидов, а сверху — эмульсия водных капель в масле, содержащем липиды для внутреннего листка. Во время кратковременной центрифугирования капли проходят через промежуточный и нижний слои, захватывая вторую липидную оболочку и закрываясь в везикулы. Подбор двух масел разной плотности и наличие промежуточного слоя резко ограничивают смешивание между пулами липидов, так что внутренний и внешний листки сохраняют разные составы.
Проверка, что две стороны остаются разными
Чтобы убедиться в реальной разности листков, исследователи использовали как химические, так и белковые индикаторы. В одном наборе испытаний они добавляли флуоресцентный липид только в один листок, а затем подвергали везикулы действию в растворенной снаружи химии, которая тушит флуоресценцию, но не может пересечь мембрану. Когда флуоресцентный липид был снаружи, сигнал почти полностью исчезал; когда он находился внутри, сигнал почти не менялся, что показало, что большинство меченых липидов оставалось на месте. Во втором наборе экспериментов они помещали липиды, связывающие специфические белки — например, биотинилированные липиды для стрептавидина или особые головные группы для His‑маркера зеленого флуоресцентного белка — только в один листок. Белки, добавленные в противоположный компартмент (внутри или снаружи), связывались лишь тогда, когда соответствующий липид находился на той же стороне мембраны, что подтвердило сильную асимметрию и сохранённую функцию белков.
Создание «раптов» и наблюдение за выбуханием мембран
Реальные клеточные мембраны также содержат «рапты» — крошечные участки, обогащённые определёнными липидами, такими как холестерин и сфингомиелин, которые могут собирать белки и влиять на форму. Достижение такого фазового разделения при методе перевёрнутой эмульсии было затруднено тем, что холестерин склонен оставаться растворённым в масле, а не входить в мембрану. Используя сквален в нижнем масляном слое, который удерживает холестерин слабее, чем стандартное минеральное масло, авторы смогли устойчиво получать везикулы с мембранами, разделяющимися на сосуществующие жидко‑упорядоченные и жидко‑неупорядоченные области, подобно раптам. Затем они объединили эту латеральную структуру с асимметрией листков: один домен нёс внутри лиганды во внутреннем листке, связывающие стрептавидин, а другой домен на внешней стороне нёс гликолипиды, связывающие токсин холеры. 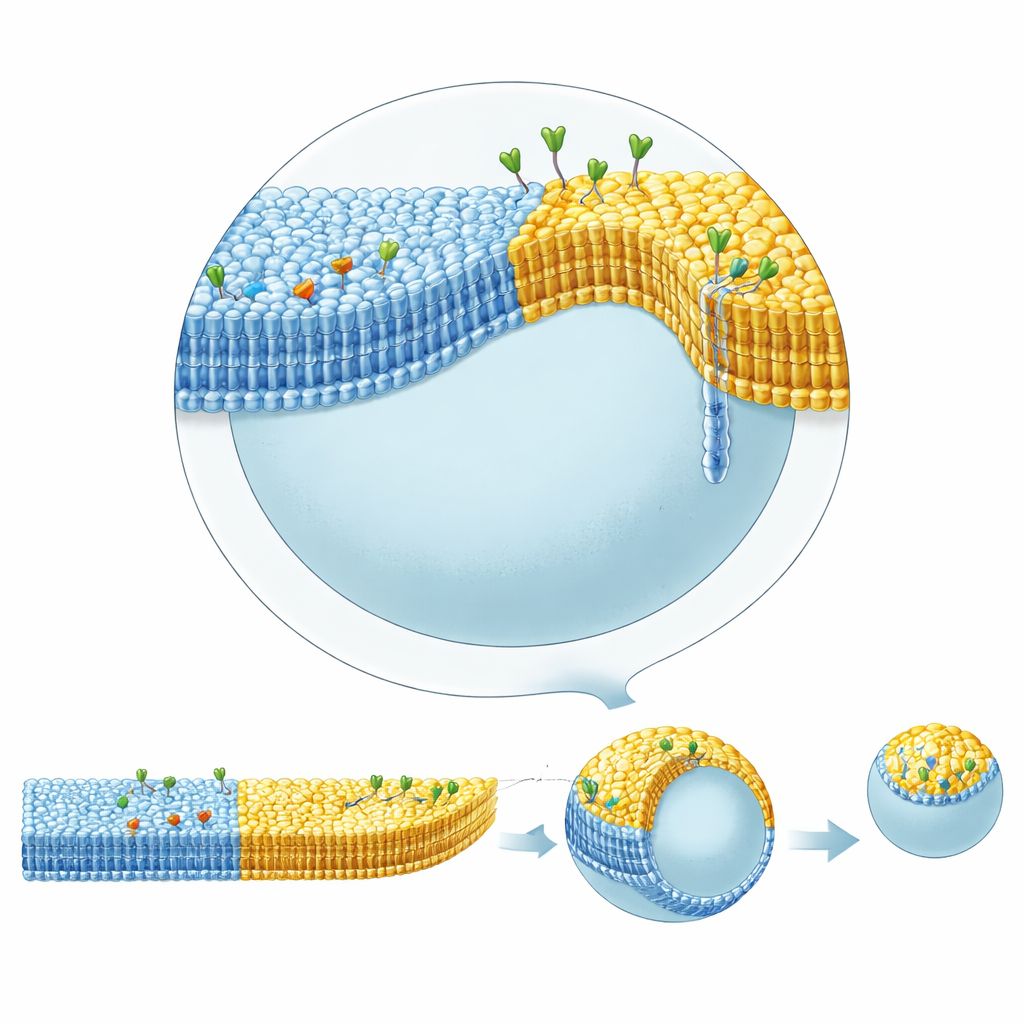
Как белки и узоры управляют изменением формы
Эти сложные везикулы демонстрировали впечатляющую динамику форм. Когда токсин холеры связывался с гликолипидами в упорядоченном домене снаружи, этот домен выпячивался наружу в изогнутую бутоноподобную структуру, соединённую узкой шейкой, и при лёгком осмотическом обезвоживании мог полностью отщепляться в виде дочернего везикула. Это выбухание не требовало молекул, несущих энергию, таких как АТФ, или специализированного делительного оборудования — оно возникало только из взаимодействия состава липидов, границ доменов и асимметричного связывания белков. При увеличении количества связанного внутри стрептавидина в неупорядоченном домене команда могла противодействовать наружному выгибу упорядоченного домена и постепенно восстанавливать более сферическую форму. Детальный геометрический анализ контуров везикул показал, что кривизна мембраны скачкообразно меняется на границе между доменами, и что узкие шейки, образующиеся при выбухании, должны выдерживать силы по крайней мере в десятки пиконьютонов — что количественно характеризует, как структура доменов и уплотнение белков механически формуют мембраны.
Что это значит для будущих синтетических клеток
Проще говоря, авторы разработали рецепт для создания мягких, клеткоразмерных пузырьков, чьи «кожи» сегментированы и двусторонни почти так же, как у настоящих клеточных мембран. Поскольку метод относительно прост, работает с множеством различных липидов и позволяет захватывать внутри белки и другие крупные молекулы, он прокладывает путь к созданию более правдоподобных искусственных клеток снизу вверх. Такие синтетические клетки могут помочь учёным разложить по полочкам, как мембранные узоры контролируют сигнализацию, транспорт и деление, а в перспективе их можно будет использовать как умные носители лекарств, которые меняют форму или делятся по сигналу внутри организма.
Цитирование: Yandrapalli, N., Seemann, T., Lipowsky, R. et al. Engineering synthetic cells with intramembrane domains possessing distinct bilayer asymmetries. Nat Commun 17, 2620 (2026). https://doi.org/10.1038/s41467-026-68997-x
Ключевые слова: синтетические клетки, липидные мембраны, асимметрия мембраны, фазовое разделение, выбухание мембраны