Clear Sky Science · ru
Платформа нанодисков с вирусными гликопротоидами для аналитики вакцин
Преобразование вирусных белков в измеряемые мишени
Современные вакцины всё чаще опираются на точно сконструированные версии белков, покрывающих поверхность вирусов. Эти белки — главные мишени для защитных антител, но в своей естественной, связаной с мембраной форме их сложно изучать. В этой работе описана новая лабораторная платформа, помещающая полноразмерные вирусные поверхностные белки в крошечные плоские липидные частицы — нанодиски. Такая система позволяет учёным измерять, насколько хорошо кандидаты в вакцины имитируют настоящий вирус, как к ним прикрепляются антитела и как перестраивать вакцины для лучшей защиты.
Почему важно воссоздать вирусную поверхность
Многие ключевые вирусные белки прикреплены к жирной мембране, как и на реальном вирусе. Традиционные лабораторные подходы отрезают мембранную часть, чтобы упростить производство и очистку белков в растворе. Но этот упрощённый подход удаляет участки рядом с мембраной, где находятся особенно ценные мишени для антител, включая сегмент ВИЧ, известный как мембрано-близкая внешняя область (MPER). Эти близкомембранные участки могут выглядеть и функционировать иначе вне реалистичной липидной среды, поэтому растворимые фрагменты белков дают неполную или вводящую в заблуждение картину того, как вакцина поведёт себя в организме.
Создание универсальной платформы на основе нанодисков
Исследователи разработали оптимизированный пятидневный рабочий процесс: выделять полноразмерные вирусные поверхностные белки из человеческих клеток, сохранять их естественные мембранные сегменты и вновь вводить их в контролируемый липидный диск. Сначала они экспрессировали модифицированные гликопротеины ВИЧ и Эболы на поверхности клеток, затем аккуратно извлекали их детергентом и захватывали на матрице для очистки. Пока белки ещё были прикреплены, в смесь добавляли определённые липиды и поясоподобный белок-скелет, который самосборкой формировал небольшой дискообразный мембранный фрагмент. По мере удаления детергента вирусные белки оседали в эти нанодиски. Полученные препараты были очень чистыми, стабильными месяцами в холодильнике и несли гликаны (сахарные покрытия), близкие к тем, что наблюдаются на нативных вирусных шипах. 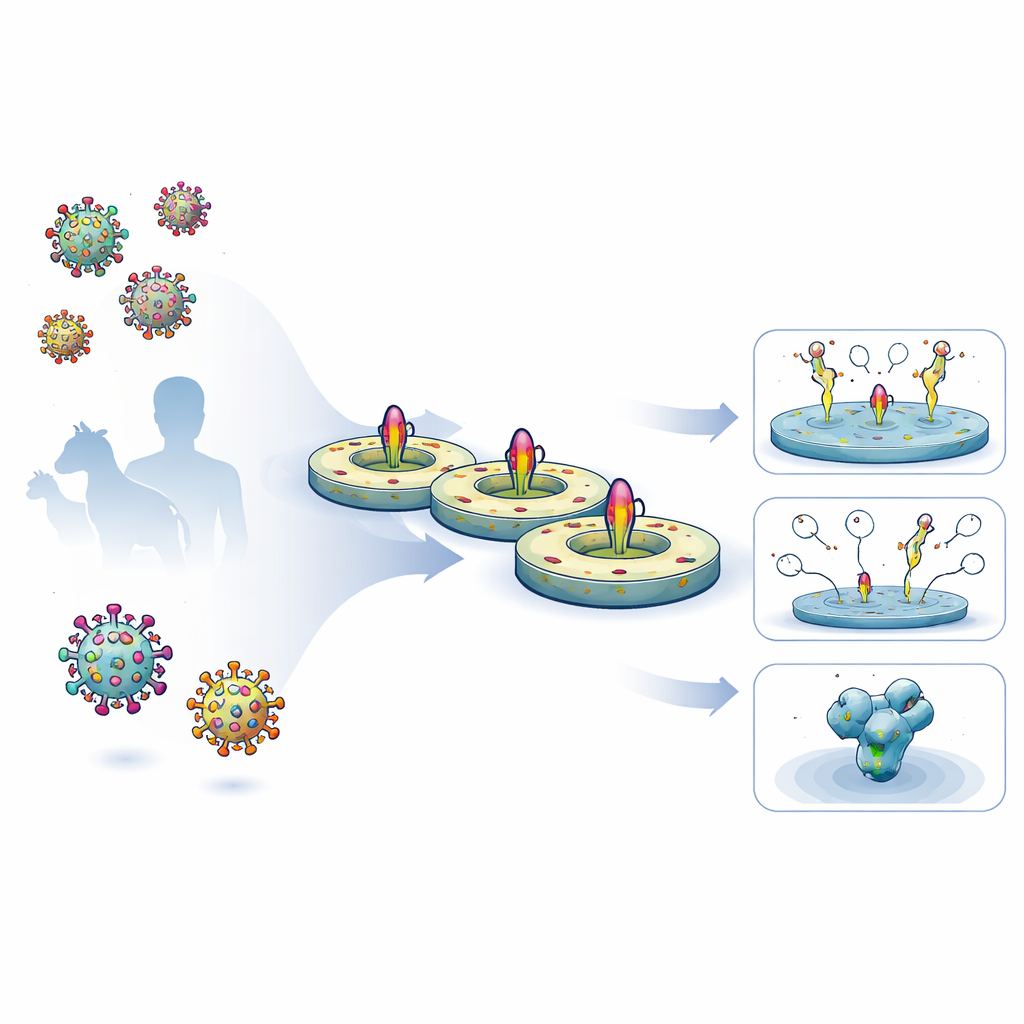
Измерение связывания антител и иммунных ответов
Имея белки, встроенные в нанодиски, команда проверила, насколько хорошо различные антитела связываются в нескольких конфигурациях поверхностного плазмонного резонанса (SPR) — методе отслеживания связи в реальном времени. Используя нанодиски ВИЧ, сконструированные так, чтобы открывать регион MPER, они показали, что мощное широко нейтрализующее антитело 10E8 связывалось примерно в 70 раз плотнее с улучшенным конструктом, чем с предыдущей версией, в основном из‑за значительно более медленного диссоциирования. Контрольные мутации, разрушающие регион MPER, полностью устраняли связывание 10E8, что подтверждает способность платформы чувствительно фиксировать влияние изменений дизайна на ключевые эпитопы. Те же нанодиски работали как зонды в проточной цитометрии, помогая отбирать B‑клетки у иммунизированных мышей и обезьян, распознававшие полнотрансмембранную форму белка ВИЧ, включая участки, отсутствующие в стандартных растворимых зондаx. 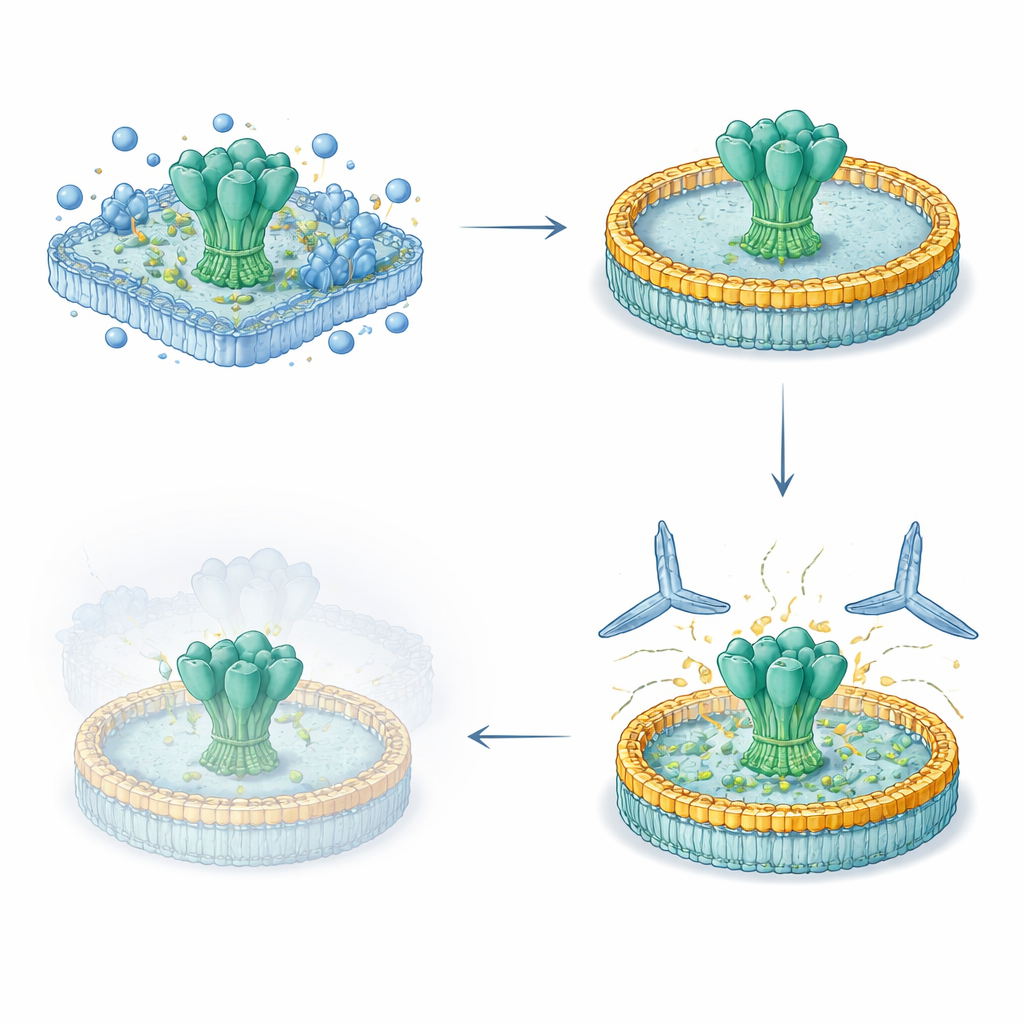
Наблюдение полной мишени в атомных деталях
Чтобы понять точно, как антитела узнают MPER в его нативной обстановке, авторы использовали криогенную электронную микроскопию для визуализации сконструированных нанодисков ВИЧ в комплексе с тремя различными широко нейтрализующими антителами. Они получили структуру с разрешением 3,5 ангстрема одного антитела, 10E8, взаимодействующего с сегментом MPER при том, что остальная часть шипа ВИЧ оставалась закреплённой в липидном диске. Это выявило непрерывную сеть контактов между 10E8 и как MPER, так и близлежащими участками внешнего белка, включая глубокий карман на стыке двух субъединиц. Сравнение этой структуры с ранее полученными изображениями 10E8, связанным только с коротким пептидом, показало, что мембранная среда и полноразмерный шип обеспечивают дополнительные контакты и динамические движения, невидимые в более простых моделях, и что отдельные аминокислоты в вирусе существенно влияют на способность 10E8 его нейтрализовать.
Широкие применения для более умных вакцин
Практически эта платформа нанодисков даёт разработчикам вакцин возможность оценивать трансмембранные кандидаты с теми же мощными аналитическими инструментами, которые долгое время применялись к растворимым фрагментам белков. Она работает для разных вирусов, поддерживает подробные измерения связывания, позволяет точно сортировать и секвенировать B‑клетки, индуцированные вакциной, и даёт высокоразрешающиеся структуры, улавливающие реалистичные мембрано‑близкие эпитопы. Для неспециалиста главный вывод таков: у учёных теперь есть более реалистичное испытательное поле для вирусных поверхностных белков, которое показывает, какие конструкции вакцин действительно похожи и ведут себя как настоящий вирус, и как их изменить для более сильных и широких антительнных ответов. Это должно ускорить разработку вакцин следующего поколения не только против ВИЧ, но и против многих других оболочечных вирусов.
Цитирование: Rantalainen, K., Liguori, A., Ozorowski, G. et al. Virus glycoprotein nanodisc platform for vaccine analytics. Nat Commun 17, 2561 (2026). https://doi.org/10.1038/s41467-026-68985-1
Ключевые слова: нанодиски, вакцины против ВИЧ, вирусные гликопротеины, широко нейтрализующие антитела, крио-ЭМ