Clear Sky Science · ru
Изменения на C‑конце белка влияют на протеостаз
Как хвостик белков формирует здоровье
Каждый белок в наших клетках заканчивается крошечным «хвостиком» длиной всего в несколько звеньев. На первый взгляд эти хвостики кажутся второстепенными, но исследование показывает: именно они тихо решают, какие белки задерживаются в клетке, а какие быстро удаляются. Поскольку уровни белков определяют развитие рака, наследственных заболеваний и реакцию клеток на стресс, понимание роли этих хвостов открывает новые пути для оценки риска болезни и даже разработки будущих терапий.
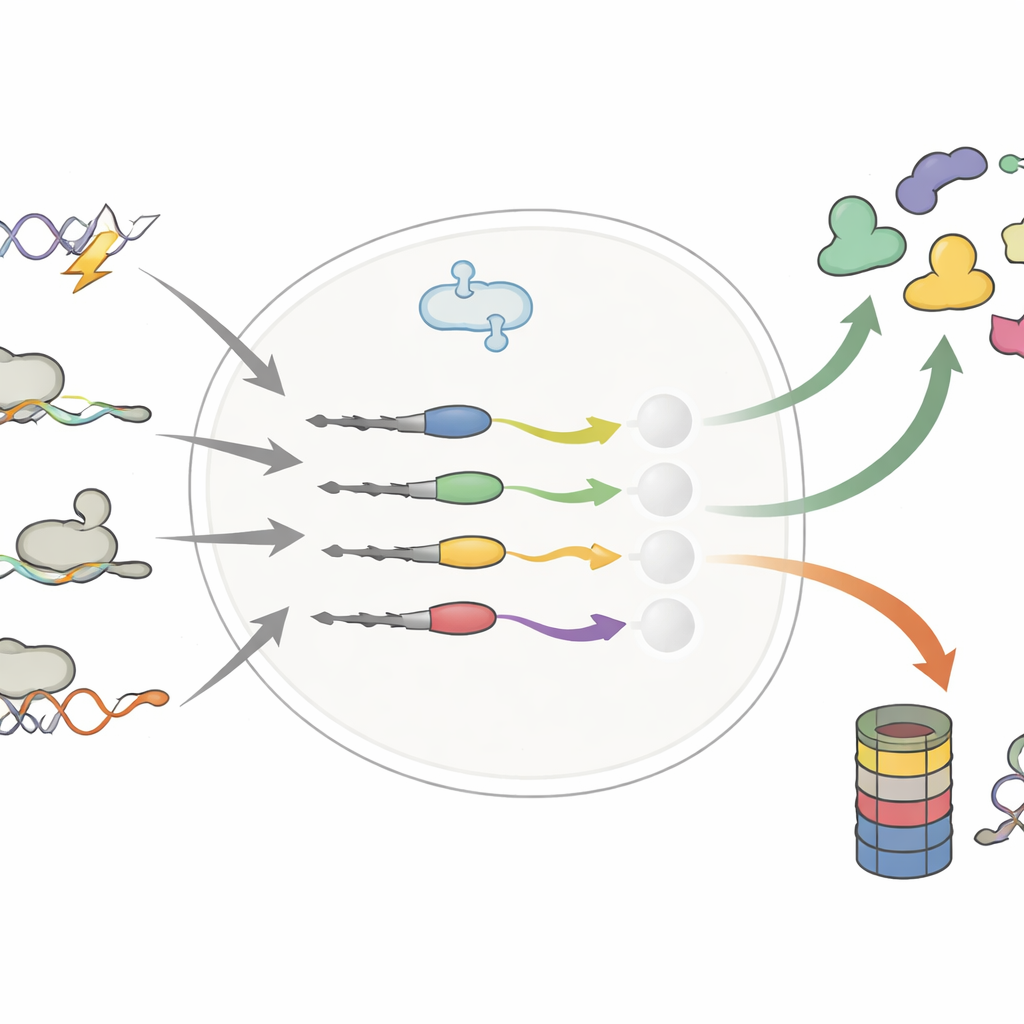
Небольшие изменения на хвосте белка — большие сдвиги в сроке жизни
Авторы сосредоточились на дальнем конце белков — C‑терминале — где даже несколько добавленных или заменённых звеньев могут появиться из‑за ДНК‑мутаций, альтернативного сплайсинга РНК или того, что рибосомы читают «стоп» дальше обычного. Ранее считали, что такие «ошибочные» хвосты в основном служат метками утилизации, отправляя дефектные белки на переработку. Систематически сравнив тысячи нормальных и модифицированных хвостов, это исследование опрокидывает простую картину. Группа показывает, что изменённые хвосты могут как укоротить, так и продлить жизнь белка, иногда стабилизируя онкогены или, наоборот, дестабилизируя белки‑супрессоры опухолей.
Когда генетические ошибки помогают или вредят белкам
Одним из основных источников изменений хвостов являются «nonstop»‑мутации, которые стирают нормальный сигнал стопа, и рибосома продолжает синтез в участке РНК, который обычно молчит. Исследователи проверили более 3000 таких вариантов, связанных с болезнями, с помощью двухцветного репортера, измеряющего, насколько каждый хвост защищает или ослабляет модельный белок. В среднем мутантные хвосты делали белки менее стабильными по сравнению с нормой, но значительная доля действовала противоположно: примерно одна из десяти nonstop‑мутаций стабилизировала белок, тогда как почти треть — дестабилизировала. Эти изменения затронули хорошо знакомые онкопротеиды и опухолевые супрессоры, что означает: то, что выглядело как тонкая мутация, может сдвинуть баланс между ростом и гибелью клетки.
Встроенное разнообразие от сплайсинга и ридтру‑скрытия стопа
Не все различия в хвостах — случайность. Наши гены регулярно дают несколько версий белка через альтернативный сплайсинг и программируемый ридтру (чтение стоп‑кодона). Анализируя каталоги человеческих генов, авторы обнаружили, что почти две трети генов кодируют белки с более чем одним дизайном хвоста, и многие из них различаются лишь в последних нескольких звеньях. Тестирование выбранных примеров показало, что эти почти идентичные версии часто имеют явно разные времена полураспада. Некоторые хвосты, образованные ридтру, делали белки более стабильными, другие — менее. Это указывает на то, что клетки намеренно используют вариации хвостов как тонкий регулятор, подстраивая длительность существования конкретных форм белков в разных тканях или условиях.
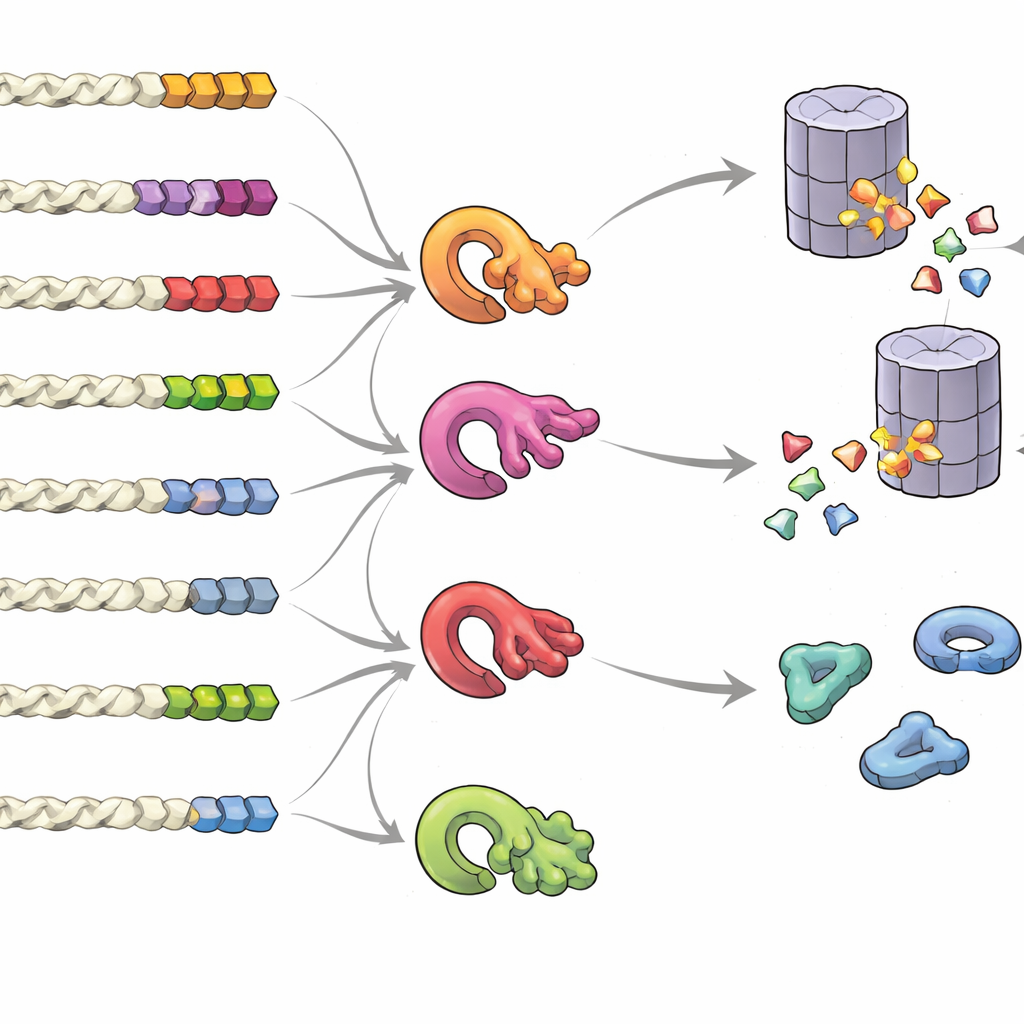
Что делает хвост сигналом «хранить» или «выбрасывать»
Чтобы понять, какие характеристики хвоста решают судьбу белка, команда создала библиотеки случайных хвостов и массово измерила их влияние. Оказалось, что это не один фиксированный «мотив», а общая композиция, позиция и кластерность определённых звеньев имеют значение. Хвосты, обогащённые малыми или гидрофобными компонентами, а также реже встречающимися цистеином и триптофаном, склонны вызывать деградацию, особенно если эти остатки сгруппированы. Напротив, хвосты, богатые кислотными остатками, способствовали стабильности. Сравнение многих видов показало, что нормальные белковые хвосты несут признаки эволюционного давления, направленного на избегание рискованных паттернов, тогда как хвосты, образующиеся при ридтру или сдвиге рамки считывания, сдвинуты в сторону дестабилизирующих композиций. Группа также обнаружила, что несколько ферментов контроля качества — разные убиквитин‑лигазы — специализируются на распознании различных гидрофобных паттернов хвоста, формируя сложную сеть, которая решает, какие белки уничтожать.
Почему это важно для медицины и биотехнологий
Работа переквалифицирует хвосты белков из пассивных окончаний в активные регуляторы их количества. Для неспециалиста это означает, что многие болезни могут возникать не только из‑за дефектных белков, но и из‑за тонких изменений в том, как долго белки сохраняются, вызванных крошечными различиями на их концах. Исследование также предупреждает, что терапии, намеренно продвигающие ридтру стоп‑сигналов и используемые для лечения некоторых генетических болезней, могут непреднамеренно изменить сроки жизни многих нормальных белков. В то же время результаты предлагают мощные новые стратегии: инженеря последовательности хвостов или побуждая клетки предпочитать определённые формы сплайсинга или ридтру, учёные однажды смогут точно регулировать уровни белков вверх или вниз.
Цитирование: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
Ключевые слова: стабильность белка, C‑концевой хвост, деградация белка, генетические мутации, протеостаз