Clear Sky Science · ru
VSIG10L — важный фактор поддержания гомеостаза пищевода и наследственной предрасположенности к пищеводу Барретта
Почему это важно для людей с изжогой
Хроническая изжога — распространённое явление, но лишь небольшая часть людей впоследствии развивает пищевод Барретта, состояние, которое может привести к раку пищевода. В этом исследовании задают простой, но важный вопрос: почему одни семьи значительно более склонны к появлению пищевода Барретта, чем другие? Проследив роль одного гена и изучив, как он формирует выстилку пищевода у людей и мышей, исследователи выявили недостающую связь между наследственным риском, повреждением от рефлюкса и способностью организма поддерживать здоровье пищевода.
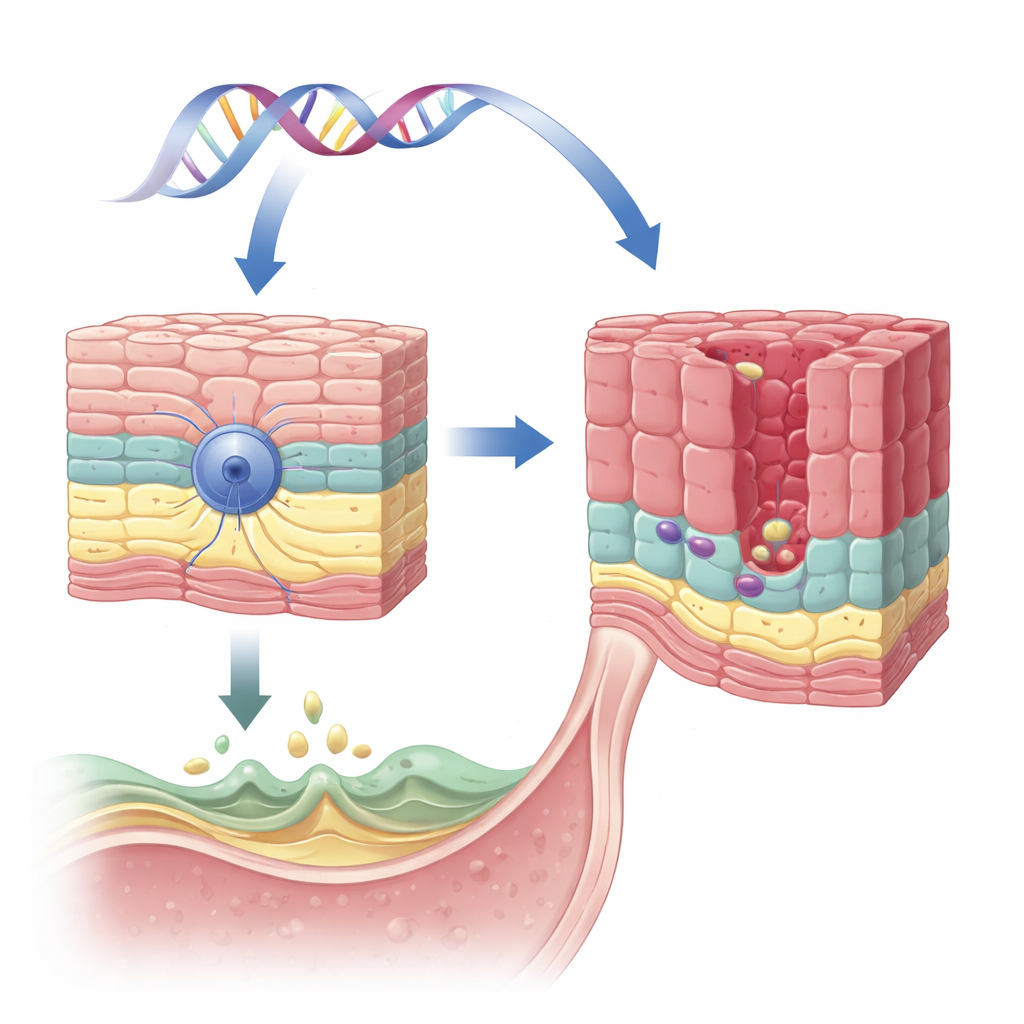
Защитный ген в слизистой пищевода
Команда сосредоточилась на гене под названием VSIG10L, ранее отмеченном в одной большой семье с множеством случаев пищевода Барретта и родственных раков. VSIG10L активен в верхних слоях плоских (покровных) клеток, выстилающих пищевод, но не в более глубоких, стволоподобных базальных клетках. С помощью чувствительного метода обнаружения РНК в тканях человека, свиньи и мыши, а также в трёхмерных культурах человеческих клеток пищевода исследователи показали, что VSIG10L постоянно включён только в «созревающих» клетках прямо над базальным слоем. Такая картина указывает на то, что VSIG10L помогает плоским клеткам завершить последние стадии созревания и сформировать стабильный барьер.
Наследственные изменения, ослабляющие барьер
Проследив последовательности гена VSIG10L у 684 человек из 302 семей с пищеводом Барретта и раком пищевода, исследователи обнаружили несколько редких вредоносных вариантов. Чтобы проверить эффект этих вариантов, они создали органоиды пищевода, полученные из стволовых клеток пациента с одной такой мутацией. По сравнению с органоидами от здорового донора мутантные органоиды не смогли построить нормальную многослойную плоскую структуру. Вместо этого они часто формировали аномальные, похожие на железы шаровидные скопления клеток, остававшиеся в базальном, незрелом состоянии, отмеченном белком p63. Это искажение нормальной слоистости и созревания повторяет ранние этапы, которые, как считают, предшествуют развитию пищевода Барретта у пациентов.
Мышиные модели, воспроизводящие человеческое заболевание
Чтобы выйти за рамки клеточных культур, команда создала мышей, несущих либо точную копию семейной человеческой мутации VSIG10L, либо полную потерю гена. У здоровых мышей соответствующий ген Vsig10l снова оказывался активен только в надбазальных плоских клетках. При электронном микроскопе у мутантных животных наблюдалась выраженная потеря десмосом — крошечных «заклёпок», скрепляющих соседние клетки — в этих слоях. Карты активности генов из плоского отдела желудка мыши, региона, напоминающего нижний отдел пищевода, показали широкое нарушение программ структуры и дифференцировки. Когда мышей кормили диетой, содержащей желчную кислоту деоксихолат, моделируя хронический рефлюкс, у 70–100% животных с мутантным Vsig10l развивались обширные участки, похожие на пищевод Барретта, богатые слизью, в месте перехода плоской эпителии — столбчатой, тогда как у мышей дикого типа возникали лишь маленькие, ограниченные поражения.
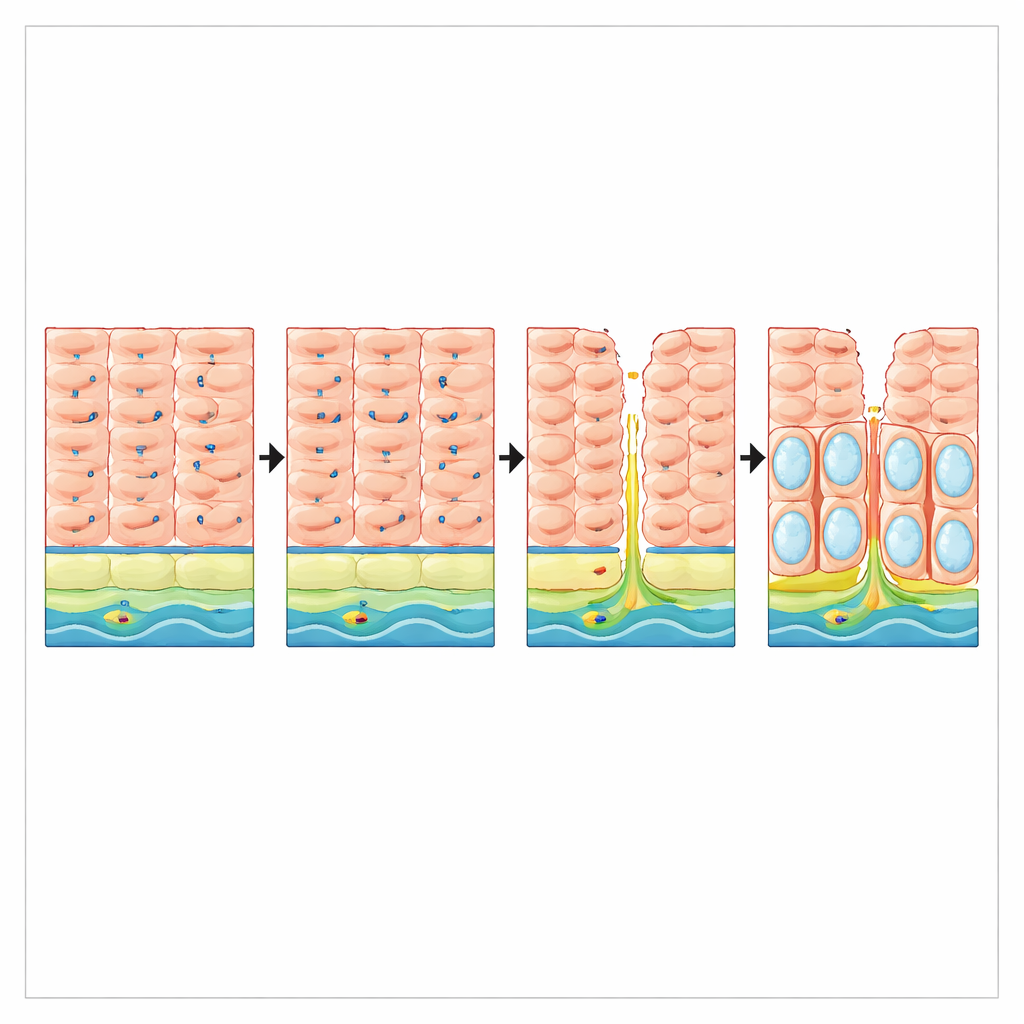
Повреждение от рефлюкса и утрата защиты у пациентов
Далее исследователи выясняли, может ли сам рефлюкс нарушать экспрессию VSIG10L у людей. В биоптатах пациентов с длительным гастроэзофагеальным рефлюксом, но без пищевода Барретта, уровень РНК VSIG10L был примерно в три раза ниже, чем у людей без рефлюкса, хотя базовый маркер плоских клеток TP63 оставался неизменным. В срезах ткани здоровая слизистая пищевода демонстрировала чёткую полосу VSIG10L-положительных клеток над базальным слоем. Напротив, при повреждении рефлюксом слизистой наблюдалось расширение базалеподобных клеток, богатых p63, и почти полная утрата градиента VSIG10L-положительной дифференцировки. Эти результаты свидетельствуют о том, что хронический рефлюкс разъедает не только физическую целостность выстилки, но и генетическую программу, поддерживающую упорядоченное обновление эпителия.
Сводя факты воедино
В целом работа поддерживает простую модель: VSIG10L — ключевой страж плоского эпителиального барьера пищевода. Наследственные дефекты в этом гене или приобретённое его угнетение при хроническом рефлюксе приводят к нарушению созревания выстилки, сокращению числа клеточно-клеточных анкеров и более проницаемой поверхности. В таком уязвимом состоянии повторные воздействия кислоты и желчи способствуют аномальному, железистому заживлению вместо восстановления исходного плоского эпителия, что создаёт предпосылки для развития пищевода Барретта. Для пациентов и семей это исследование указывает путь к будущим генетическим тестам, которые могут выявлять наиболее подверженных риску, и к новым терапиям, направленным на сохранение или восстановление функции VSIG10L с долгосрочной целью предотвращения пищевода Барретта и его прогрессирования в рак.
Цитирование: Ravillah, D., Singh, S., Katabathula, R.M. et al. VSIG10L is a major determinant of esophageal homeostasis and inherited predisposition to Barrett’s esophagus. Nat Commun 17, 2167 (2026). https://doi.org/10.1038/s41467-026-68975-3
Ключевые слова: Пищевод Барретта, гастроэзофагеальный рефлюкс, генетическая предрасположенность, эпителиальный гомеостаз, риск рака пищевода