Clear Sky Science · ru
Эксплуатация аллостерии человеческой фукозилтрансферазы 8 с помощью ковалентного ингибитора для подавления карбоновой фукозилизации
Почему блокирование крошечной сахарной метки имеет значение при раке
Наши клетки постоянно украшают белки небольшими сахарными цепочками, которые точно настраивают их функции. Одна из таких сахарных меток, называемая карбоновой фукозилизацией, способствует росту опухолей, их распространению, уклонению от иммунной системы и даже развитию резистентности к современным противораковым препаратам. В этой работе описано, как исследователи обнаружили скрытый контрольный пункт на человеческом ферменте, добавляющем этот сахар, и создали новое малотоксичное соединение, которое к нему ковалентно прикрепляется и выключает активность фермента. Их работа открывает новый путь для лекарств, которые тонко перенастраивают клеточные поверхностные сахара вместо того, чтобы напрямую атаковать ДНК или белки.
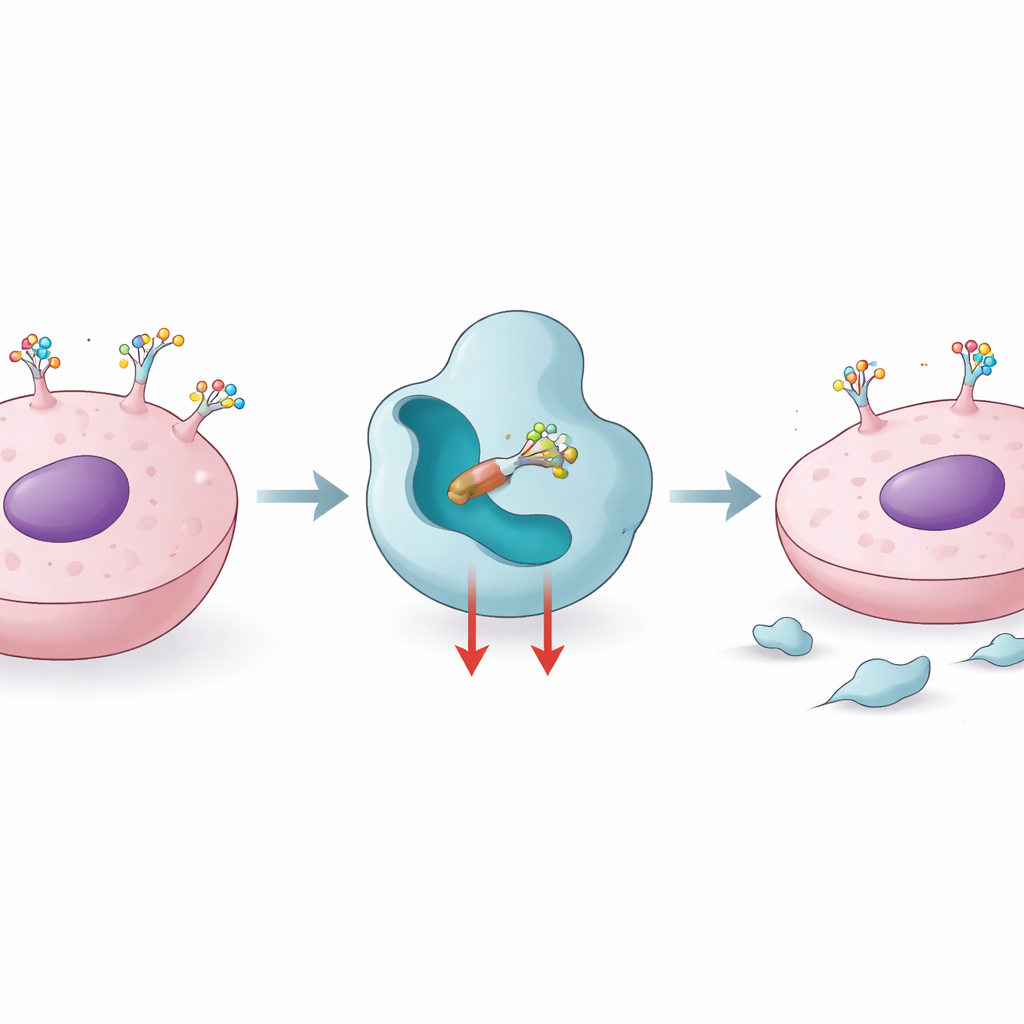
Как клетки используют сахарные метки для формирования болезни
Белки, покидающие внутриклеточный «завод», проходят через молекулярную «финишную линию», где к ним присоединяют и редактируют сахарные цепочки. Карбоновая фукозилизация — один из таких завершающих этапов, который выполняет фермент FUT8, добавляющий один сахар фукозу к ключевой позиции на многих связанных с белком гликанах. При повышении уровня FUT8 эта сахарная метка становится более распространённой на молекулах, контролирующих рост клеток, их подвижность и распознавание иммунной системой. Исследования связывают высокую активность FUT8 с агрессивной меланомой, тройным-негативным раком молочной железы, раком лёгких и устойчивостью к таргетной терапии и некоторым антителозависимым препаратам. Блокирование FUT8 может снять с поверхности клетки определённые иммунные тормоза, такие как PD‑1, и сделать опухоль более заметной для иммунной системы, что делает FUT8 привлекательной мишенью для иммуннотерапии рака и для улучшения биологических лекарств.
Необходимость более умных и селективных блокаторов
Создание препаратов против FUT8 было сложным, потому что многие родственные ферменты используют одно и то же базовое сахарное «топливо». Ранние ингибиторы часто имитировали это топливо, что приводило к широкому, неселективному подавлению множества путей фукозилирования и нежелательным побочным эффектам, включая проблемы с свертыванием крови, которые остановили клиническое испытание. Авторы предположили, что лучшая стратегия — избегать перегруженного главного активного центра и вместо этого искать уникальное «удалённое» место на FUT8, работающее как управляющий переключатель. Используя высокопроизводительный скрининг активности фермента, они просеяли более шести тысяч соединений и выделили несколько цепочечных молекул, которые замедляли FUT8 и одновременно снижали инвазивность раковых клеток в лабораторных культурах.
Открытие скрытого контрольного кармана
С помощью рентгеновской кристаллографии команда решила трёхмерные структуры FUT8, связанного с двумя из этих ингибиторов. К их удивлению, ни одно из соединений не находилось в обычном месте, где связываются донор и акцептор сахара. Вместо этого оба молекулы расположились в длинном, похожем на канал кармане между двумя крупными лопастями фермента, близко, но отдельно от активного центра. Связывание в этом участке смещало определённые петли и ключевые аминокислоты, в частности элементы, которые обычно помогают захватывать донор сахара. Компьютерное моделирование показало, что при заполнении кармана общая подвижность и энергетический ландшафт FUT8 изменяются в сторону конформаций, плохо подходящих для катализа реакции. Иными словами, ингибиторы действовали аллостерически: они нажимали удалённую «кнопку», из‑за чего рабочие части фермента приходили в несоосное состояние.
Преобразование «хита» в точный ковалентный инструмент
Ориентируясь на эту структурную карту, исследователи искали молекулы, которые не только заполняли бы карман, но и могли сформировать постоянную связь с близлежащим остатком лизина (K216), который естественным образом поворачивается в сторону канала. Они обнаружили реагент SSO, несущий реактивный N‑гидроксисукцинимидный эфир, который связывался в той же борозде и формировал ковалентную связь с K216, запирая фермент в неактивном состоянии. Опираясь на общие черты SSO и ранее обнаруженного компонента NH125, они объединили фрагменты обоих для создания новой молекулы, названной CAIF. Кристаллические структуры подтвердили, что CAIF проходит вдоль канала, плотно размещается среди гидрофобных остатков и образует ковалентную связь с K216. Этот дизайн многократно усилил ингибирование FUT8 по сравнению с исходными соединениями при сохранении щадящего действия по отношению к близкородственным ферментам, подчёркивая уникальную форму аллостерического кармана FUT8.
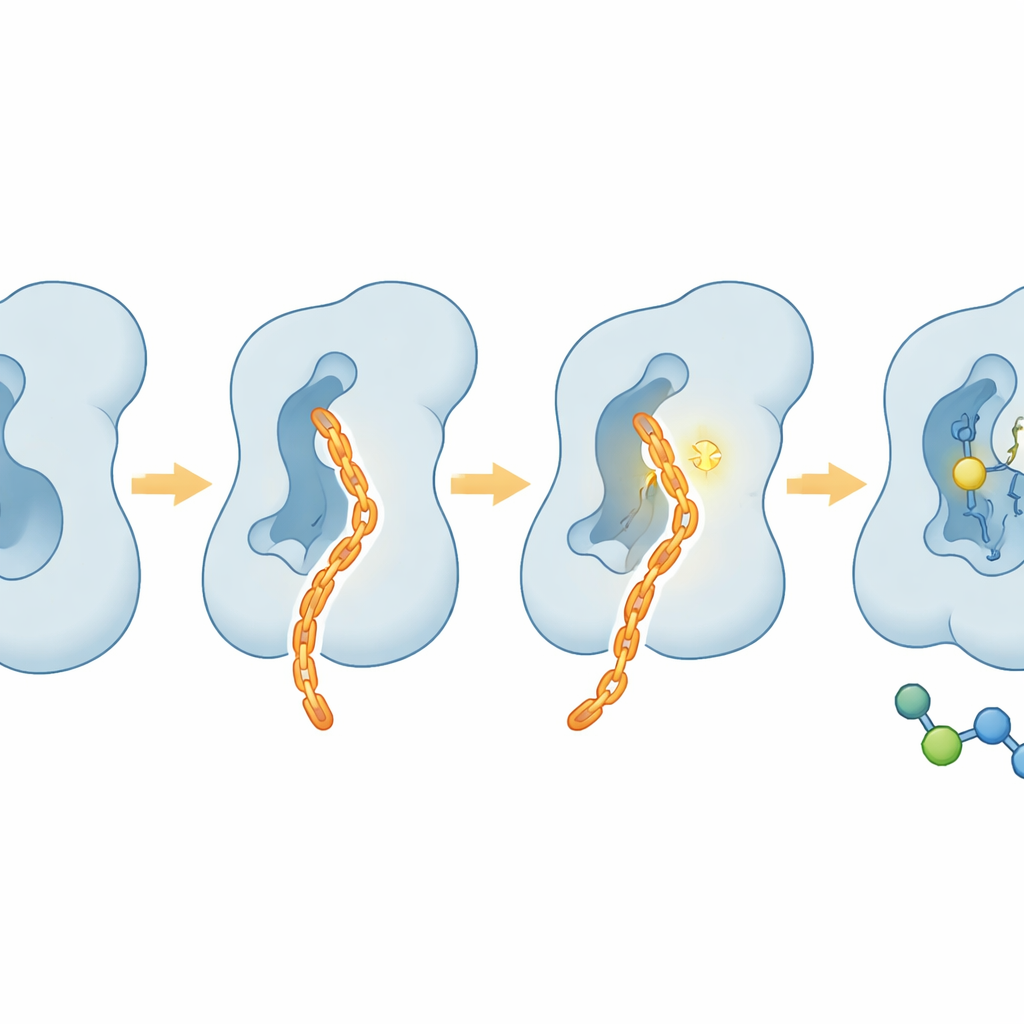
Мягко для клеток, жёстко для поведения опухоли
Помимо пробирок, команда изучила поведение CAIF в живых клетках. В нескольких линиях человеческих клеток CAIF продемонстрировал минимальную токсичность даже при высоких дозах, что указывает на отсутствие широкотоксичного воздействия на клеточную машину. Тем не менее он значительно уменьшал карбоновую фукозилизацию на поверхности клеток, как показали красители, связывающие сахара, и при этом был гораздо более селективен в отношении FUT8, чем ранние пан‑ингибиторы. В тестах инвазии раковых клеток CAIF превзошёл широко используемый сахарный блокатор по ограничению способности опухолевых клеток мигрировать через матрикс — признаку метастатического потенциала. Эти эффекты согласуются с известной ролью FUT8 в усилении инвазии и уклонении от иммунитета, а не с прямым стимулированием деления клеток.
Что это значит для будущего лечения рака
Это исследование не утверждает, что сам CAIF готов стать лекарством. Скорее оно демонстрирует, что у FUT8 есть ранее неизвестный, пригодный для лекарственной атаки аллостерический карман, нацелившись на который можно с помощью тщательно подобранных молекул сформировать прочную связь с одним лизином. Используя это место, исследователи могут выборочно приглушать фермент, модифицирующий сахара, который находится на стыке прогрессии рака, уклонения от иммунитета и лекарственной резистентности, при этом не затрагивая в значительной мере родственные ферменты. Работа предлагает план для разработки следующего поколения ингибиторов, которые будут перестраивать паттерны сахарных модификаций на белках, и потенциально расширит арсенал средств для иммуннотерапии рака и улучшения антителесодержащих препаратов.
Цитирование: Jiang, J., He, D., Ke, M. et al. Exploiting human fucosyltransferase 8 allostery with a covalent inhibitor for core fucosylation suppression. Nat Commun 17, 2607 (2026). https://doi.org/10.1038/s41467-026-68971-7
Ключевые слова: ингибирование FUT8, карбоновая фукозилизация, ковалентные аллостерические ингибиторы, гликозилирование при раке, дизайн препаратов против гликозилтрансфераз