Clear Sky Science · ru
FANCD2 сдерживает продвижение вилки и предотвращает хрупкость на ранних началах при повторном реплицировании
Когда копирование ДНК немного сбивается с ритма
При каждом делении клетки она должна скопировать всю свою библиотеку ДНК ровно один раз. Если фрагменты этой библиотеки копируются дважды или копирование происходит поспешно и неаккуратно, это может привести к разрывам хромосом и мутациям, питающим развитие рака. В этом исследовании изучают, что происходит, когда барьеры клетки против дополнительных раундов копирования ослабевают, и показывают, как белок репарации FANCD2 вмешивается, чтобы не дать слегка нарушающим правила клеткам скатиться в полную геномную катастрофу.
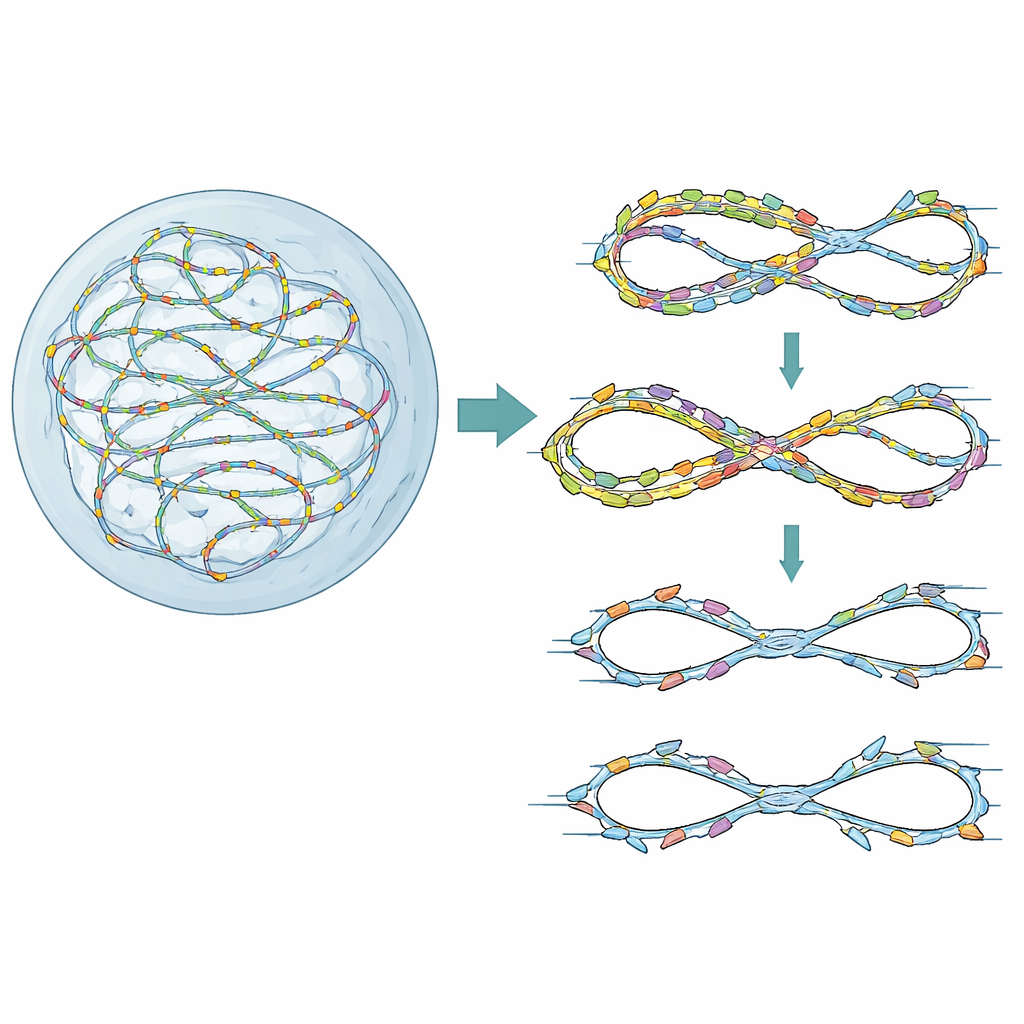
Ограждения для одного аккуратного дубля
Наши хромосомы дублируются с тысяч стартовых точек, или «источников», которые лицензируются и затем активируются в строго скоординированной последовательности. Небольшой белок Geminin обычно помогает гарантировать, что каждый источник активируется только один раз за цикл клетки. При потере или ослаблении Geminin некоторые источники могут активироваться повторно на уже скопированной ДНК — состояние, известное как повторное реплицирование. Раковые клетки, которые часто перепроизводят факторы лицензирования, особенно подвержены этой проблеме. Авторы сначала провели большой генетический скрининг в человеческих клетках, подготовленных к низкому уровню повторного реплицирования за счёт истощения Geminin. Они выясняли, какие гены репарации ДНК и контрольных точек становятся критическими в этом стрессовом состоянии, и обнаружили, что FANCD2, наиболее известный ремонтом межцепочечных сшивок ДНК при анемии Фанкони, выступает ключевым защитником выживания клетки и целостности генома.
Первый реагент у перегруженных копировальных машин
Команда затем проследила, где и когда появляется FANCD2 в клетках, подвергающихся повторному реплицированию. Вскоре после удаления Geminin FANCD2 быстро накапливается на хроматине и образует яркие ядерные фокусы, задолго до появления широкомасштабных разрывов ДНК. С помощью маркировки недавно синтезированной ДНК и методов близости они показали, что FANCD2 привлекается прямо к активным репликационным комплексам, особенно в клетках, чья ДНК уже копируется во второй раз. В синхронизированных клетках, выпущенных в следующий клеточный цикл, возникла отдельная популяция с диффузным паттерном чрезмерного реплицирования. Эти клетки демонстрировали сильные сигналы FANCD2 и RPA, что указывает на продолжающийся репликационный стресс, и задерживались перед митозом активной контрольной точкой, что предполагает: FANCD2 участвует в раннем ответе, стабилизирующем нагруженные вилки, а не просто реагирует на уже сломанную ДНК.
Сдерживание убегающих вилок и скрытых разрывов
Чтобы проверить, как FANCD2 влияет на копирование ДНК, исследователи совместили потерю Geminin с истощением FANCD2. Удивительно, но удаление FANCD2 не увеличивало долю клеток с явно повторно реплицированными геномами. Вместо этого анализ одиночных молекул ДНК в ассиметричных «волокнах» выявил, что репликационные вилки прошли дальше и стали более асимметричными — признак неравномерного и нестабильного продвижения. Эти более быстрые вилки оставляли после себя больше одноцепочечных разрывов в недавно синтезированной ДНК, обнаруживаемых как интенсивные фокусы RPA и native BrdU и подтверждённые чувствительностью меченых участков к ферменту, расщепляющему одноцепочечные области. Клетки, лишённые и Geminin, и FANCD2, демонстрировали резкий рост числа хромосомных разрывов, фрагментов, ядерных телец и микронуклеусов — все признаки серьёзной геномной нестабильности. Блокирование PARP, фактора, который обычно помогает управлять такими разрывами, имитировало и усугубляло эти дефекты, подчёркивая, что неконтролируемое образование зазоров является центральной причиной повреждений.
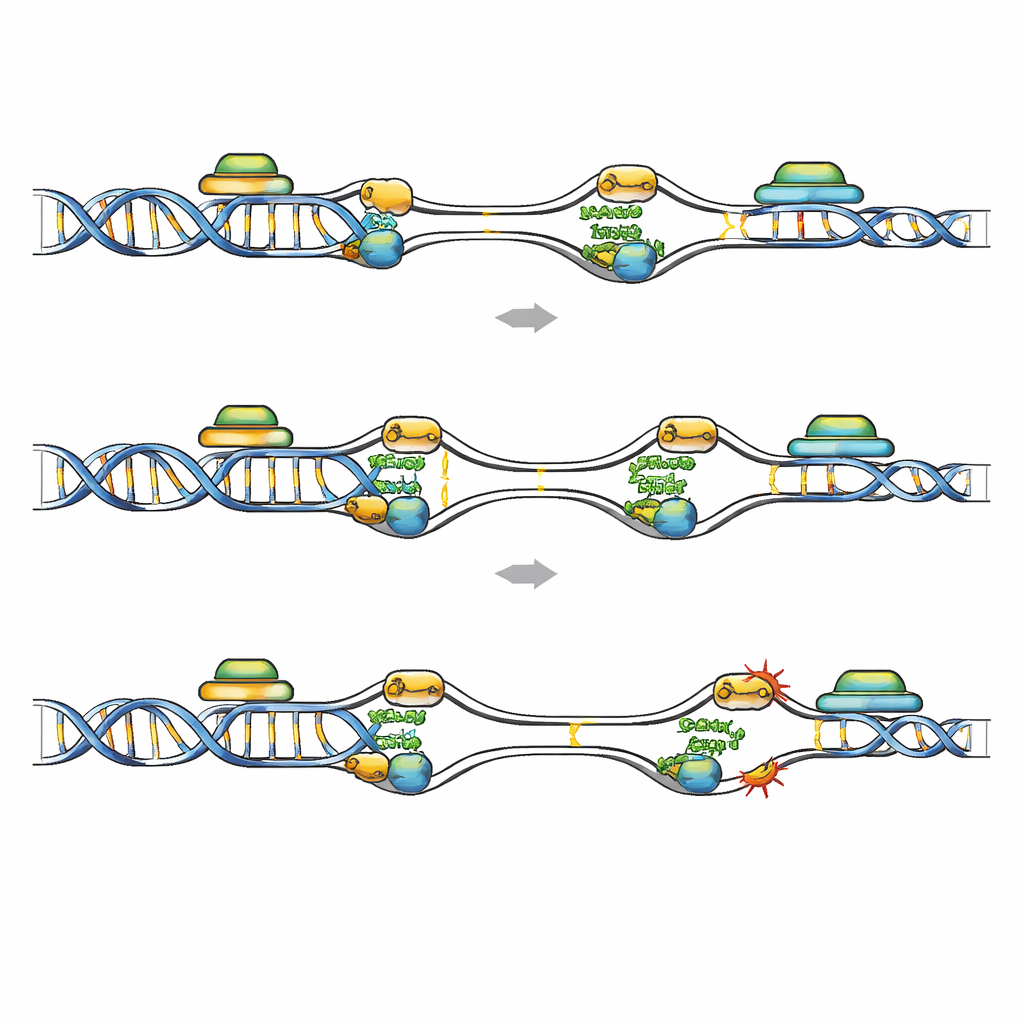
Хрупкие горячие точки, где копирование сталкивается с чтением
Картирование на уровне всего генома локусов связывания FANCD2 показало, где повторное реплицирование наиболее опасно. В лейкемических клетках с истощённым Geminin FANCD2 сместился от классических общих хрупких сайтов к раннеактивирующимся источникам репликации, расположенным внутри коротких, богатых GC и активно транскрибируемых генов. Эти регионы несут признаки активной транскрипции и склонны к образованию R-образных структур (R-loops), где вновь синтезируемая РНК гибридизируется с матричной ДНК, потенциально блокируя репликацию. Публичные наборы данных показали больше повреждений ДНК и повышенные сигналы РНК–ДНК гибридов в генах, обогащённых FANCD2 после потери Geminin, и эти участки перекрывались с так называемыми ранними реплицируемыми хрупкими сайтами. Когда транскрипция была широко подавлена лекарством или когда R-loops специально убирали переэкспрессией RNase H1, число фокусов FANCD2, RPA и повреждений ДНК в клетках, лишённых Geminin, заметно уменьшалось. Это указывает на то, что столкновения между повторно активированными источниками и активными транскрипционными единицами, усиленные R-loops, создают хрупкие горячие точки, которые должен защищать FANCD2.
Тонкая настройка защиты с помощью химических меток
FANCD2 активируется частично за счёт присоединения маленькой убиквитиноподобной метки. Путём истощения FANCA, ключевого компонента системы пометки, и с использованием клеток, экспрессирующих мутант FANCD2, устойчивый к этой модификации, авторы показали, что моно-убиквитинирование улучшает выживаемость при повторном реплицировании, но не является абсолютно обязательным. Даже не модифицированный FANCD2 предоставлял частичную защиту, что согласуется с различными ролями белка в распознавании и стабилизации нагруженных вилок. В целом картина такова: FANCD2 помогает замедлять и организовывать репликацию на уязвимых ранних источниках и ограничивает число и размер одноцепочечных зазоров.
Почему это важно для лечения рака
Для неспециалистов основной вывод состоит в том, что не все ошибки репликации изначально катастрофичны. Слабое повторное реплицирование, как это бывает в некоторых опухолях, может переноситься, если такие защитные системы, как FANCD2, сдерживают неконтролируемое копирование ДНК и не дают хрупким зазорам превратиться в разорванные хромосомы. Когда эта защита утрачена или переполнена, те же самые незначительные ошибки лицензирования быстро перерастают в разрушение генома. Поскольку потеря Geminin и дефекты лицензирования репликации характерны для раковых клеток, а многие опухоли уже несут уязвимости в сети Fanconi/BRCA, выявленные здесь уязвимости предлагают терапевтические подходы: сочетание ингибиторов, подталкивающих раковые клетки к повторному реплицированию, с препаратами, усиливающими накопление зазоров, например ингибиторами PARP, может выборочно довести злокачественные клетки до предела их терпимости, сохранив нормальные клетки с целой защитой.
Цитирование: Badra-Fajardo, N., Karydi, E., Bayona-Feliu, A. et al. FANCD2 restrains fork progression and prevents fragility at early origins upon re-replication. Nat Commun 17, 2478 (2026). https://doi.org/10.1038/s41467-026-68966-4
Ключевые слова: стресс репликации ДНК, FANCD2, Geminin, повторное реплицирование, нестабильность генома