Clear Sky Science · ru
Сборка суррогатной легкой цепи и пред‑B‑клеточного рецептора управляется укладкой, вызванной ассоциацией
Как наш организм проводит «тест‑драйв» новых антител
Прежде чем молодая B‑клетка в костном мозге получит право войти в состав иммунной системы, ей предстоит пройти строгую проверку: сможет ли она собрать работоспособное ядро антитела? В этой статье исследуется, как специальная «репетиционная» версия части антитела, называемая суррогатной легкой цепью, помогает выполнить эту проверку. Наблюдая, как эти белки сворачиваются и соединяются, авторы выявляют скрытую систему контроля качества, которая решает, какие будущие антитела достаточно хороши, чтобы их оставить, а какие — отбраковать.
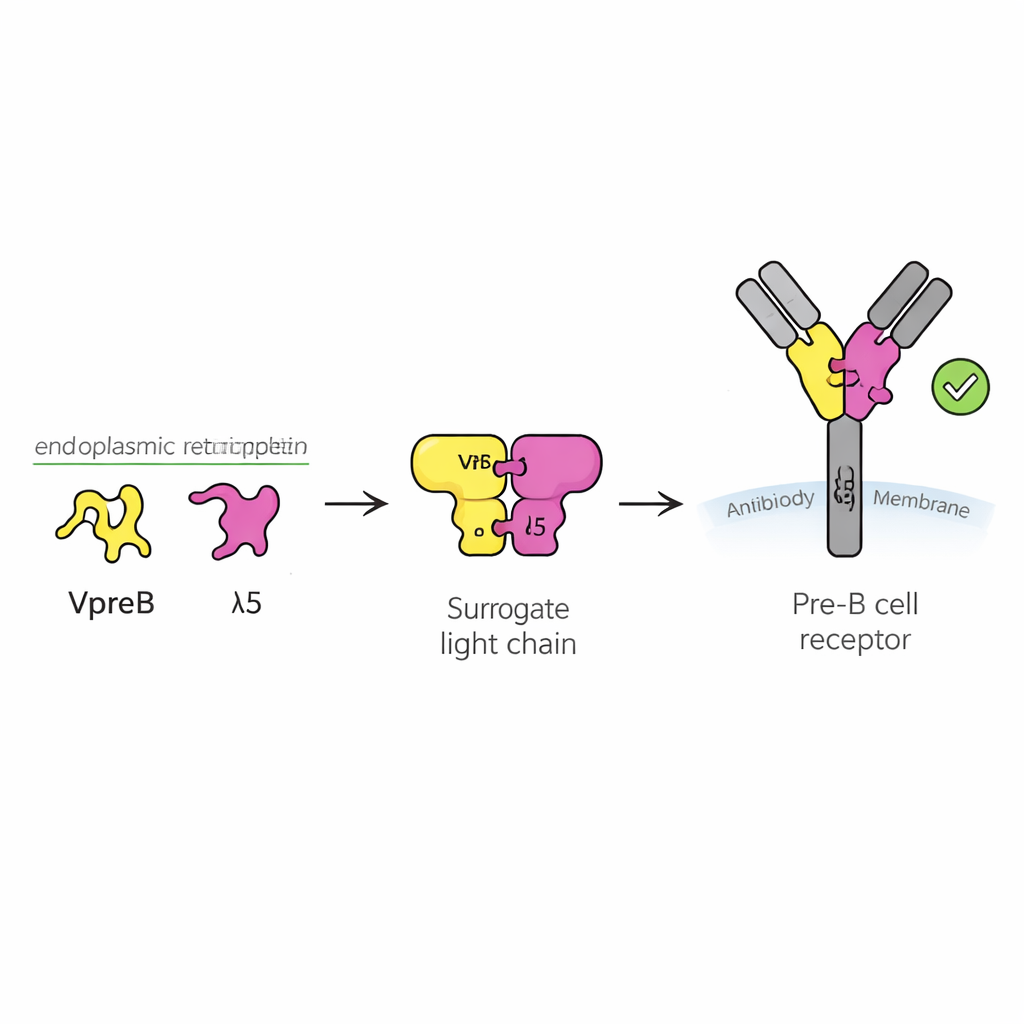
Контрольная точка безопасности для молодых иммунных клеток
Антитела — это белки Y‑образной формы, распознающие чужеродные микроорганизмы. Они состоят из двух основных частей: тяжелых и легких цепей. В процессе развития B‑клетки сначала синтезируется тяжелая цепь, и клетке нужно понять, полезна ли эта новая тяжелая цепь, прежде чем тратить ресурсы на создание подходящей легкой цепи. Для этого клетка использует временную замену, называемую суррогатной легкой цепью, состоящую из двух белков — VpreB и λ5. Вместе с тяжелой цепью они формируют пред‑B‑клеточный рецептор, сенсор на поверхности клетки, который передаёт сигнал «вперёд» или «стоп». Примерно половина недавно перестроенных тяжелых цепей не проходит эту проверку, поэтому понимание работы суррогатной легкой цепи — ключ к объяснению, как формируется здоровый репертуар антител.
Укладка через ассоциацию: помощь нестабильному партнёру
Авторы обнаружили, что один компонент — VpreB — в одиночку в основном неструктурирован и нестабилен. С помощью биофизических методов они показали, что он приобретает свою правильную трёхмерную форму лишь при связывании с λ5. Короткий участок λ5, имеющий форму бета‑цепи, вставляется в VpreB и завершает его структуру, как недостающий зубец в шестерёнке. Такая «укладка, вызванная ассоциацией», не только стабилизирует VpreB, но и создаёт очень прочное партнёрство между двумя белками с аффинностью в низком наномолярном диапазоне. В клетке только после сборки VpreB и λ5 в суррогатную легкую цепь они избегают удержания в эндоплазматическом ретикулуме и могут секретироваться или дальше транспортироваться, что подчёркивает тесную связь между укладкой и контролем качества.
Завершение тяжёлой цепи и прохождение инспекции
История не заканчивается на VpreB и λ5. Критически важный участок тяжёлой цепи, называемый CH1, изначально неструктурирован и удерживается внутри клетки. Исследователи показали, что λ5, выступая в роли некоего шаперона, может инициировать сворачивание CH1 при их взаимодействии. Этот второй шаг «укладки, вызванной ассоциацией», необходим для построения полного пред‑B‑клеточного рецептора и его выхода из эндоплазматического ретикулума на поверхность клетки. Любопытно, что обе части суррогатной легкой цепи — VpreB и λ5 — могут контактировать с тяжёлой цепью, но только λ5 способна привести CH1 в завершённое, пригодное к дальнейшему сворачиванию состояние. Когда этого не происходит, частичный рецептор задерживается, и клетка фактически отвергает данную тяжёлую цепь.
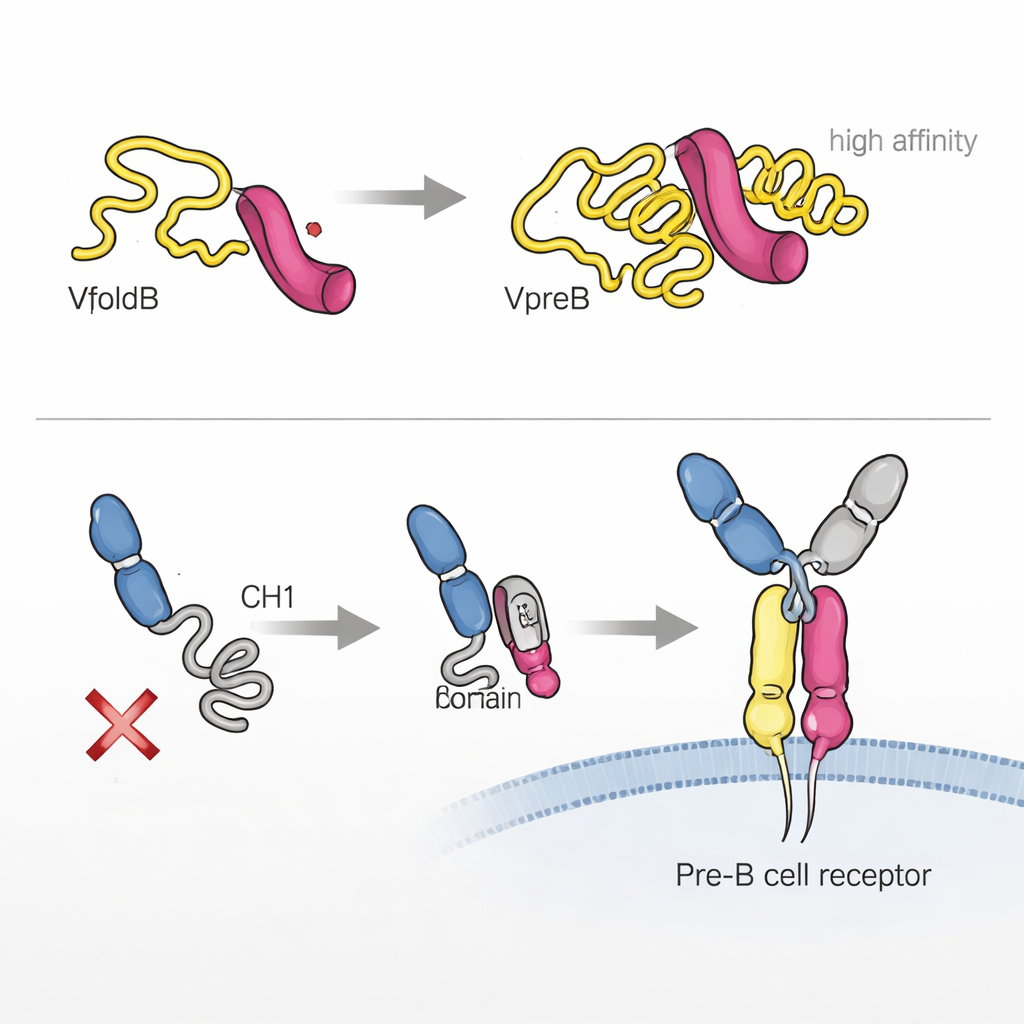
Гибкие хвосты, точно настраивающие связывание и сигнализацию
И VpreB, и λ5 несут гибкие, неструктурированные сегменты, известные как уникальные области, не похожие на какие‑либо известные последовательности белков. Хотя эти хвосты формально не обязательны для сборки двух белков в пробирке, исследователи обнаружили, что они сильно влияют на скорость образования суррогатной легкой цепи, её стабильность и силу связывания с участками тяжёлой цепи. В клетке удаление этих областей снижало эффективность секреции собранных комплексов. Хвост λ5 в особенности проявил многофункциональность: он ускоряет сборку, необходим для определённых контактов с вариабельной областью тяжёлой цепи и вносит значительный вклад в то, как пред‑B‑клеточный рецептор взаимодействует с антигенами и другими лигандами. В некоторых случаях сила связывания комбинации суррогатная легкая цепь–тяжёлая цепь приближалась к уровню нормального фрагмента антитела.
Почему это важно для разнообразия антител
Сопоставляя эти поэтапные события сворачивания и сборки, авторы предлагают, что суррогатная легкая цепь делает больше, чем просто удерживает тяжёлую цепь на месте. Она действует как динамичный инспектор, используя своё структурированное ядро и гибкие хвосты, чтобы оценить, может ли тяжёлая цепь правильно свернуться и продуктивно взаимодействовать с потенциальными мишенями. Успешные комбинации сворачиваются, стабилизируются и допускаются на поверхность клетки, где посылают сигналы, позволяющие B‑клетке продолжить созревание. Ошибочные комбинации задерживаются и в конечном итоге устраняются. Для неспециалиста главный вывод таков: ваша иммунная система использует сложную «испытательную станцию» для будущих антител, основанную на белках, которые буквально сворачивают друг друга в форму, гарантируя, что вперёд идут только хорошо «ведущие себя» ядра антител.
Цитирование: König, J., Sarmiento Alam, N.C., He, R. et al. Association-induced folding governs surrogate light chain and pre-B cell receptor core assembly. Nat Commun 17, 1202 (2026). https://doi.org/10.1038/s41467-026-68965-5
Ключевые слова: развитие B‑клеток, укладка антител, суррогатная легкая цепь, контроль качества белков, пред‑B‑клеточный рецептор