Clear Sky Science · ru
Инфекция HCMV нарушает барьерные функции и вызывает эпителиально-мезенхимальную трансформацию в модели органоида холангиоцитов
Почему эта история о вирусе в печени важна
Человеческий цитомегаловирус — очень распространённый вирус, который у большинства людей присутствует бессимптомно. Тем не менее у новорождённых и лиц с ослабленным иммунитетом он может быть связан с серьёзными поражениями печени и желчных протоков, включая редкое, но разрушительное детское заболевание — билиарную атрезию. В этом исследовании использовали миниатюрные выращенные в лаборатории человеческие желчные протоки, чтобы показать, как вирус может прямо повреждать эти тонкие каналы и вызывать рубцевание, что может помочь объяснить давно обсуждаемые связи между инфекцией и пожизненным заболеванием печени.
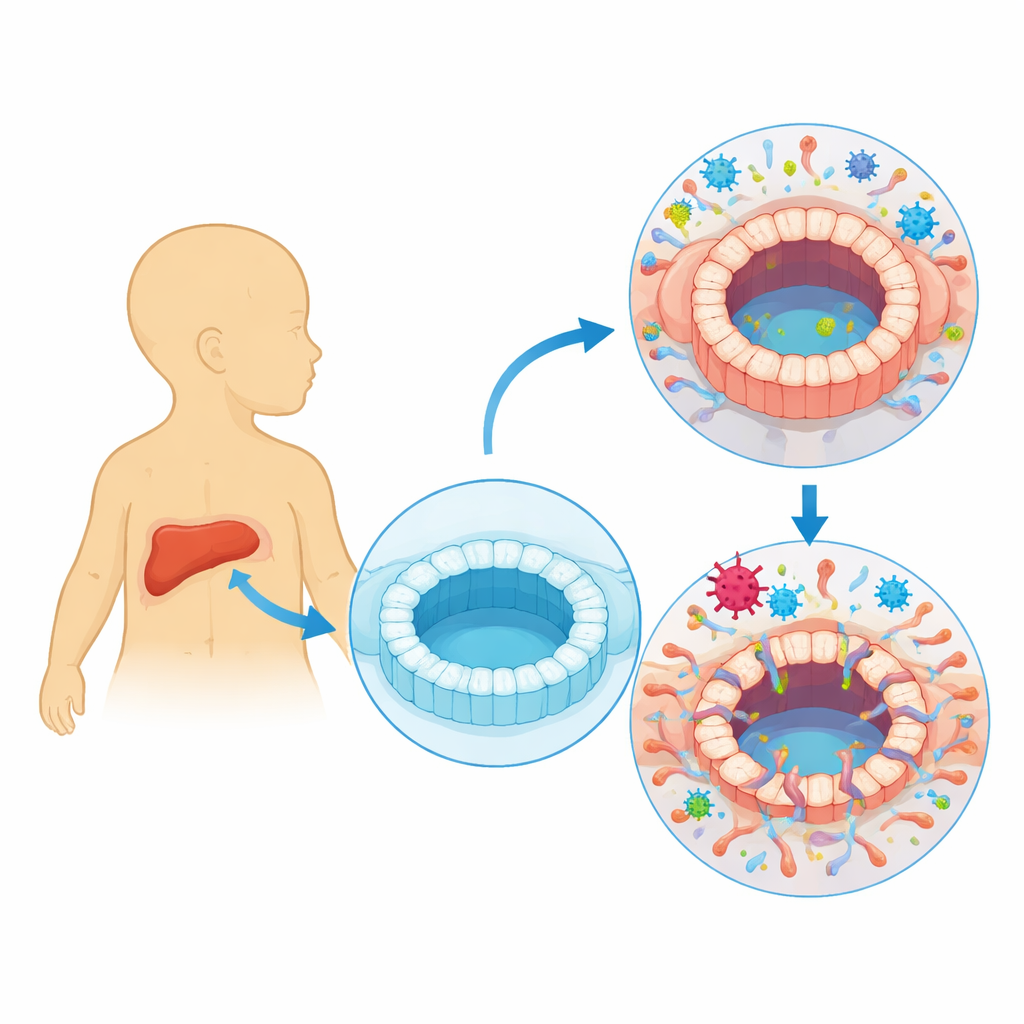
Более пристальный взгляд на распространённый, но бесшумный вирус
Человеческий цитомегаловирус (HCMV) обычно ведёт себя безактивно в наших организмах, переключаясь между фазой репликации, когда он создаёт новые вирусные частицы, и латентной фазой, когда скрывается в определённых клетках крови. Врачи давно отмечают, что у людей с явной HCMV-инфекцией может возникать повреждение желчных протоков и холестаз, при котором желчь не может нормально оттекать. Многие младенцы с билиарной атрезией — состоянием, при котором желчные протоки вскоре после рождения блокируются и рубцуются — также демонстрируют признаки недавней HCMV-инфекции. Однако оставалось неясным, заражает ли вирус непосредственно клетки, выстилающие желчные протоки, или лишь является попутным свидетельством болезни.
Создание крошечных желчных протоков в чашке Петри
Чтобы ответить на этот вопрос, исследователи создали трёхмерные «органоиды», имитирующие человеческие желчные протоки. Они начали с индуцированных плюрипотентных стволовых клеток, перепрограммированных из человеческой крови, и направили их дифференцировку в клетки, похожие на холангиоциты — клетки, выстилающие желчные протоки. Эти клетки самоорганизовались в полые сферы с центральной полостью и плотными межклеточными контактами, напоминая миниатюрный желчный проток. Команда затем подвергла эти органоиды воздействию штамма HCMV, помеченного флуоресцентным маркером, который светится при активной репликации вируса. Это позволило проследить инфицированные клетки и измерить, как органоиды меняются со временем.
Как инфекция деформирует структуру и ослабляет барьер
После инфицирования органоиды перестали нормально расти и деформировались, с утолщёнными и неровными стенками. Некоторые клетки ярко светились, показывая полную вирусную активность и производство новых вирусных частиц; другие содержали вирусный генетический материал в меньших количествах, что указывало на более латентное состояние. Функциональные тесты показали, что инфицированные органоиды утратили ключевые способности желчного протока. Они больше не набухали должным образом в ответ на стимул, зависящий от ионных каналов, и демонстрировали повышенную проницаемость в измерении электрического сопротивления, которое оценивает плотность барьера. Белки, которые обычно запечатывают пространства между клетками, такие как компоненты плотных контактов, были снижены, а транспорт тестового красителя внутрь и из внутренней полости стал аномальным. В совокупности эти изменения показывают, что HCMV может напрямую подрывать стенку желчного протока, делая её проницаемой и дисфункциональной.
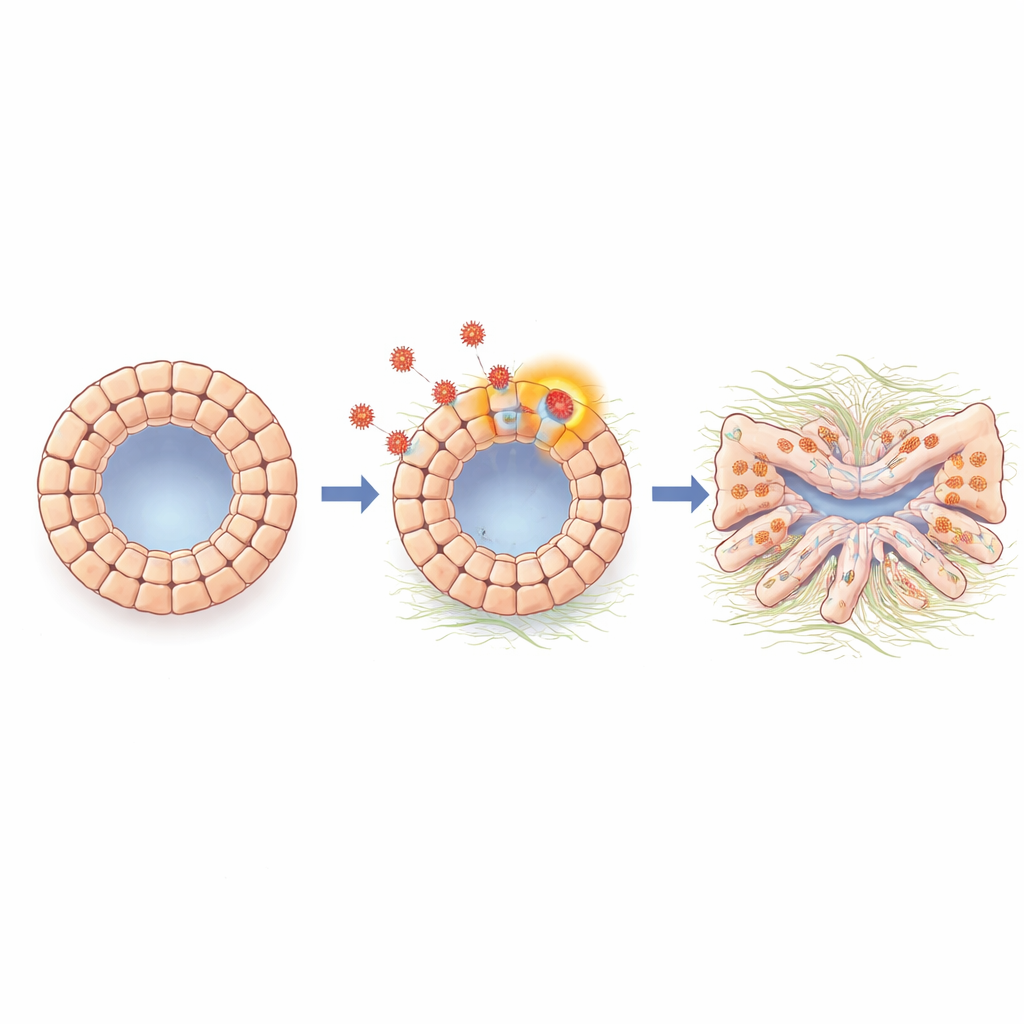
Клетки смещают идентичность в сторону рубцевания
Углублённый анализ активности генов в органоидах как в целом, так и на уровне одиночных клеток выявил сильную активацию программы, сходной с эпителиально‑мезенхимальной трансформацией — процесса, при котором плотные поверхностные клетки ослабляют связи, приобретают более подвижный, фиброзный фенотип и начинают продуцировать молекулы, связанные с рубцеванием ткани. В инфицированных органоидах повысились уровни N‑кадгерина и других маркеров, связанных с этим сдвигом, а также генов, вовлечённых в фиброз и синтез внеклеточного матрикса. Сигнальная молекула TGF‑бета, известная как ключевой драйвер рубцевания во многих органах, была усилена во время инфекции. Когда команда блокировала сигналирование TGF‑бета с помощью ингибитора низкомолекулярного соединения или антитела, органоиды восстановили более нормальную форму, а многие гены, связанные с рубцеванием и трансформацией, вернулись ближе к исходному уровню, что указывает на TGF‑бета как на важный посредник, связывающий присутствие вируса с вредными клеточными изменениями.
От выращенных в лаборатории трубок к больным детям
Чтобы проверить, соответствуют ли эти лабораторные наблюдения реальной болезни, исследователи изучили печёночную ткань детей с билиарной атрезией и при других педиатрических заболеваниях печени. С помощью чувствительных зондов они обнаружили ДНК HCMV в холангиоцитах — клетках желчных протоков — примерно в двух третях образцов билиарной атрезии, но гораздо реже в тканях печени без билиарной атрезии. В тех же областях, где была найдена вирусная ДНК, клетки желчных протоков демонстрировали повышенные уровни TGF‑бета и N‑кадгерина, повторяя картину трансформации и рубцевания, наблюдавшуюся в органоидах. Это позволяет предположить, что по крайней мере у части детей HCMV непосредственно инфицирует клетки желчных протоков и сдвигает их в фиброзное состояние, активируя пути, опосредованные TGF‑бета.
Что это означает для понимания и лечения заболеваний желчных протоков
Проще говоря, работа показывает, что распространённый вирус может проникать в клетки, выстилающие желчные протоки, ослаблять их плотные соединения и сдвигать их в рубцовое, менее специализированное состояние через сигнал на основе TGF‑бета. Эти изменения ослабляют барьерные и транспортные функции протоков и могут способствовать блокированию и фиброзу желчных протоков, наблюдаемым при таких заболеваниях, как билиарная атрезия. Хотя не во всех случаях заболевание желчных протоков вызвано HCMV, исследование укрепляет идею о том, что у уязвимых младенцев вирусная инфекция может быть важной частью этой картины, и что нацеливание на пути, связанные с TGF‑бета, потенциально могло бы помочь защитить или восстановить уязвимые желчные протоки в будущем.
Цитирование: Ye, Z., Hu, X., Rahaman, S.M. et al. HCMV infection disrupts barrier functions and promotes epithelial–mesenchymal transition in a cholangiocyte organoid model. Nat Commun 17, 2273 (2026). https://doi.org/10.1038/s41467-026-68962-8
Ключевые слова: цитомегаловирус, билиарная атрезия, органоиды желчных протоков, эпителиально-мезенхимальная трансформация, сигнальный путь TGF-бета