Clear Sky Science · ru
Медь-катализируемая энантиоконвергентная N-алкилирование гидразинов рацемическими α‑галамидов для получения энантиомерообогащённых гидразинов
Почему эти крошечные молекулы важны
Во многих современных лекарствах и экспериментальных соединениях есть небольшая, но важная фрагмент — гидразин. Когда этот фрагмент «ручный», то есть присутствует преимущественно в одной зеркальной форме, а не в смеси 50:50, это может кардинально изменить поведение молекулы в организме. Исследование, лежащее в основе этой статьи, представляет новый, эффективный способ получения таких одноручных (хиральных) гидразинов из дешёвых и доступных исходных материалов, что потенциально упрощает создание новых лекарств и биологически активных молекул.
От простых ингредиентов к точным продуктам
Авторы сосредоточились на двух типах простых строительных блоков: гидразинах и рацемических α‑галамидах. Гидразины содержат пару азот–азот и широко встречаются в фармацевтике, пептидоподобных структурах и азотно‑насыщенных циклах. Рацемические α‑галамиды — легко синтезируемые соединения, где реакционноспособный углерод расположен рядом с галогеном (например, хлором или бромом) и амидной группой. Если бы эти два партнёра можно было связать контролируемым образом, это обеспечило бы прямой путь к хиральным гидразинам без предварительного построения более сложных промежуточных соединений. До настоящего времени существующие методы либо требовали множества шагов, либо нестабильных окисленных реагентов, либо ограничивались редкими типами партнёров, которые не всегда встречаются в практических молекулах.
Новая роль меди как молекулярного проводника
Чтобы решить эту задачу, команда разработала медный катализатор, который превращает рацемическую смесь α‑галамидов в один предпочтительный хиральный продукт при взаимодействии с гидразинами. Вместо классического двухэлектронного пути образования связи, который плохо работает с нуклеофильными гидразинами и приводит к «отравлению» катализатора, они воспользовались радикально‑полярным переходом. На первом этапе медный комплекс использует одноэлектронную химию, чтобы оторвать галоген от α‑галамида, формируя короткоживущий радикал, связанный с металлом. Этот радикал затем рекомбинирует в центре меди, давая высокореакционноспособный, положительно поляризованный медный комплекс. На втором этапе гидразин атакует этот активированный партнёр с тщательно контролируемой стороны, так что формируется только одна зеркальная форма с высокой селективностью.
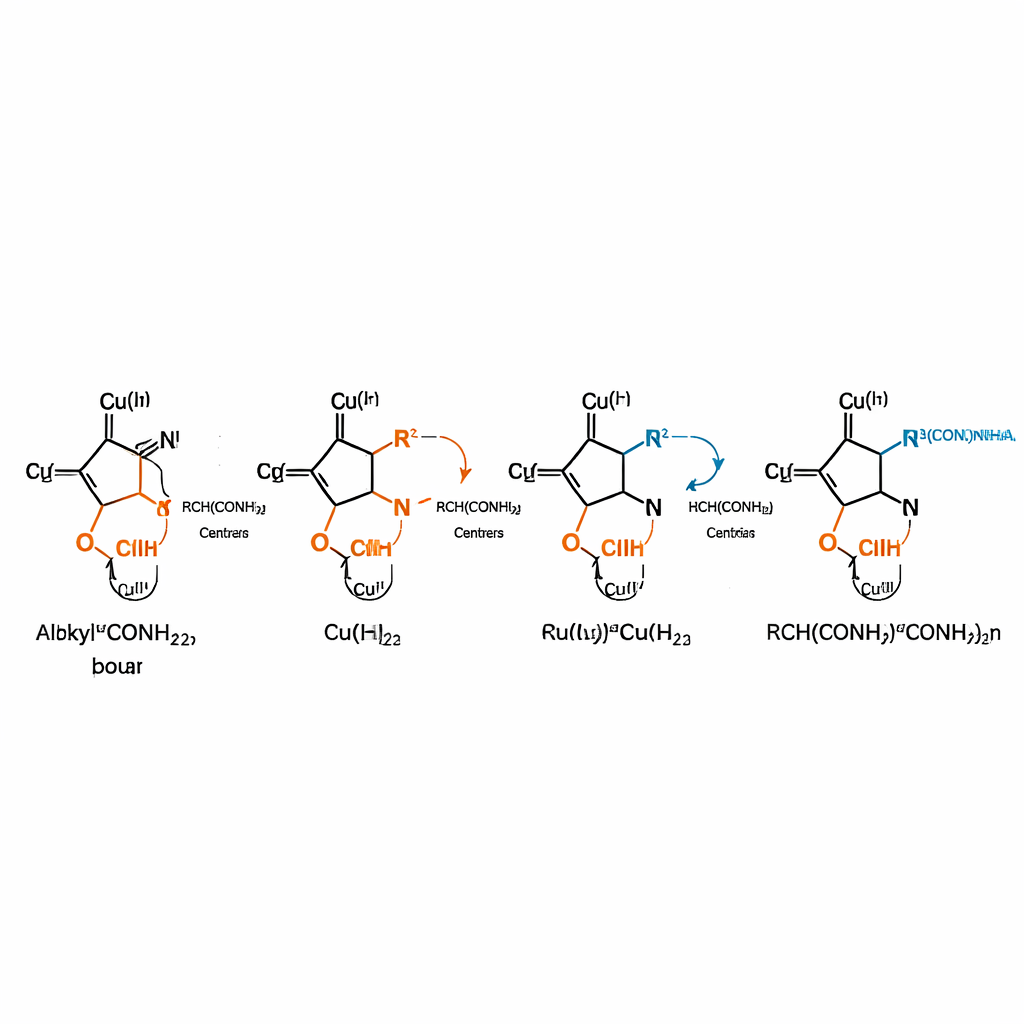
Настройка рецептуры для широкой и практичной применимости
Ключевым элементом прорыва стало проектирование хирального лиганда, окружающего атом меди. Исследователи обнаружили, что трехзвенный (тринента́тный), отрицательно заряженный N,N,N‑лиганда — трёхрукий, азотсодержащий каркас — критически важен. Он плотно связывается с меди́, увеличивает её восстановительную способность, что ускоряет образование радикалов, и стабилизирует высокоэнергетичную стадию меди(III), в которой определяется селективность. Путём систематического тестирования различных защитных групп гидразина они выделили N,N‑bis‑Boc гидразин как идеального партнёра: он направляет реакцию на один только азотный центр, выдерживает условия и затем может быть мягко удалён, чтобы получить свободный хиральный гидразин. При оптимизированных мягких условиях эта система превращает десятки рацемических α‑галамидов в хиральные гидразины с хорошими выходами и отличной энантиомерной чистотой — независимо от того, связан ли исходный углерод с ароматическим кольцом или с алкильной цепью.
Сборка пептидов и колец с точной формой
Преимущество платформы проявляется при работе со сложными блоками. Используя α‑галамиды, полученные из природных аминокислот, команда подготовила N‑аминоди‑пептиды — короткие фрагменты, в которых один азот заменён гидразином. Такие N‑аминные звенья известны тем, что стабилизируют необычные конформации пептидов и делают их устойчивыми к ферментативному разрушению, что привлекательно для дизайна лекарств. Удивительно, что сочетая нормальную или зеркальную версию хирального лиганда с исходными аминокислотами любой хиральности, химики получили все четыре возможных стереоизомера данного N‑аминоди‑пептида. Эта «стереодивергентная» управляемость позволяет из одинаковых простых входных материалов получить полный набор вариантов формы для биологического тестирования.
От строительных блоков к сложным структурам
После образования защищённых гидразинов их защитные группы можно удалить, получив свободные хиральные гидразины в виде стабильных солей. Эти соли затем гладко реагируют с простыми карбонильными соединениями, образуя разнообразные азотно‑насыщенные циклы — такие как пиразолы, фталазиноны и конденсированные гибриды пептид–кольцо — при сохранении их хиральности. Авторы также демонстрируют, что методика масштабируется без потери эффективности, что важно для практического применения. В целом работа предлагает простой, модульный маршрут от коммерчески доступных материалов к точно настроенным хиральным гидразинам и их производным.
Что это значит в перспективе
Для неспециалиста ключевая суть в том, что исследователи научили недорогой металлический катализатор — медь — собирать из перемешанных исходных компонентов один точно «ручный» продукт по требованию. Поскольку эти хиральные гидразины легко превращаются в пептиды и азотно‑богатые циклы, которые важны для многих лекарств, метод предоставляет мощную короткую дорогу для медицинских химиков и химических биологов. Он должен упростить и ускорить изучение того, как форма молекулы влияет на биологическую активность, в конечном счёте помогая выявлять новые терапевтические кандидаты и функциональные материалы.
Цитирование: Li, N., He, SY., Wang, PF. et al. Copper-catalysed enantioconvergent N-alkylation of hydrazines with racemic α-haloamides to access enantioenriched hydrazines. Nat Commun 17, 2070 (2026). https://doi.org/10.1038/s41467-026-68961-9
Ключевые слова: хиральные гидразины, медный катализ, радикально-полярный переход, энантиоселективный синтез, N-аминовыe пептиды