Clear Sky Science · ru
Понимание роль щелочных металлов в гидрогенизационном катализе через сильное взаимодействие металл–основание
Почему важно настраивать катализаторы для повседневной жизни
Преобразование простых молекул, таких как диоксид углерода и водород, в полезные топлива и химикаты имеет решающее значение для более чистой энергетики и экологически дружественной промышленности. Многие металлические катализаторы, которые управляют этими реакциями, уже содержат крошечные дозы щелочных металлов, таких как натрий или калий, в качестве «промоутеров», но их реальная роль долгое время оставалась неясной. В этом исследовании выявлен единый принцип работы этих добавок, предлагающий путь к созданию более разумных катализаторов, которые могут направлять реакции в сторону желаемых продуктов и уменьшать образование отходов.
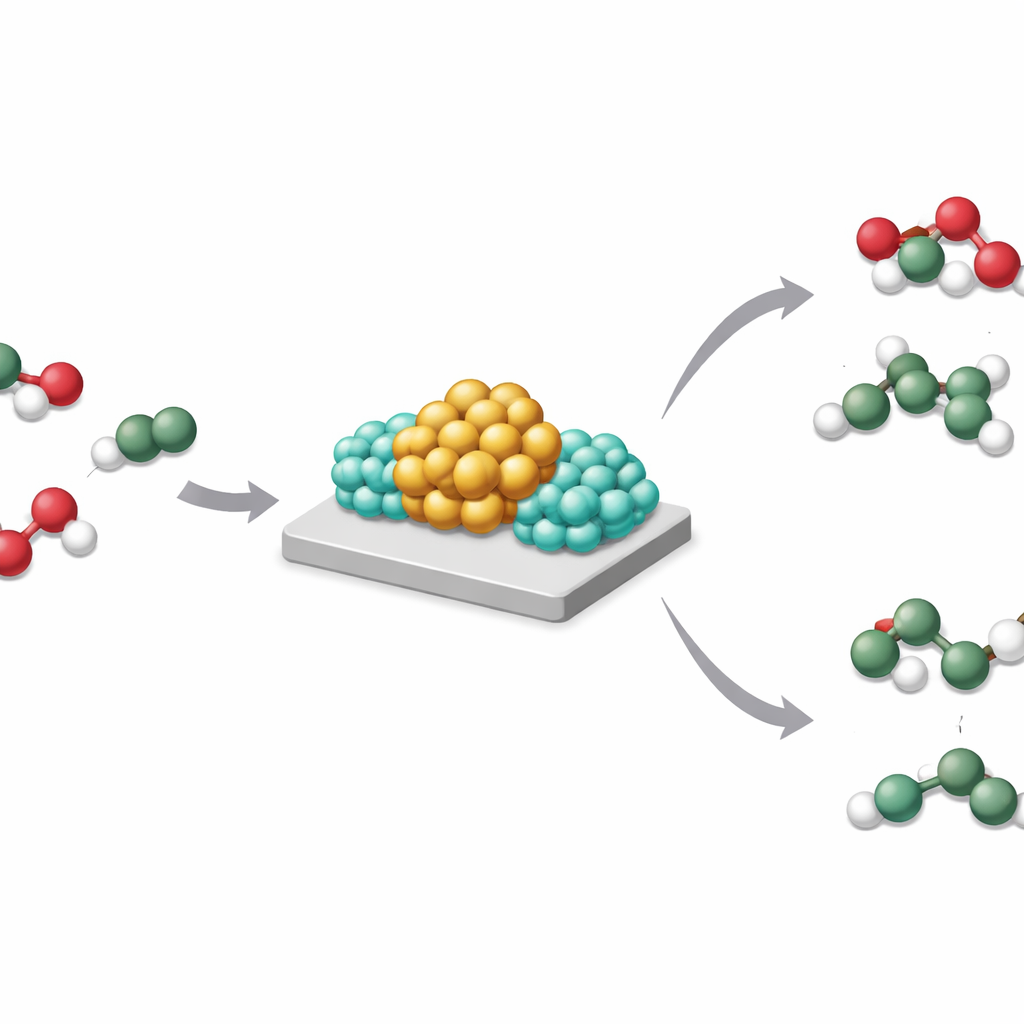
Более пристальный взгляд на усиленные металлические катализаторы
Катализаторы на основе переходных металлов, таких как родий и никель, расположенные на твердых носителях, помогают разрывать и восстанавливать химические связи. Десятилетиями промышленность добавляла щелочные металлы, чтобы сделать эти катализаторы более активными, селективными или долговечными. Обычно такие эффекты объясняли простыми геометрическими причинами (изменением формы и размера частиц) или прямой передачей электронов от щелочного металла к активному металлу. Однако в реальных рабочих условиях эти промоутеры присутствуют главным образом в виде оксидов, а не в виде голых атомов металла, что делает модель прямой передачи электронов неполной.
Открытие сильного партнерства на поверхности
Авторы изучали модельную систему: наночастицы родия на диоксиде титана, с добавлением натрия и без него. С помощью передовой электронной микроскопии, рентгеновской спектроскопии и компьютерного моделирования они обнаружили, что натрий располагается в виде оксида, Na₂O, прямо в краевой зоне контакта частиц родия с носителем. Под действием водорода такая конфигурация создает то, что они называют Сильным Взаимодействием Металл–Основание (SMBI). В этих особых контактных точках молекулы водорода расщепляются гетеролитически: более основный Na₂O захватывает протоноподобную часть, а родий удерживает электронно‑богатую часть. Такое «гетеролитическое» расщепление делает поверхность родия необычно богатой электронами и мешает распространению водорода, или «перетеканию» (spillover), на диоксид титана.
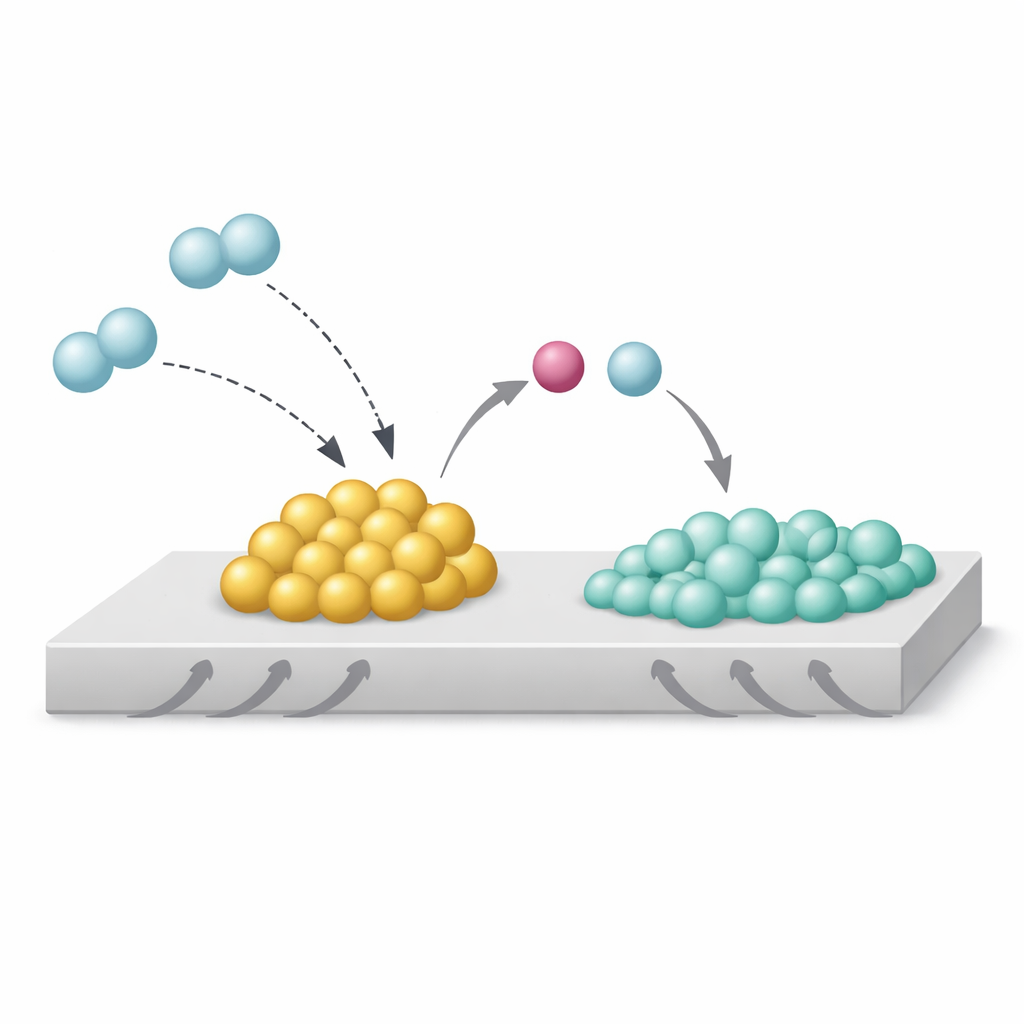
Как этот скрытый эффект управляет реакциями
Это тонкое перераспределение водорода и электронов имеет серьезные последствия. В гидрогенизации диоксида углерода чистый родий на диоксиде титана склонен к глубокой гидрогенизации с образованием метана. При добавлении натрия тот же катализатор в основном дает оксид углерода (CO), ценный строительный блок, и значительно меньше метана. Похожее поведение наблюдается при использовании лития или калия, а также при замене родия никелем. Авторы показывают, что когда водород свободно перетекает на носитель, доминирует глубокая гидрогенизация; когда же SMBI удерживает водород сосредоточенным на границе металл–основание и предотвращает его перенос на носитель, образуются более щадящие продукты.
Разные двойные связи — разные результаты
Далее команда изучала, как SMBI влияет на обычные органические гидрогенизации, затрагивающие двойные связи C=C, C=O и N=O. Для C=C в винилацетате промотор на основе натрия делает катализатор быстрее, вероятно потому, что электронно‑богатый родий ослабляет эту связь, а более слабо связанный водород эффективно присоединяется к ней. Напротив, для молекул вроде ацетофенона и нитробензола, реакционноспособные группы которых предпочитают располагаться на оксидном носителе, та же добавка натрия замедляет реакцию. Здесь подавление перетекания водорода означает, что носитель больше не получает достаточного количества водорода для проведения этих преобразований, показывая, что не все двойные связи выигрывают от одного и того же промоторного эффекта.
Проектирование катализаторов с намеренным контролем
Объединив эксперименты и теорию, авторы утверждают, что SMBI дает единый подход к пониманию того, как промоутеры на основе щелочных металлов перестраивают каталитические поверхности. Вместо того чтобы действовать как простые доноры электронов, оксиды щелочных металлов выступают в роли сильных ловушек для протонов, заставляя водород расщепляться поляризованно и удерживая реактивный водород рядом с интерфейсом металл–основание. Это понимание объясняет ранее вызывавшие вопросы закономерности в разнообразных реакциях гидрогенизации и для разных металлов и указывает на практическое правило проектирования: регулируя количество и расположение оксидов щелочных металлов вокруг металлических частиц, химики могут целенаправленно направлять реакции к определенным продуктам, одновременно оптимизируя активность и стабильность для более чистых химических процессов.
Цитирование: Jung, M., Dickieson, M.P., Chen, P. et al. Understanding alkali metal promotion in hydrogenation catalysis through Strong Metal–Base Interaction. Nat Commun 17, 2465 (2026). https://doi.org/10.1038/s41467-026-68952-w
Ключевые слова: катализ гидрогенизации, попрессоры на основе щелочных металлов, преобразование CO2, гетерогенные катализаторы, интерфейсы металл–оксид