Clear Sky Science · ru
Аллостерический ингибитор протеазы NS2B-NS3 вируса Зика с пероральной эффективностью в мышиных моделях
Новый способ перехитрить опасный вирус
Вирус Зика попал в заголовки новостей десять лет назад, когда инфекции у беременных женщин стали связаны с рождением детей с аномально малыми головами и повреждением мозга. И тем не менее до сих пор не существует одобренного препарата для лечения или профилактики Зика. В этом исследовании описан многообещающий новый пероральный соединение в форме таблетки, которое выключает ключевой вирусный фермент неожиданным способом и защищает мышей от тяжелой инфекции Зика, указывая путь к возможному лекарству, способному однажды обезопасить уязвимые группы людей, особенно во время вспышек.
Почему Зика по‑прежнему имеет значение
Вирус Зика преимущественно передаётся комарами рода Aedes и относится к тому же семейству, что и денге и вирус Западного Нила. У большинства инфицированных болезнь протекает бессимптомно или с лёгкими проявлениями, но примерно у каждого пятого развиваются проблемы от лихорадки и сыпи до серьёзных осложнений, таких как поражения глаз, отказ органов и расстройства нервной системы. Наибольшую опасность представляет риск для плода: инфицирование во время беременности может привести к микроцефалии и пожизненной инвалидности. Поскольку нет одобренной вакцины или антивирусной терапии, врачи могут предложить только поддерживающую помощь. Поэтому учёные рассматривают Зика как приоритет в подготовке к пандемиям и ищут лекарства, которые могли бы защитить группы риска и сдержать новые вспышки.
В поисках скрытых уязвимостей
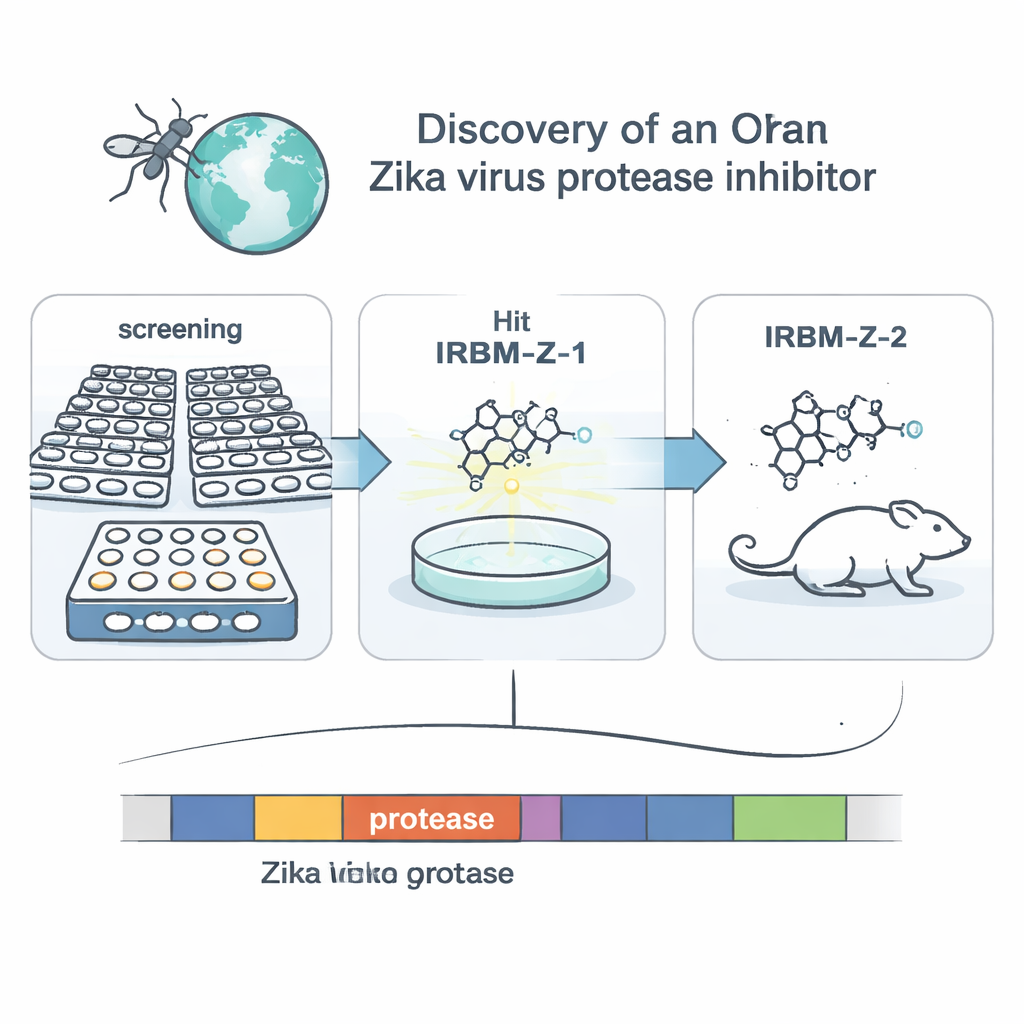
Исследователи сосредоточились на вирусном ферменте NS2B–NS3 протеазе. Эти «молекулярные ножницы» разрезают большой стартовый вирусный белок на фрагменты, необходимые для сборки новых вирусов, что делает фермент привлекательной мишенью для лекарств. Вместо того чтобы разрабатывать препарат для очевидного каталитического участка, команда использовала клеточный скрининг, имитирующий репликацию Зика в клетках почки обезьяны. Они создали модифицированный геном Зика, или репликон, лишённый структурных генов, но несущий луциферазный репортер, так что световой сигнал отражал копирование вируса. Просмотрев более 120 000 малых молекул из национальной химической библиотеки, они отобрали те, которые существенно снижали световой сигнал, не повреждая клетки, и затем подбирали вирусные репликоны, ставшие резистентными к каждому из «хитов». Эта генетическая детективная работа указала на протеазу как ключевую мишень для одного семейства соединений, во главе которого стояла исходная молекула IRBM-Z-1.
Фиксация фермента в неправильной форме
Биохимические тесты показали, что IRBM-Z-1 не конкурирует с обычным субстратом на каталитическом участке. Вместо этого он действует как неконкурентный, то есть аллостерический ингибитор — связываясь в отдельном кармане и не давая ферменту принять активную форму. Рентгеноструктурный анализ высокой чёткости показал, что соединение устраивается в ранее неизвестном кармане далеко от каталитического центра. Там его необычное «N‑ацилсидинон-иминное» ядро образует сеть водородных связей и стэкинговых взаимодействий, которые смещают ключевую область протеазы в открытую, неактивную конформацию. Одна аминокислотная замена в этой области, на позиции 156, делает вирус резистентным, что подчёркивает то, насколько точно соединение использует это скрытое место. Этот карман также отличается от аллостерических сайтов, описанных у родственныых флавивирусов, предлагая по-настоящему новую опору для разработки лекарств.
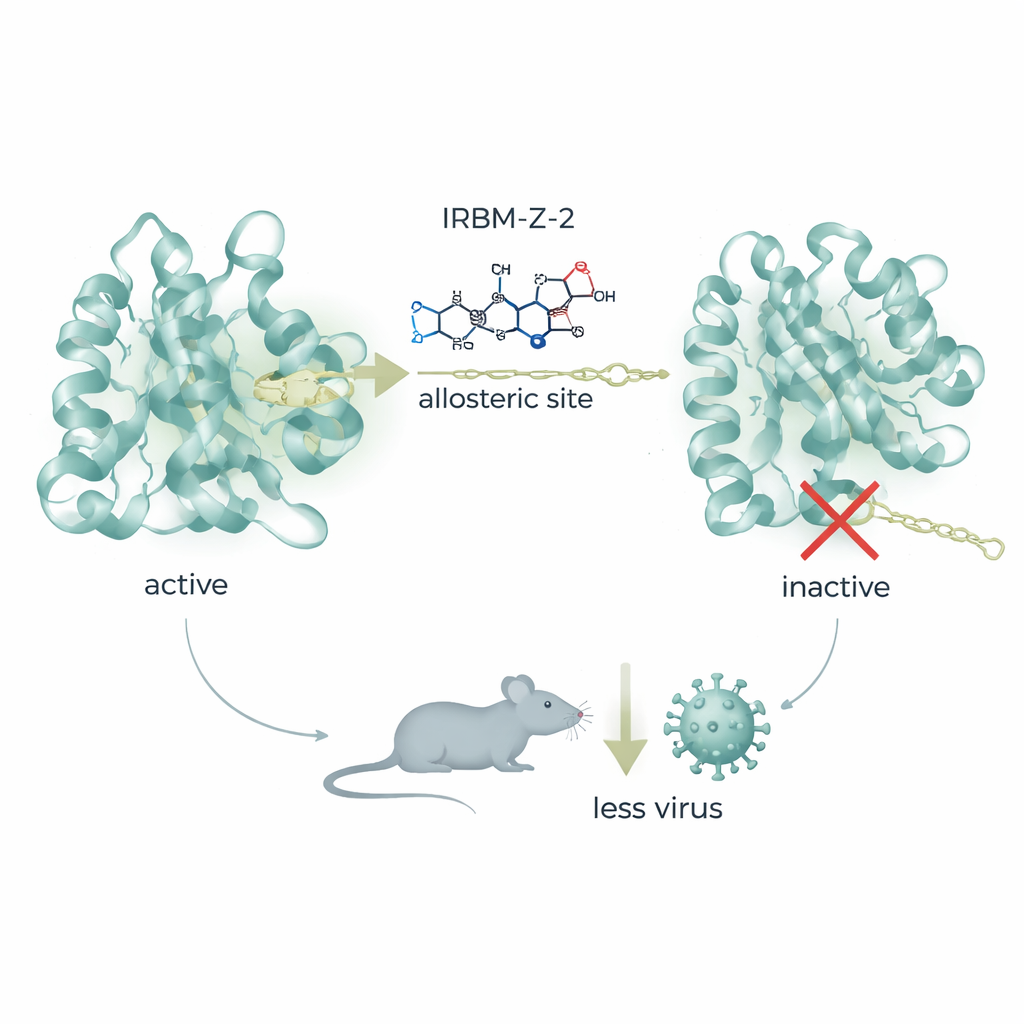
От «хит»-молекулы до защитного препарата в мышах
Опираясь на структурные данные, команда усовершенствовала IRBM-Z-1, получив более мощную молекулу под названием IRBM-Z-2. Это улучшенное соединение блокирует протеазу Зика в наномолярных концентрациях, сильно подавляет репликацию вируса в нескольких типах клеток и проявляет активность против родственных протеаз денге и Западного Нила при невредящем отношении к человеческим ферментам. В доклинических исследованиях IRBM-Z-2 показал благоприятные «лекарственные» свойства: стабилен в организме, хорошо всасывается при приёме внутрь и поддерживает концентрации в крови значительно выше требуемых для подавления вируса, без явных признаков токсичности. У особо восприимчивых мышей линии AG129, инфицированных Зика, ежедневное лечение — как инъекционно, так и перорально — резко снижало количество вирусной РНК в крови, предотвращало потерю веса и симптомы болезни и обеспечивало выживание всех леченных животных, тогда как контрольные незалеченные особи погибали от инфекции.
Что это может значить для будущих вспышек
В совокупности эти результаты представляют новый класс противовирусных средств против Зика, действующих путём «замораживания» критического вирусного фермента в неактивной позе, а не прямой блокадой его активного центра. Поскольку IRBM-Z-2 может применяться перорально, демонстрирует сильную защиту в строгих мышиных моделях и до сих пор имеет чистый профиль безопасности, он выглядит многообещающим кандидатом для дальнейшей разработки в качестве профилактического средства — потенциально для защиты беременных женщин, медицинских работников и путешественников в случае возобновления активности Зика. В более широком смысле недавно обнаруженный аллостерический карман может вдохновить на создание похожих препаратов против родственных вирусов, открывая новый фронт в борьбе с заболеваниями, передающимися комарами.
Цитирование: Ontoria, J.M., Torrente, E., Missineo, A. et al. An allosteric inhibitor of the Zika virus NS2B-NS3 protease with oral efficacy in mouse models. Nat Commun 17, 1439 (2026). https://doi.org/10.1038/s41467-026-68943-x
Ключевые слова: вирус Зика, противовирусный препарат, ингибитор протеазы, аллостерическая модуляция, заболевание, передающееся комарами