Clear Sky Science · ru
FCHo2, а не талин, обеспечивает внутренняя активацию интегрина ɑvβ5 в изгибах контактов
Как клетки ощущают форму окружения
Наши тела состоят из клеток, которые постоянно цепляются за окружающую среду, тянут и толкают, чтобы перемещаться, делиться или оставаться на месте. В этой статье показано, что клетки воспринимают не только жесткость окружения — они также считывают его форму. Открыв особую систему прикрепления, включающуюся лишь там, где мембрана клетки сильно искривлена, авторы демонстрируют, что для плоских и волокнистых поверхностей клетки используют разные внутренние «хватки», что важно для формирования тканей и распространения рака.
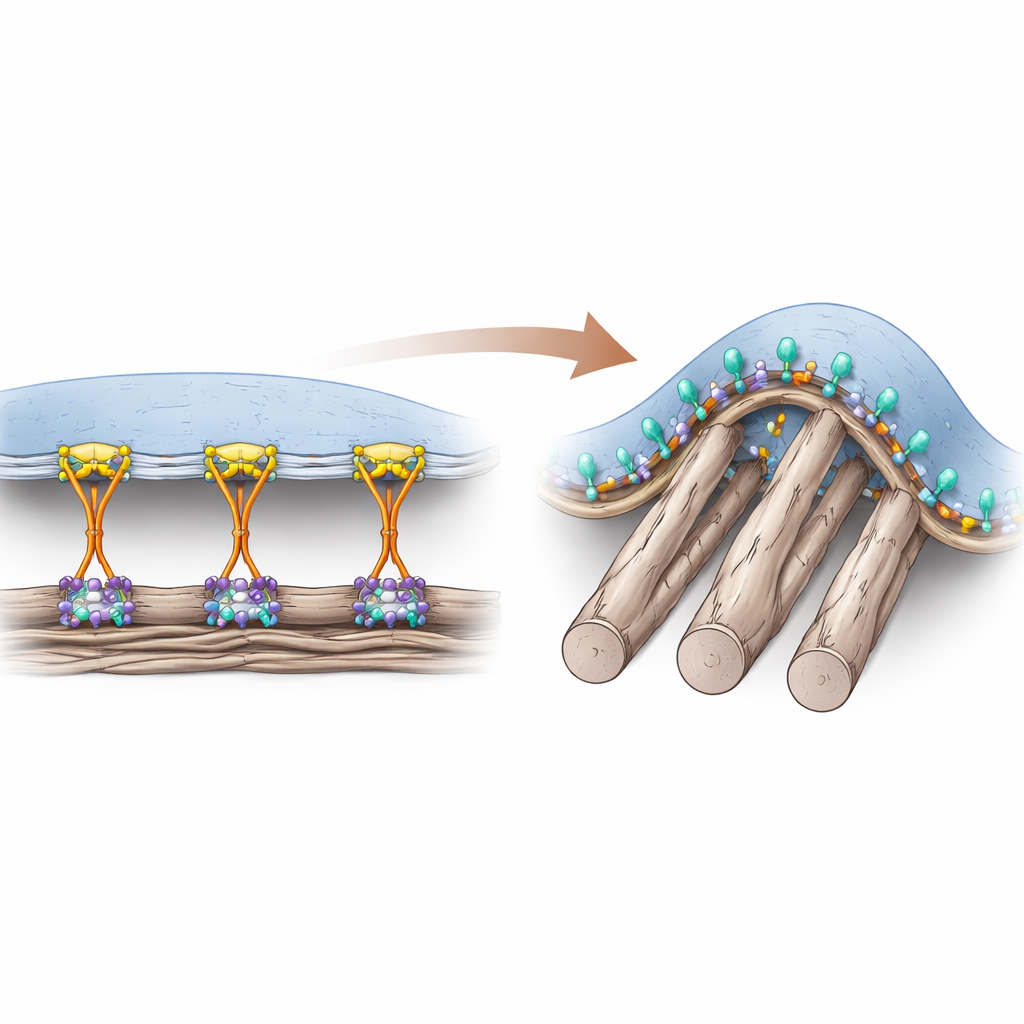
Два способа прикрепления клеток
Клетки присоединяются к белковой матрице вокруг них с помощью рецепторов на поверхности — интегринов. В течение многих лет считали, что вспомогательный белок талин абсолютно необходим для «включения» интегринов изнутри клетки, что обеспечивает прочное сцепление в классических якорных точках — фокальных адгезиях. Эти адгезии формируются преимущественно на плоских жестких поверхностях и передают большие силы через клеточный скелет. Однако в живых тканях многие окружающие волокна мягкие и цилиндрические, создавая изогнутые точки контакта, которые плохо поддерживают такие силовые структуры. Ранее авторы обнаружили другой тип адгезионной структуры — «кривую адгезию», возникающую именно там, где мембрана огибает тонкие волокна, и опирающуюся на специфический интегрин αvβ5.
Изогнутые захваты работают с другим помощником
В новом исследовании группа показывает, что талин, хотя и присутствует, не является ключевым активатором интегрина αvβ5 в кривых адгезиях. Вместо него эту роль берет на себя белок, распознающий кривизну, FCHo2. С помощью точно изготовленных нано-балок и столбиков, изгибающих мембраны клеток в контролируемых условиях, они наблюдали, что αvβ5 сильно кластируется в искривленных участках, но только если FCHo2 может связаться с очень короткой последовательностью — мотивом HDRRE — на внутреннем конце хвоста β5. При разрушении этого мотива интегрин по-прежнему функционирует в фокальных адгезиях, но уже не может формировать кривые адгезии. Подавление FCHo2 сохраняет классические фокальные адгезии в основном нетронутыми, но уничтожает кривые адгезии, тогда как удаление талина существенно ослабляет фокальные адгезии, оставляя кривые адгезии в основном неизменными.
Один аминокислотный переключатель как селектор формы
Одной из загадок было то, почему родственный интегрин αvβ3 не образует кривые адгезии, хотя его внутренний хвост похож на хвост β5. Меняя домены между двумя интегринами и вводя точечные мутации, авторы выделили одну ключевую позицию рядом с сайтом связывания талина: у большинства β-интегринов на этой позиции стоит триптофан (W), тогда как в β5 уникально присутствует тирозин (Y766). При замене тирозина в β5 на триптофан интегрин терял способность участвовать в кривых адгезиях и вел себя больше как β3, предпочитая только фокальные адгезии. Обратная замена — введение тирозина в химеру, подобную β3 — восстанавливала чувствительность к кривизне. Дальнейшие эксперименты с вариантами, имитирующими фосфорилированное или нефосфорилированное состояние этого тирозина, указывают, что его химическая модификация может смещать интегрин в сторону либо плоских, высоконапряженных фокальных адгезий, либо изогнутых, слабонапряженных адгезий.
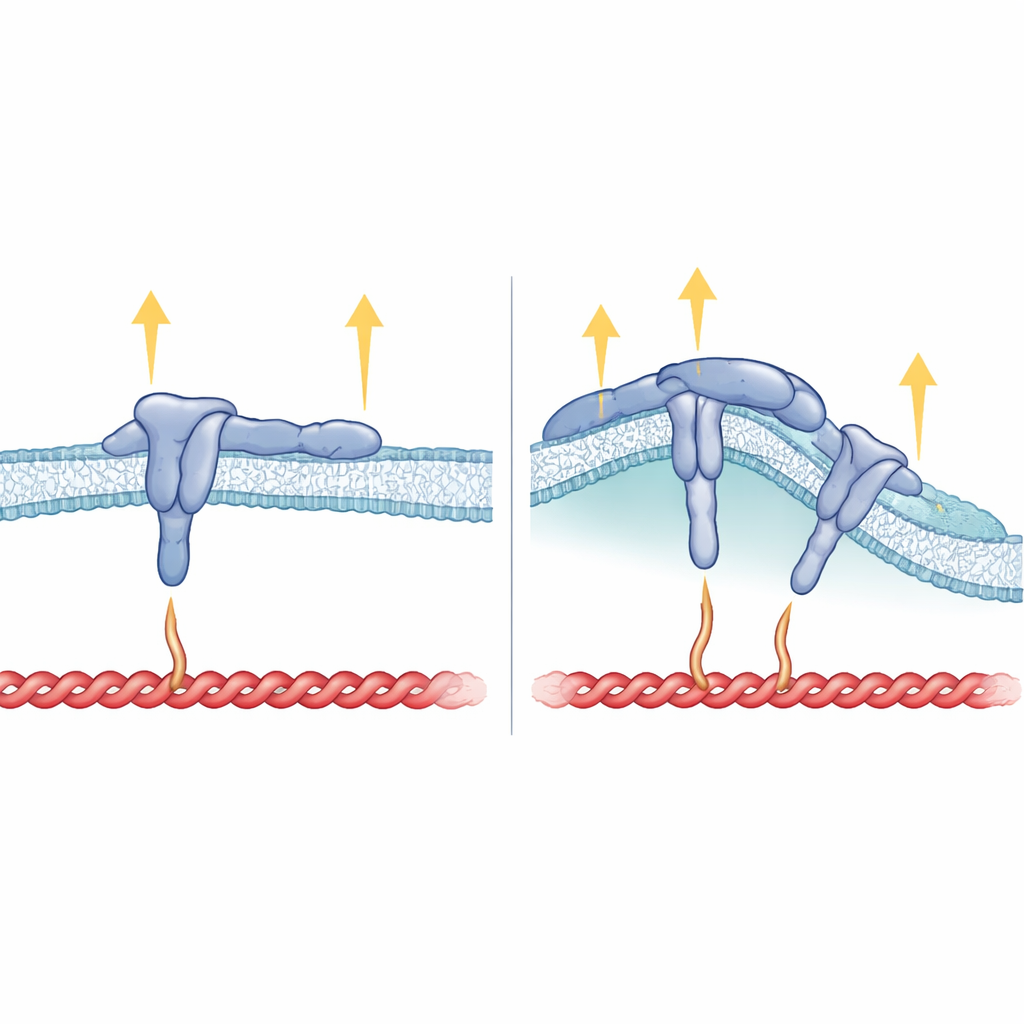
Как форма мембраны, структура интегрина и силы сочетаются
Помимо внутреннего хвоста, важную роль сыграл и участок β5, проходящий через мембрану. Когда исследователи заменили трансмембранный сегмент β5 на сегмент β3, полученный интегрин все еще мог образовывать фокальные адгезии, но больше не предпочитал изогнутые участки и не следовал за FCHo2. Это свидетельствует о том, что положение интегрина в мембране помогает ориентировать мотив HDRRE так, чтобы FCHo2 мог захватиться в изогнутых регионах и стабилизировать лигандо-связанный, активный αvβ5. В кривых адгезиях талин, по-видимому, касается лишь более отдаленной части хвоста интегрина и не испытывает большого натяжения, что объясняет отсутствие там других силовых компонентов, таких как винкулин, тензин и киндин. Напротив, в фокальных адгезиях талин захватывает и ближние, и дальние участки хвоста и мембрану, поддерживая сильные тяговые силы, но при этом блокируя доступ FCHo2 к той же области.
Что это означает для поведения клеток
Для непрофессионального наблюдателя смысл этой работы в том, что клетки имеют две отдельные «режимы захвата» для сцепления с окружением. На плоских, жестких участках они используют талин-зависимые фокальные адгезии, рассчитанные на сильное натяжение. На мягких, волокнистых и изогнутых структурах они переключаются на FCHo2-зависимые кривые адгезии, которые стабилизируют интегрин αvβ5 при гораздо меньших силах. Крошечное изменение в последовательности интегрина — и то, фосфорилирован ли этот сайт — помогает определить, какой режим будет задействован. Эта двойная система позволяет клеткам учитывать одновременно жесткость и форму в трехмерной среде, влияя на их миграцию, организацию тканей и потенциально на их инвазивность при заболеваниях.
Цитирование: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
Ключевые слова: интегрины, клеточная адгезия, кривизна мембраны, FCHo2, цитоскелет